
Badania z podwójnie ślepą próbą stanowią fundament rzetelności badań klinicznych, eliminując stronniczość i zapewniając obiektywną ocenę badanych produktów. Jednak za naukową rygorystycznością kryje się kluczowy element kreatywny – etykiety opakowań przeznaczonych do badań klinicznych. Dla artwork regulacyjnych tworzenie projektów na potrzeby badań z podwójnie ślepą próbą wymaga znalezienia równowagi między zgodnością z przepisami, poufnością a przejrzystością.
W Freyr Solutionsspecjalizujemy się w artwork zgodnej z przepisami i gotowej do audytu artwork globalnych badań klinicznych. W tym wpisie na blogu zastanawiamy się, w jaki sposób artwork opakowań do badań klinicznych artwork być dostosowana, aby spełnić specyficzne wymagania badań z podwójnie ślepą próbą.
Dlaczego Artwork w badaniach z zaślepieniem
Projektowanie etykiet opakowań do badań z podwójnie ślepą próbą (zwykle w ramach badań klinicznych) wymaga zastosowania specjalnych procedur, które pozwalają zachować ślepą próbę oraz zapewnić zgodność z wymogami regulacyjnymi i specyficznymi dla danego badania.
W odróżnieniu od produktów dostępnych na rynku, artwork badaniach z zaślepieniem muszą ukrywać tożsamość produktu, a jednocześnie zawierać jasne, zatwierdzone przez organy regulacyjne informacje dla użytkowników końcowych, takich jak badacze, farmaceuci i pacjenci. Jakakolwiek rozbieżność – czy to w kolorze, kształcie, typografii, czy treści etykiety – może nieumyślnie doprowadzić do zniesienia zaślepienia badania.
Badania Artwork metod ślepych muszą zatem mieć następujące główne cele:
- Zapewnienie ślepej próby: Etykieta nie może zawierać żadnych informacji, które mogłyby ujawnić rodzaj podawanego leku. We wszystkich grupach badanych należy zachować spójność wizualną.
- Użyteczność: Należy zapewnić bezpieczne i prawidłowe użytkowanie (np. właściwe stosowanie przez personel placówki). Należy zapobiegać rozróżnianiu produktów poprzez elementy projektu.
- Obsługa zmiennych danych: Kluczowe elementy zmiennych danych — takie jak kody randomizacji, daty ważności, numery zestawów, identyfikatory pacjentów oraz informacje dotyczące konkretnych wizyt — muszą być dostępne.
- Zgodność z przepisami: Należy przestrzegać globalnych i regionalnych przepisów dotyczących badań klinicznych
- Identyfikowalność: Należy zapewnić jednoznaczne powiązanie z badaniem i pacjentem bez ujawniania rodzaju produktu. System powinien być zarządzany wersjami i umożliwiać przeprowadzenie audytu.
Proces tworzenia etykiet opakowań do badań klinicznych z zaślepieniem
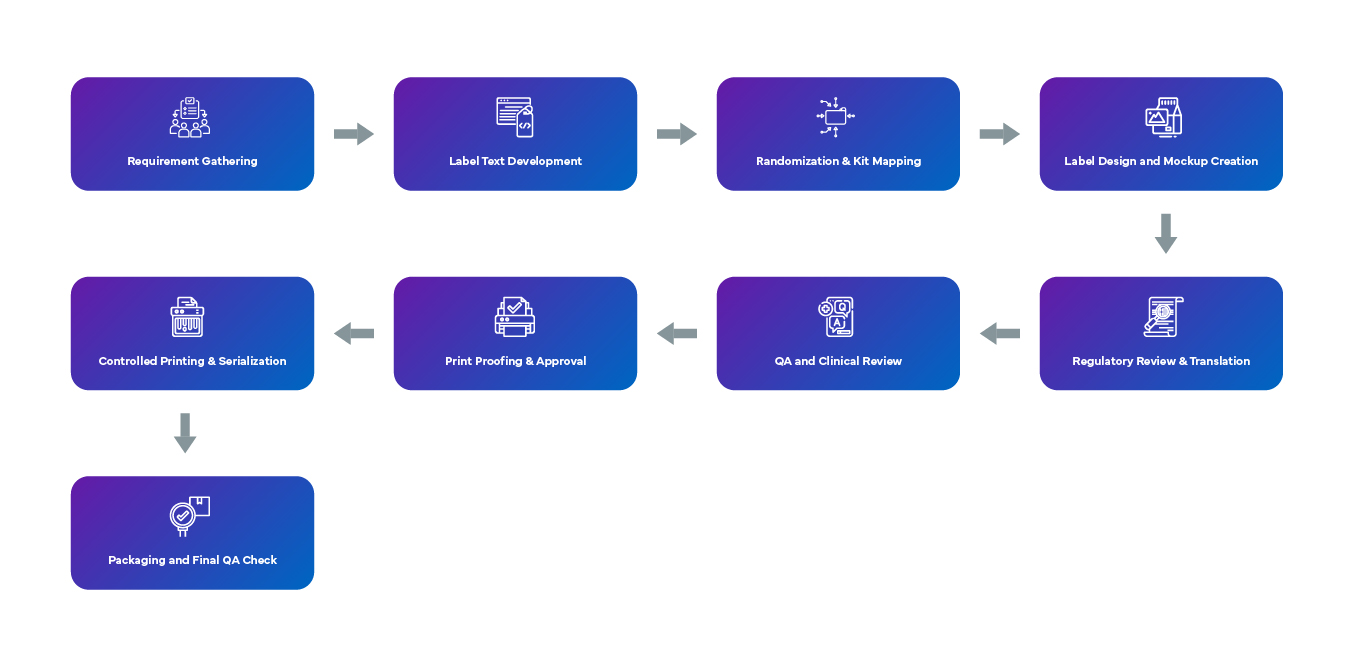
Proces projektowania etykiet ślepych rozpoczyna się od zebrania wymagań poprzez analizę protokołu i uwag interesariuszy, co gwarantuje zgodność z przepisami obowiązującymi w danym kraju. Neutralny tekst etykiety jest opracowywany z wykorzystaniem terminów takich jak „lek badany” i zawiera kluczowe informacje, takie jak numery badań, daty ważności oraz ostrzeżenia, przy jednoczesnym unikaniu elementów identyfikujących, które mogłyby ujawnić rodzaj leczenia. Randomizacja i mapowanie zestawów są obsługiwane w sposób bezpieczny, a etykiety są projektowane tak, aby zachować ślepą próbę, często z wykorzystaniem kodów kreskowych. Makiety projektowe są tworzone z uwzględnieniem rozmiaru pojemnika, potrzeb wielojęzycznych oraz wymagań dotyczących nakładek. Przeglądy regulacyjne i tłumaczeniowe zapewniają zgodność z przepisami na całym świecie. Zespoły QA kliniczne weryfikują zgodność z protokołem, a proofy etykiet przechodzą elektroniczne kontrole i formalne zatwierdzenia. Strategia nakładania etykiet — czy to pierwotnych, wtórnych, czy nakładanych na inne etykiety — uwzględnia ograniczenia środowiskowe. Kontrolowany druk, często realizowany na bieżąco, zapewnia identyfikowalność seryjną, a ostateczne pakowanie odbywa się pod QA w celu potwierdzenia dokładności etykiety, przyczepności i integralności ślepej próby.
Najważniejsze Artwork dotyczące Artwork na etykietach przeznaczonych do badań z zaślepieniem
| Artwork | Wymagania projektowe w badaniach z podwójnie ślepą próbą | Artwork Freyr |
| Schemat kolorów | Pozwala uniknąć różnic w zabarwieniu, które mogłyby wskazywać na grupy terapeutyczne | Jednolite palety kolorów we wszystkich sekcjach; preferowana skala szarości lub neutralne odcienie |
| Czcionki i typografia | Jednolity styl i rozmiar czcionki we wszystkich wariantach, aby uniknąć widocznych wskazówek | W projektach graficznych etykiet stosuje się spójne, ustalone wytyczne dotyczące typografii |
| Układ i hierarchia etykiet | Rozmieszczenie tekstu i grafiki zgodnie z wytycznymi technicznymi | Układy graficzne oparte na szablonach zapewniające spójność |
| Placebo a oznaczenie jako lek czynny | Nie mogą występować żadne różnice wizualne | Należy stosować identyczne szablony etykiet; różnią się one jedynie polami zmiennymi, w których zawarte są zakodowane dane. |
| Kody randomizacji/śledzenia | Musi być obecny, ale nie może być odczytywany przez użytkownika końcowego | Możliwość generowania dowolnych kodów kreskowych. |
| Zarządzanie językami | Treści wielojęzyczne nie powinny powodować zaburzeń układu strony | Bloki językowe mają symetryczny układ. |
| Dynamiczne pola danych | Dane takie jak numer partii, data ważności i identyfikator składnika różnią się w zależności od opakowania | Pola zastępcze lub zgodnie z ustaleniami dotyczącymi rozmieszczenia na opakowaniu |
| Materiał i format etykiety | Należy zapewnić możliwość zaślepienia i odślepienia badania zgodnie z jego wymaganiami | W razie potrzeby stosowanie etykiet w formie książeczek, etykiet samoprzylepnych lub naklejek |
| Kontrola wersji i zatwierdzanie | Etykiety są często aktualizowane w związku ze zmianami w protokołach | Scentralizowane artwork z kontrolą wersji etykiet i procesem zatwierdzania |
Odniesienia do przepisów dotyczących oznakowania badań klinicznych
Region | Organ regulacyjny | Odniesienie do wytycznych |
| UE | EMA | Załącznik VI do rozporządzenia (UE) nr 536/2014 |
| US | FDA | 21 CFR, część 312.6 |
| Wielka Brytania | MHRA | Przewodnik po dobrej praktyce klinicznej |
| Kanada | Health Canada | Wytyczne dla sponsorów badań klinicznych |
Typowe błędy w Artwork badań z grupą ślepą Artwork i jak ich unikać)
✗ Stosowanie etykiet o różnych wymiarach dla grupy aktywnej i placebo
✓ Ujednolicenie rozmiaru i kształtu we wszystkich grupach
✗ Rozmieszczenie języków różni się w zależności od kraju
✓ Należy stosować lustrzane bloki językowe o spójnym formatowaniu
✗ Widoczne identyfikatory partii/produktu na artwork produktu
✓ Należy stosować zakodowane dane i kody kreskowe w celu ukrycia widocznych identyfikatorów
Dlaczego warto nawiązać współpracę z firmą Freyr w zakresie Artwork do badań z zasłoniętymi danymi?
- Kompleksowe usługi w zakresie projektowania etykiet dla badań klinicznych o zasięgu globalnym
- Dostępność informacji dotyczących regulacji prawnych w US, Unii Europejskiej, Wielkiej Brytanii, Kanadzie oraz regionie Azji i Pacyfiku
- W razie potrzeby można skorzystać z narzędzia Artwork . Narzędzie to można dostosować do wymagań badania klinicznego.
- Pliki podlegające kontroli wersji, zgodne z wymogami i gotowe do audytu
- Obsługa wielu języków oraz korekta techniczna etykiet przeznaczonych dla dowolnego kraju lub regionu










