
W Hongkongu proces zatwierdzania leków sierocych na rzadkie choroby, zwłaszcza tych zawierających nowe jednostki chemiczne lub biologiczne (NCEs) przeznaczone do leczenia chorób zagrażających życiu lub poważnie wyniszczających, jest zarządzany przez Radę ds. Aptek i Substancji Toksycznych w Hongkongu. Poniżej przedstawiono przewodnik krok po kroku, jak przejść przez ten proces:
Przewodnik krok po kroku dotyczący procesu zatwierdzania leków sierocych przeznaczonych do leczenia rzadkich chorób
Przygotowanie i złożenie wniosku
Przygotuj wniosek wraz z niezbędnymi dokumentami:
- Raporty z oceny eksperckiej oraz dokumenty CTD dotyczące bezpieczeństwa, skuteczności i jakości
- Plany zarządzania ryzykiem (RMP)
- Etykiety produktów i ulotki informacyjne
- Raporty dotyczące oceny ryzyka związanego z zanieczyszczeniami pierwiastkowymi
- Światowy rekord rejestracji
Złóż wniosek o rejestrację za pośrednictwem Systemu Rejestracji Produktów Farmaceutycznych 2.0 (PRS 2.0) na stronie internetowej Urzędu ds. Leków. Jest to kluczowy pierwszy krok dla osób rejestrujących leki sieroce na rzadkie choroby w Hongkongu.
Uiszczanie opłat
Opłać opłatę aplikacyjną poprzez:
- PRS 2.0 (online) – kartą kredytową lub PPS
- Osobiście – gotówką lub czekiem w Urzędzie ds. Leków
- Weryfikacja i ocena
- Urząd ds. Leków przegląda wszystkie złożone dokumenty przed przyjęciem wniosku do oceny.
- W przypadku niekompletności dokumentów zostanie wystawione pismo o brakach.
- Mechanizm odmowy przyjęcia wniosku (RTF)
- Od 1 lipca 2024 r. mechanizm RTF gwarantuje, że do oceny trafiają wyłącznie kompletne i prawidłowo udokumentowane wnioski. Wnioskodawcy mają 60 dni na usunięcie wszelkich braków stwierdzonych podczas wstępnej weryfikacji.
- Niekompletne wnioski zostaną odrzucone na etapie wstępnej selekcji. Brak odpowiedzi w ciągu 60 dni spowoduje automatyczne odrzucenie wniosku.
Ulepszone procedury dla produktów NCE
W odniesieniu do NCE objętych„mechanizmem 1+”(dotyczącym chorób zagrażających życiu lub powodujących poważne upośledzenie funkcji organizmu) Rada zatwierdziła zmiany mające na celu ułatwienie i przyspieszenie procesu rejestracji – co jest szczególnie korzystne w przypadku leków na choroby rzadkie.
- Wymagania po zatwierdzeniu
- Po zarejestrowaniu produktu:
- Przestrzegaj wymogów monitorowania bezpieczeństwa stosowania produktów leczniczych
- Zgłaszaj poważne niepożądane działania leków (ADR)
- Wdrażanie i utrzymywanie planów zarządzania ryzykiem
- Po zarejestrowaniu produktu:
Odwołania
W przypadku niezadowolenia z decyzji komisji, wnioskodawca może odwołać się do Trybunału Odwoławczego ds. Farmacji i Substancji Toksycznych.
Terminy
Departament Zdrowia dąży do zakończenia procesu rejestracji w ciągu około 9 miesięcy od złożenia wniosku, pod warunkiem, że wszystkie dokumenty są kompletne. Pomaga to w skutecznym wprowadzaniu na rynek leków na choroby rzadkie.
Konsultacje i opinie
Zarząd może prowadzić konsultacje z interesariuszami i ekspertami branżowymi na etapach oceny i wdrażania polityki.
Ciągłe aktualizacje
Bądź na bieżąco, regularnie sprawdzając:
- Oficjalna strona internetowa Rady
- Ogłoszenia Urzędu ds. Leków
Schemat
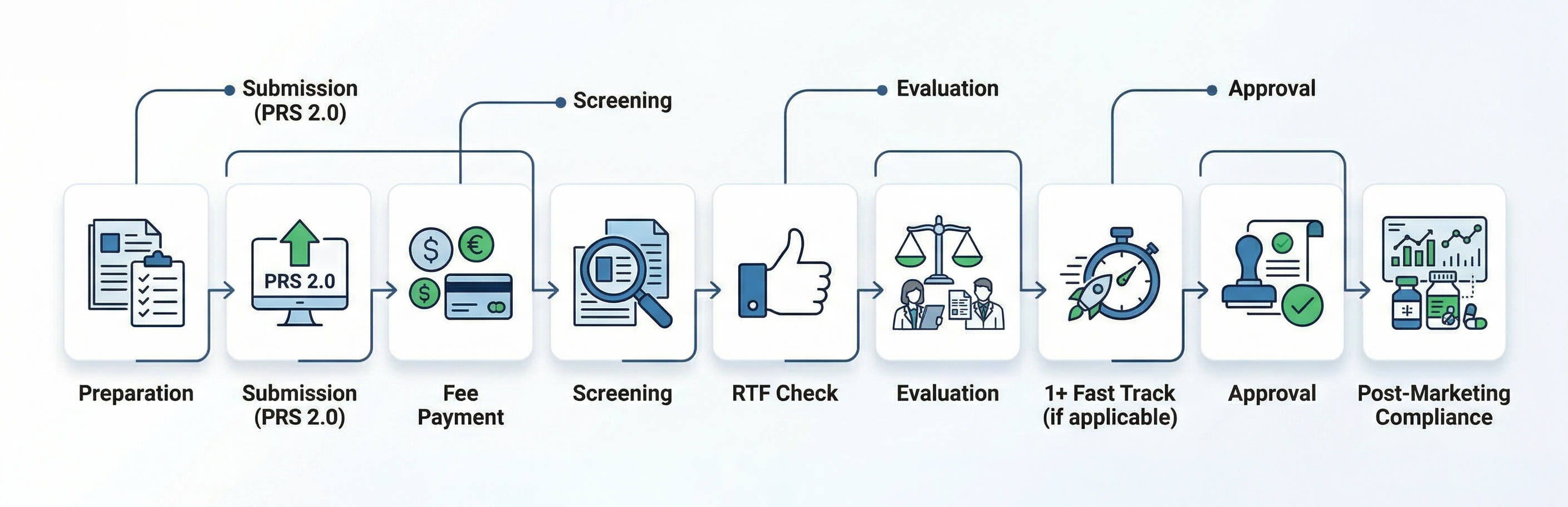
Jak Freyr może pomóc
Freyr oferuje kompleksowe wsparcie End-to-End w zakresie rejestracji leków sierocych w Hongkongu, w tym przygotowanie dokumentacji, nawigację w PRS 2.0 oraz zgodność po zatwierdzeniu. Dzięki lokalnej wiedzy i strategicznemu podejściu pomagamy zapewnić szybsze i zgodne z przepisami wprowadzenie na rynek leków sierocych na choroby rzadkie.









