
Zarządzanie zmianami po zatwierdzeniu jest istotnym, choć często pomijanym aspektem zarządzania cyklem życia produktu farmaceutycznego. Po zatwierdzeniu produktu leczniczego musi on nadal spełniać standardy regulacyjne, aby zapewnić jego bezpieczeństwo, skuteczność i jakość. Wiąże się to z wprowadzaniem niezbędnych zmian w produkcie, jego procesie wytwarzania lub opakowaniu.
Zmiany te często obejmują poprawę wydajności produkcji, rozwiązywanie problemów bezpieczeństwa lub zgodność z najnowszymi i/lub nowymi wymaganiami regulacyjnymi. Jednak zarządzanie tymi zmianami wiąże się z kilkoma ukrytymi wyzwaniami, które mogą wpłynąć na cykl życia produktu i jego obecność na rynku. W takim przedsięwzięciu niezbędna jest obecność partnera regulacyjnego, który będzie nadzorował zarządzanie procesem zmian i sprawnie prowadził operacje regulacyjne.
Wyzwania dla firmy farmaceutycznej
Poruszanie się po zmianach po zatwierdzeniu wiąże się ze złożonościami, które znacząco różnią się w zależności od regionu, tworząc przeszkody w zachowaniu zgodności. Dodatkowo, zapewnienie integralności danych, koordynacja wielu interesariuszy oraz zarządzanie obszerną dokumentacją może być zniechęcające. Nieskuteczne zarządzanie tymi aspektami może skutkować niezgodnością regulacyjną, wycofaniem produktów z rynku oraz poważnymi szkodami dla reputacji i działalności operacyjnej.
Niewiele wyzwań w zarządzaniu zmianami po zatwierdzeniu
- Złożoność regulacyjna
- Różne organy ds. zdrowia (HA) na całym świecie mają unikalne wymagania dotyczące zmian po zatwierdzeniu, co wymaga dogłębnego zrozumienia specyficznych wytycznych i terminów dla każdego regionu. Zrozumienie tych różnic jest kluczowe dla terminowego i pomyślnego składania wniosków.
- Opóźnienia w zrozumieniu tych przepisów mogą prowadzić do znaczących przeszkód w cyklu życia produktu.
- Integralność danych
- Zapewnienie dokładności i integralności danych przesyłanych w związku ze zmianami po zatwierdzeniu jest kluczowe. Niedokładne lub niekompletne dane mogą prowadzić do odrzucenia przez organy regulacyjne i znacznych opóźnień.
- Utrzymywanie wysokich standardów jakości danych wymaga rygorystycznych procesów walidacji i częstych audytów w celu zapobiegania rozbieżnościom.
- Koordynacja z interesariuszami
- Skuteczne zarządzanie zmianami po zatwierdzeniu wymaga koordynacji między zespołami wewnętrznymi (takimi jak Dział Badań i Rozwoju, produkcja i zapewnienie jakości) oraz partnerami zewnętrznymi (takimi jak organizacje produkcji kontraktowej).
- Wykorzystywanie narzędzi do zarządzania projektami i regularne spotkania międzyfunkcyjne mogą usprawnić współpracę i zapewnić zgodność wszystkich stron.
- Dokumentacja
- Szczegółowa i precyzyjna dokumentacja jest kluczowa dla wykazania zgodności i ułatwienia płynnych procesów przeglądu.
- Wręcz przeciwnie, niewłaściwe praktyki dokumentacyjne mogą prowadzić do zapytań regulacyjnych, dodatkowych żądań danych i opóźnień w składaniu wniosków.
- Zarządzanie Ryzykiem
- Proaktywne zarządzanie ryzykiem pomaga w przewidywaniu wyzwań i wdrażaniu rozwiązań, aby proces składania dokumentów przebiegał bez zakłóceń.
- Skuteczny plan zarządzania ryzykiem minimalizuje prawdopodobieństwo niepowodzeń regulacyjnych i zapewnia ciągłą zgodność.
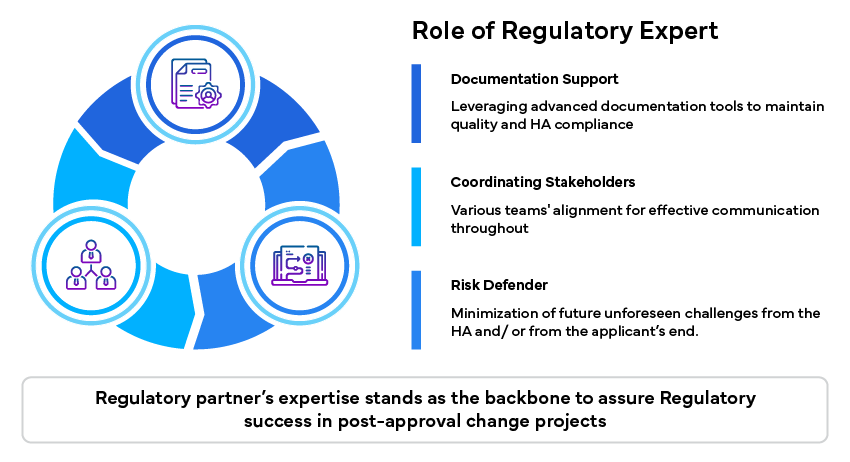
Rola eksperta regulacyjnego
Eksperci regulacyjni odgrywają znaczącą rolę w pokonywaniu tych wyzwań, zapewniając specjalistyczną wiedzę i wsparcie:
Podsumowanie
Skuteczne zarządzanie zmianami po zatwierdzeniu jest kluczowe dla utrzymania jakości, bezpieczeństwa i skuteczności farmaceutycznych produktów leczniczych. Poruszanie się po złożonościach regulacyjnych jest niezbędne do uzyskania zgód na zarządzanie zmianami od organów ds. zdrowia (HA). Eksperci regulacyjni zapewniają nieocenione wsparcie w pokonywaniu tych wyzwań, oferując swoją wiedzę, ułatwiając koordynację i ograniczając ryzyko. Wykorzystując ich możliwości, wnioskodawcy mogą zapewnić skuteczne zarządzanie zmianami po zatwierdzeniu i utrzymać obecność swoich produktów na rynku.










