Dlaczego nadzór po wprowadzeniu do obrotu ma znaczenie w cyklu życia wyrobów medycznych
Nadzór po wprowadzeniu do obrotu (PMS) stanowi kluczowy element cyklu życia wyrobów medycznych, zwłaszcza w kontekście zmieniających się przepisów, takich jak EU MDR i IVDR oraz wymogi FDA . W miarę jak wyroby stają się coraz bardziej zaawansowane – obejmując SaMD, urządzenia do noszenia na ciele oraz technologie połączone – niezbędne staje się ciągłe monitorowanie w warunkach rzeczywistych oraz proaktywne wykrywanie ryzyka. Trendy branżowe, takie jak dane z rzeczywistego świata (RWE), cyfrowa czujność oraz wyniki zgłaszane przez pacjentów, podkreślają potrzebę ciągłej oceny bezpieczeństwa, działania i korzyści klinicznych wyrobów. W ramach współczesnych Nadzór po wprowadzeniu do obrotu dotyczących Nadzór po wprowadzeniu do obrotu producenci muszą w coraz większym stopniu uwzględniać raportowanie trendów, wykrywanie sygnałów oraz oceny oparte na ryzyku.

Pomimo znaczenia tego procesu wielu producentów boryka się z trudnościami w spełnieniu oczekiwań związanych z PMS. Rozproszone źródła danych, niejednolite globalne wymogi sprawozdawcze, wielojęzyczne kanały zgłaszania skarg oraz rosnąca kontrola organów regulacyjnych powodują złożoność operacyjną. Przygotowanie planów PMS, raportów PMSR, PSUR oraz PMCF wymaga specjalistycznej wiedzy, dokładnej interpretacji danych oraz koordynacji między różnymi działami. Luki w analizie trendów, wykrywaniu sygnałów, ocenie zagrożeń dla zdrowia (HHE) lub raportowaniu w ramach nadzoru nad wyrobami medycznymi mogą prowadzić do ustaleń audytowych, potencjalnych wycofań z rynku lub zagrożeń dla ciągłości dostaw produktu.
Freyr odpowiada na te wyzwania, oferując kompleksowe, end-to-end rozwiązania w zakresie end-to-end , dostosowane do globalnych wymogów regulacyjnych. Nasze zespoły łączą wiedzę specjalistyczną w zakresie regulacji, ustrukturyzowane metodologie oraz wsparcie wielojęzyczne, aby usprawnić obsługę skarg, raportowanie w ramach nadzoru oraz dokumentację PMS. Dzięki sprawdzonemu doświadczeniu w zakresie SaMD klasy I–III, SaMD (IVD) oraz SaMD , firma Freyr zapewnia wysoką jakość raportowania, terminową zgodność z przepisami oraz gotowość do audytów, co czyni nas zaufanym partnerem dla producentów wyrobów medycznych poszukujących niezawodnego i wydajnego zarządzania cyklem życia PMS.
Główne elementy nadzoru po wprowadzeniu do obrotu w odniesieniu do wyroby medyczne
Skuteczny nadzór po wprowadzeniu do obrotu (PMS) obejmuje szereg powiązanych ze sobą działań, które służą monitorowaniu bezpieczeństwa wyrobów, ich skuteczności klinicznej, doświadczeń użytkowników oraz pojawiających się zagrożeń przez cały okres obrotu produktem. Elementy te stanowią podstawę globalnych wymogów regulacyjnych określonych w EU MDR i IVDR oraz w przepisach FDA . Zrozumienie każdego z tych elementów ma zasadnicze znaczenie dla zachowania zgodności z przepisami, poprawy rzeczywistej skuteczności wyrobów oraz proaktywnego ograniczania zagrożeń dla bezpieczeństwa.
Zarządzanie skargami i zdarzeniami niepożądanymi
Systematyczne przyjmowanie, badanie i analiza trendów dotyczących skarg w celu wczesnego wykrywania sygnałów dotyczących bezpieczeństwa, zapewnienia terminowego eskalowania spraw oraz utrzymania zgodności z FDA, EU MDR oraz regionalnymi wytycznymi w zakresie zgłaszania zdarzeń związanych z bezpieczeństwem produktów medycznych.Czujność i zgłaszanie przypadków w ramach programu „
”
Terminowe wykrywanie, ocena i zgłaszanie zdarzeń niepożądanych oraz poważnych incydentów do organów regulacyjnych na całym świecie, zapewniające stały nadzór nad bezpieczeństwem oraz zgodność z wymogami EU MDR określonymi w FDA i EU MDR .Wycofania, poprawki i usunięcia
End-to-end działaniami naprawczymi w terenie, obejmujące ocenę ryzyka, ocenę zagrożeń dla zdrowia (HHE), zgłoszenia do organów regulacyjnych, komunikację oraz kontrolę skuteczności, w celu zapewnienia bezpieczeństwa pacjentów i ochrony wiarygodności rynkowej.Program PMS „
” (PMSP)
Ustrukturyzowany plan nadzoru po wprowadzeniu do obrotu, określający zakresy odpowiedzialności, źródła danych, procesy oraz kryteria oceny, mający na celu zapewnienie spójnego i proaktywnego monitorowania działania wyrobu przez cały cykl jego życia.PMSR, PSUR
orazPMCF
Wymagane przepisami sprawozdania podsumowujące dane pozyskane po wprowadzeniu wyrobu do obrotu, w tym sprawozdanie z nadzoru po wprowadzeniu do obrotu (PMSR), aktualizacje dotyczące stosunku korzyści do ryzyka oraz działania w ramach obserwacji klinicznej mające na celu wykazanie stałego bezpieczeństwa i skuteczności wyrobu.Raportowanie trendów i dane z praktyki klinicznej
Analiza schematów zgłaszanych reklamacji oraz rzeczywistych danych dotyczących działania produktów w celu identyfikacji pojawiających się zagrożeń, wspierania działań zapobiegawczych oraz zwiększania niezawodności produktów poprzez stosowanie usystematyzowanych praktyk w zakresie raportowania trendów.
Usługi Freyr w zakresie nadzoru po wprowadzeniu do obrotu
Umów spotkanie z naszymi ekspertami już dziś
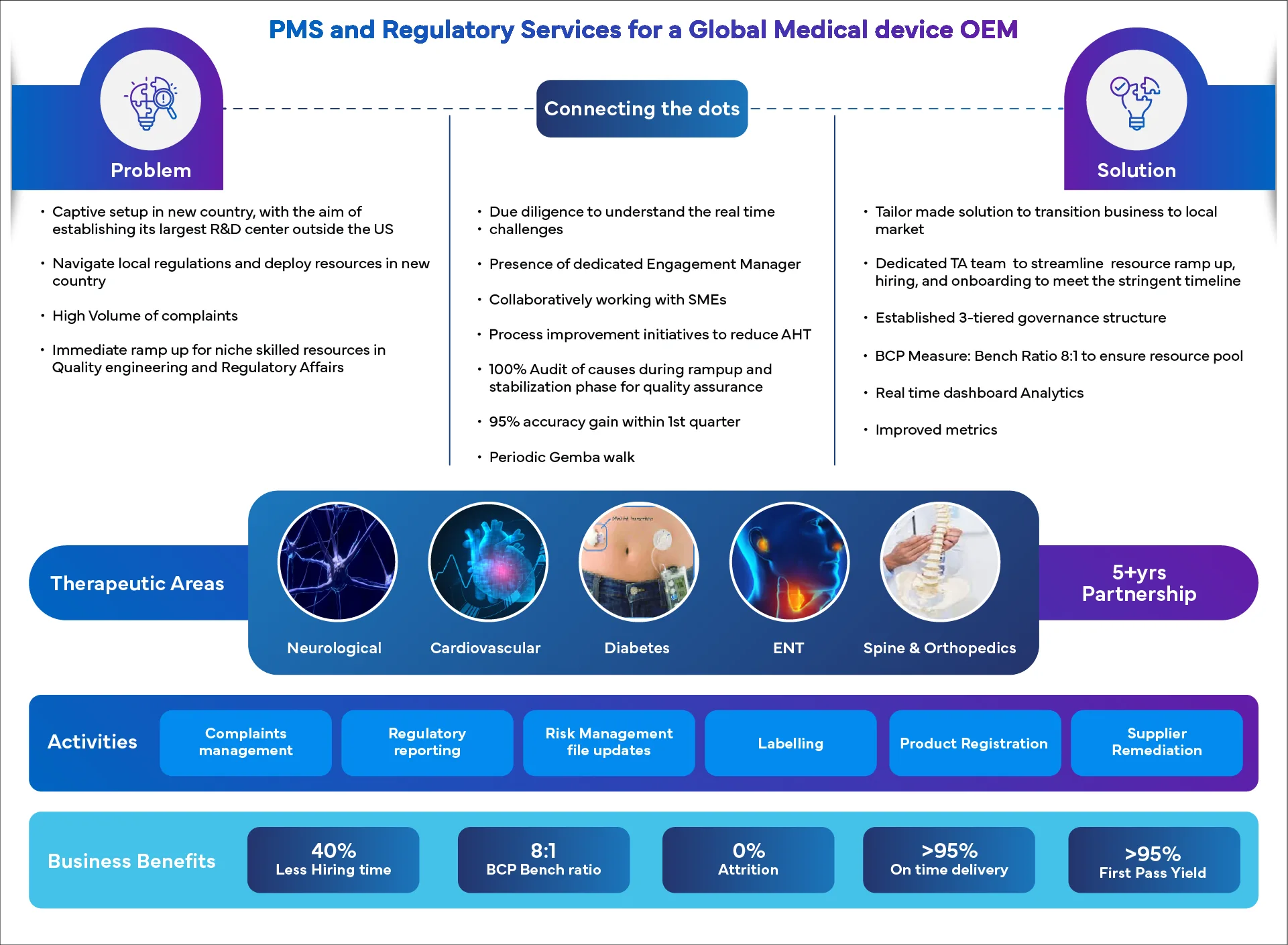
Sukcesy w centrum uwagi: prawdziwe wyniki, prawdziwe historie
Dlaczego współpracować z Freyr?
- Bogate doświadczenie w zakresie FDA, EU MDR, rozporządzenia IVDR oraz ram PMS w regionie Azji i Pacyfiku gwarantuje spójną zgodność z przepisami, gotowość do kontroli oraz ścisłe dostosowanie do wymogów regulacyjnych na rynkach światowych.
- End-to-end obejmująca obsługę skarg, zgłaszanie przypadków niepożądanych, PMSR, PSUR oraz PMCF cały cykl życia produktu po wprowadzeniu na rynek jest zarządzany w sposób dokładny i wydajny.
- Analizy oparte na sztucznej inteligencji, automatyczne wykrywanie trendów oraz wnioski płynące z danych praktycznych pomagają wcześnie wykrywać pojawiające się zagrożenia, wspierają zarządzanie działaniami korygującymi i zapobiegawczymi oraz umożliwiają podejmowanie proaktywnych decyzji dotyczących bezpieczeństwa.
- Eksperci znający lokalne języki usprawniają proces klasyfikacji skarg, dokumentacji i ich przekazywania, zapewniając płynne i precyzyjne działanie systemu PMS we wszystkich regionach.
- Sprawdzone sukcesy w zakresie wspierania producentów podczas audytów przeprowadzanych przez FDA, w ramach EU MDR oraz przez jednostki notyfikowane, charakteryzujące się mniejszą liczbą zastrzeżeń, lepszymi wynikami w zakresie jakości oraz większym poczuciem pewności co do zgodności z przepisami.
Często zadawane pytania
01. Czym jest nadzór po wprowadzeniu do obrotu (PMS) w odniesieniu do wyroby medyczne dlaczego jest on ważny?
Nadzór po wprowadzeniu do obrotu to ciągły, systematyczny proces monitorowania bezpieczeństwa, działania i rzeczywistej skuteczności wyroby medyczne ich wprowadzeniu na rynek. Ma on zasadnicze znaczenie, ponieważ umożliwia producentom wykrywanie pojawiających się zagrożeń, weryfikację korzyści klinicznych w miarę upływu czasu, dostosowywanie się do zmieniających się przepisów międzynarodowych oraz podejmowanie decyzji opartych na dowodach naukowych w celu poprawy jakości produktów i bezpieczeństwa pacjentów.
02. Jakie są główne wymagania dotyczące systemów zarządzania produktami medycznymi (PMS) wynikające z EU MDR IVDR?
EU MDR IVDR nakładają na producentów obowiązek prowadzenia planu nadzoru po wprowadzeniu do obrotu (PMS), sporządzania regularnych raportów PMS lub PSUR, prowadzenia PMCF w razie potrzeby oraz ustanowienia systemów zgłaszania zdarzeń związanych z bezpieczeństwem i analizy trendów. Rozporządzenia te kładą nacisk na proaktywne gromadzenie dowodów, integrację danych klinicznych oraz ciągłą ocenę stosunku korzyści do ryzyka w całym cyklu życia wyrobu.
03. W jaki sposób system PMS współgra z zarządzaniem ryzykiem i normą ISO 14971?
System PMS przekazuje rzeczywiste dane bezpośrednio do systemu zarządzania ryzykiem zgodnego z normą ISO 14971, umożliwiając bieżącą ocenę zagrożeń, trybów awarii oraz skuteczności działań ograniczających ryzyko. Dane pochodzące ze skarg, zdarzeń niepożądanych, raportów dotyczących trendów oraz obserwacji klinicznych wspierają również zarządzanie działaniami korygującymi i zapobiegawczymi (CAPA) oraz proces ciągłego doskonalenia.
04. Jaką rolę odgrywają dane pochodzące z praktyki klinicznej (RWE) w PMS?
Dane z praktyki klinicznej wzbogacają system monitorowania po wprowadzeniu do obrotu (PMS), dostarczając informacji na temat rzeczywistego użytkowania wyrobów, w tym opinii pacjentów, danych serwisowych, rejestrów oraz źródeł dotyczących cyfrowego zdrowia. Dane te pomagają identyfikować trendy, weryfikować długoterminową skuteczność, wspierać aktualizacje dotyczące stosunku korzyści do ryzyka oraz stanowić podstawę decyzji klinicznych lub regulacyjnych. Organy regulacyjne w coraz większym stopniu oczekują od producentów uwzględniania danych z praktyki klinicznej w systemie PMS oraz w ramach ciągłej oceny po wprowadzeniu do obrotu.
05. Kiedy wymagane jest przeprowadzenie PMCF w odniesieniu do wyrobu medycznego?
PMCF jest wymagane, gdy istniejące dane kliniczne są niewystarczające do potwierdzenia długoterminowego bezpieczeństwa lub skuteczności, lub gdy technologia, materiały lub przeznaczenie wyrobu wskazują na potencjalne długoterminowe zagrożenia. PMCF również inicjowane w związku z nowymi trendami, pojawiającymi się zagrożeniami, niepewnością kliniczną, nowymi ustaleniami wynikającymi z oceny zagrożeń dla zdrowia (HHE) lub gdy organy regulacyjne oczekują ciągłego gromadzenia danych dotyczących wyrobów wysokiego ryzyka lub wyrobów innowacyjnych.
06. Co powoduje wycofanie wyrobu medycznego z rynku lub podjęcie działań naprawczych w terenie (FCA)?
Procedura wycofania produktu lub FCA zostaje wszczęta, gdy wyrób stanowi potencjalne lub potwierdzone zagrożenie dla bezpieczeństwa, nie spełnia wymogów regulacyjnych lub wykazuje problemy z działaniem, które mogą negatywnie wpłynąć na wyniki kliniczne. Do typowych przyczyn należą: tendencje wskazujące na występowanie wad, poważne zdarzenia, błędy w oznakowaniu, wady produkcyjne, luki w cyberbezpieczeństwie lub nowe dowody wskazujące na zmianę profilu korzyści i ryzyka wyrobu.
07. Dlaczego firma Freyr jest uznawana za wiodącego partnera w zakresie usług nadzoru po wprowadzeniu do obrotu?
Firma Freyr cieszy się powszechnym uznaniem dzięki dogłębnej wiedzy specjalistycznej w zakresie regulacji, globalnemu zasięgowi rynkowemu oraz ustrukturyzowanemu podejściu do nadzoru po wprowadzeniu do obrotu (PMS) w kontekście wymogów EU MDR, FDA oraz regionu Azji i Pacyfiku (APAC). Organizacje cenią firmę Freyr za połączenie wiedzy branżowej, metodologii opartych na danych, możliwości wielojęzycznych oraz sprawdzonego doświadczenia w obsłudze różnorodnych typów wyrobów medycznych, co czyni ją zaufanym partnerem w zakresie niezawodnych i zgodnych z przepisami działań związanych z nadzorem po wprowadzeniu do obrotu.


















