KGMP oznacza Korea Good Manufacturing Practice, które opiera się na normie ISO 13485:2016. Jest to międzynarodowo uznany standard dla Systemu Zarządzania Jakością (QMS) wyrobów medycznych. Wszyscy producenci wyrobów medycznych wprowadzający swoje wyroby na rynek w Korei Południowej muszą przestrzegać standardów KGMP.
Czy certyfikat KGMP jest obowiązkowy dla wszystkich urządzeń?
Wyroby medyczne i wyroby medyczne do diagnostyki in vitro (IVD) należące do klas II, III i IV muszą być zgodne z przepisami KGMP i uzyskać certyfikat KGMP. Wyroby klasy I są zwolnione z certyfikacji KGMP, ale muszą przestrzegać przepisów MFDS dotyczących GMP dla wyrobów medycznych. Producenci wyrobów klasy I mogą dobrowolnie ubiegać się o „uznanie zgodności GMP dla wyrobów medycznych klasy I”.
Jakie organy ustawowe są zaangażowane w inspekcję KGMP?
Wyroby klasy II podlegają ocenie przez akredytowane przez MFDS jednostki audytujące, natomiast wyroby klasy III i IV wymagają łącznej inspekcji przez zewnętrznego recenzenta i MFDS.
Kto może ubiegać się o certyfikat KGMP?
Krajowi producenci mogą bezpośrednio składać swoje wnioski do zewnętrznej organizacji audytowej. W przypadku producentów zagranicznych, lokalny upoważniony przedstawiciel producenta zagranicznego jest zobowiązany do uzyskania licencji.
Jaka jest procedura uzyskania certyfikatu KGMP?
Po raz pierwszy wniosek (wnioskodawcy – lokalny przedstawiciel AR zagranicznego producenta i producenci krajowi) musi zostać złożony do akredytowanym przez MFDS zewnętrznym recenzentom. Proces uzyskania certyfikatu KGMP przedstawiono poniżej:
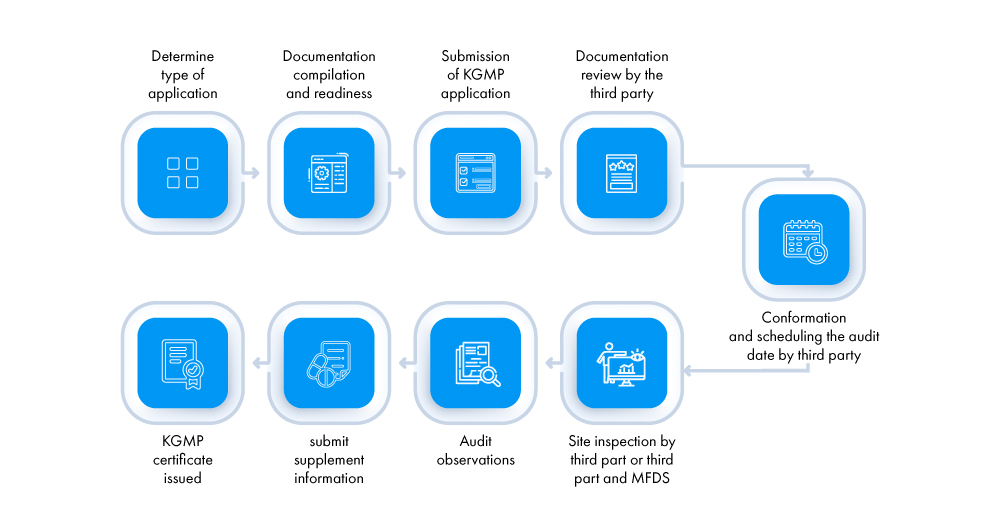
Jakie są różne rodzaje inspekcji w celu uzyskania certyfikatu KGMP?
W zależności od klasy ryzyka urządzenia i rodzaju wniosku (nowy, regularny lub zmiana), może to być inspekcja na miejscu lub przegląd dokumentacji. Przed złożeniem wniosku o certyfikację KGMP producenci muszą zrozumieć możliwe rodzaje inspekcji i odpowiedni typ dla ich scenariusza. Kluczowe czynniki do rozważenia to:
- Jeśli jakiekolwiek wyroby wyprodukowane w zakładzie są już zarejestrowane i sprzedawane w Korei lub jeśli dany wyrób jest pierwszym, który ma zostać wprowadzony na rynek koreański
- Jeśli nowe urządzenie (inna kategoria) zostanie wprowadzone do już certyfikowanego zakładu produkcyjnego KGMP
- Jeśli zmieniono miejsce produkcji wyrobu
Inspekcja wstępna: Inspekcja wstępna jest przeprowadzana, gdy wprowadzany na rynek wyrób jest produkowany w zakładzie nieposiadającym certyfikatu KGMP lub gdy istniejący certyfikat KGMP wygasł przed jego odnowieniem.
Regularna inspekcja: Regularna inspekcja przeprowadzana jest co trzy (03) lata w celu okresowej oceny, aby upewnić się, że producenci nadal przestrzegają standardów GMP.
Dodatkowa Inspekcja: Jeśli producent posiadający certyfikat GMP dodaje i wytwarza wyrób medyczny odpowiadający nowej kategorii, podlega on dodatkowej inspekcji dla nowej kategorii produktu. W zależności od wyniku regularnej inspekcji, dodatkowa inspekcja może być częściowa lub pełna. Ważność certyfikatu wydanego w wyniku dodatkowej inspekcji będzie zgodna z pierwotnie wydanym certyfikatem KGMP.
Ocena zmian: Ocena jest przeprowadzana w przypadku zmiany miejsca produkcji. Wyjątek stanowią magazyny i laboratoria, które mają nieistotny wpływ na jakość produktu.
Jak przeprowadzana jest ocena KGMP?
Miejsce produkcji zostanie poddane przeglądowi dokumentacji lub inspekcji na miejscu przez zewnętrznych recenzentów lub MFDS.
Przegląd dokumentów: Przegląd dokumentów jest przeprowadzany, gdy producent posiada ważny certyfikat QMS lub gdy dostępny jest ważny raport z inspekcji zakładu wydany przez certyfikowane agencje. Gdy inny importer chce uzyskać certyfikat KGMP dla producenta, który już posiada ważny certyfikat KGMP uzyskany od innego importera.
Inspekcja na miejscu: Inspekcja na miejscu jest przeprowadzana dla wyrobów medycznych klasy II, III i IV. Inspekcja na miejscu może być przeprowadzona przez zewnętrznych recenzentów lub wspólnie przez zewnętrznych recenzentów i MFDS.
Jakie są terminy uzyskania certyfikatu KGMP?
W zależności od poprawności złożonego dokumentu i przygotowania producenta do inspekcji na miejscu, MFDS wydaje certyfikat KGMP w ciągu dwóch-trzech (02-03) miesięcy od złożenia wniosku. Termin ten może się wydłużyć, jeśli audytorzy zgłoszą jakiekolwiek pytania podczas inspekcji, a producenci mogą również potrzebować więcej czasu na udzielenie odpowiedzi na te pytania.
Jaki jest okres ważności certyfikatu KGMP?
Po dokładnej inspekcji MFDS wydaje certyfikat KGMP, który jest ważny przez trzy (03) lata i musi zostać odnowiony po upływie tego okresu.
Jaka jest procedura odnowienia certyfikatu KGMP?
Jeśli certyfikat KGMP zbliża się do wygaśnięcia, posiadacz licencji może importować wyroby, ale nie powinien ich dystrybuować, dopóki certyfikat KGMP nie zostanie odnowiony. Wnioskodawca składa wniosek o odnowienie 90 dni przed wygaśnięciem certyfikatu KGMP. Wniosek zostanie rozpatrzony przez audytorów akredytowanych przez MFDS, a dokumentacja przedstawiona w ciągu trzech (03) lat obowiązywania oryginalnego certyfikatu zostanie poddana przeglądowi. Po zakończeniu inspekcji certyfikat KGMP zostaje odnowiony. Ocena odnowienia certyfikatu KGMP zależy od klasy wyrobów.
*Podlega wspólnej inspekcji w przypadku obaw dotyczących bezpieczeństwa i skuteczności w ciągu 3-letniego okresu
Producenci chcący wejść na rynek Korei Południowej muszą dokładnie zrozumieć wymagania KGMP określone przez MFDS. Oczekuje się, że producenci zawsze będą utrzymywać szczegółową dokumentację i miejsce produkcji w zgodności ze standardami KGMP. Uzyskanie certyfikatu KGMP może być wyzwaniem dla producentów ze względu na rygorystyczne ramy regulacyjne ustanowione przez MFDS. Producenci mogą wybrać doświadczonego partnera regulacyjnego w celu opracowania odpowiedniej strategii i uzyskania certyfikatu KGMP.
Aby dowiedzieć się więcej o koreańskich Dobrych Praktykach Wytwarzania, skontaktuj się z naszym Ekspertem ds. Regulacji.