Innowacyjne wyroby medyczne są niezbędne do poprawy wyników opieki zdrowotnej, zaspokajania zmieniających się potrzeb medycznych oraz dostarczania ekonomicznych rozwiązań dla pacjentów i świadczeniodawców opieki zdrowotnej. Strategia SAKIGAKE to przyspieszony proces przeglądu i zatwierdzania innowacyjnych wyrobów medycznych w Japonii. Strategia ta została zainicjowana przez japońskie Ministerstwo Zdrowia, Pracy i Opieki Społecznej (MHLW) w 2015 roku, w celu przyspieszenia rozwoju i komercjalizacji innowacyjnych wyrobów medycznych w Japonii.
Zgodnie ze strategią SAKIGAKE, wyroby medyczne spełniające określone kryteria innowacyjności mogą otrzymać priorytetową ocenę i zatwierdzenie przez Agencję ds. Produktów Farmaceutycznych i Wyrobów Medycznych (PMDA), Agencję Regulacyjną odpowiedzialną za zatwierdzanie wyrobów medycznych w Japonii. Kryteria kwalifikacji dla innowacji obejmują:
- Wyroby o znaczącej skuteczności; oczekuje się, że wyrób zapewni znaczące korzyści kliniczne dzięki nowatorskiemu mechanizmowi działania i radykalnej poprawie dla pacjentów w porównaniu do istniejących wyrobów medycznych.
- Po pierwsze, urządzenie ma zastosowanie do zatwierdzeń w Japonii lub jednocześnie w Japonii i innych krajach.
- Urządzenie ma potencjał, aby sprostać niezaspokojonym potrzebom medycznym w Japonii. Docelowy stan medyczny powinien być poważny, zagrażający życiu lub charakteryzujący się uporczywymi objawami.
W ramach strategii SAKIGAKE, producenci wyrobów medycznych mogą uzyskać szereg korzyści, w tym:
- Priorytetowa konsultacja: Skrócenie czasu oczekiwania na konsultację dotyczącą badania klinicznego do jednego (01) miesiąca.
- Priorytetowa ocena: Produkty objęte programem SAKIGAKE podlegają priorytetowej ocenie, której celem jest zakończenie procesu oceny w ciągu sześciu (06) miesięcy zamiast 12 miesięcy.
- Skuteczna weryfikacja przed złożeniem wniosku: Zachęcanie do konsultacji i akceptowanie materiałów w języku angielskim.
- Dedykowany Partner ds. Oceny: Każdy produkt oznaczony jako SAKIGAKE ma przypisanego dedykowanego menedżera ds. oceny na cały proces zatwierdzania.
- Wzmocnienie środków bezpieczeństwa po wprowadzeniu do obrotu: Przedłużenie okresu ponownej oceny i ułatwienie nawiązywania kontaktów ze stowarzyszeniami naukowymi.
Jak aplikować?
- Przez wnioskodawcę: Wnioskodawca składa wniosek do Działu Oceny i Licencjonowania PMDA (ELD).
- Przez PMDA-ELD: ELD kontaktuje się z potencjalnym wnioskodawcą.
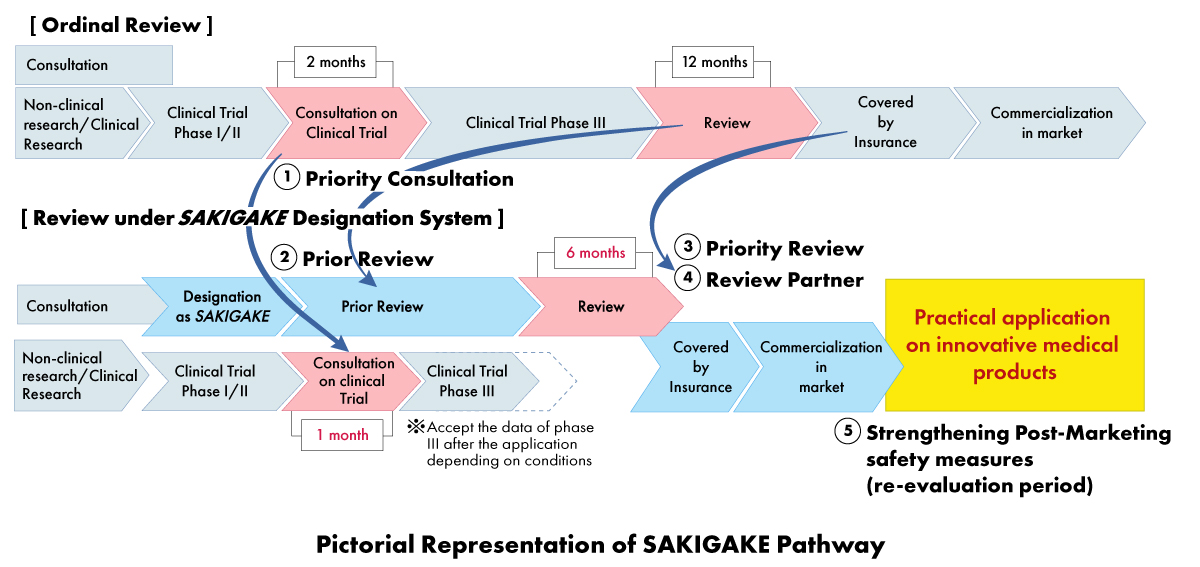
P.C- PMDA, Japonia.
Ogólnie rzecz biorąc, system SAKIGAKE zapewnia przyspieszoną ścieżkę rozwoju i zatwierdzania innowacyjnych wyrobów medycznych w Japonii. Ma na celu poprawę wyników leczenia pacjentów i promowanie innowacji w branży wyrobów medycznych. Producent musi skonsultować się z PMDA na wczesnym etapie procesu rozwoju, aby omówić wymagania regulacyjne i otrzymać informację zwrotną na temat swoich planów rozwoju produktu.
Aby dowiedzieć się więcej o ścieżkach rejestracji wyrobów medycznych w Japonii, skontaktuj się z ekspertem regulacyjnym już teraz! Bądź na bieżąco. Bądź zgodny z przepisami.
