Visão Geral do Registo de Dispositivos Médicos na Colômbia
A Colômbia oferece grandes oportunidades para as empresas de dispositivos médicos e o seu sistema de saúde é reconhecido pelo seu compromisso com a segurança do paciente e a qualidade dos serviços médicos. O país regulamenta os dispositivos médicos através do INVIMA (Instituto Nacional de Vigilância de Alimentos e Medicamentos). O INVIMA é a autoridade operacional para o registo de dispositivos médicos na Colômbia.

Autoridade Regulamentar: INVIMA (Instituto Nacional de Vigilância de Alimentos e Medicamentos)
Regulamento: Decreto 4725/2005
Via Regulamentar: Registo de Dispositivos
Representante Autorizado: Representante Legal na Colômbia
Requisito de QMS: ISO 13485:2016 / MDSAP
Avaliação de Dados Técnicos: INVIMA
Requisitos de Rotulagem: Os documentos de rotulagem devem estar em espanhol
Validade da Licença: 10 anos
Formato de Submissão: Eletrónico
Classificação de Dispositivos Médicos na Colômbia
| Classificação de Dispositivos Médicos | |
|---|---|
| Classe I (Risco mais baixo) | |
| Classe IIa | |
| Classe IIb | |
| Classe III (Risco mais elevado) | |
Representante Legal na Colômbia
Para ser um Representante Legal na Colômbia, é necessário possuir cidadania colombiana ou a autorização legal necessária para residir e trabalhar no país como cidadão estrangeiro. Um Representante Legal pode auxiliar e gerir todos os procedimentos de registo na Colômbia, atuando como elo de ligação entre a empresa e o INVIMA, a autoridade regulamentar local.
Registo de Dispositivos Médicos na Colômbia
Os Dispositivos Médicos e os IVDs estão sujeitos ao procedimento de registo, pelo que os Dispositivos Médicos devem ser registados junto do INVIMA para serem comercializados na Colômbia.
Para comercializar um dispositivo médico na Colômbia, é necessário obter um Certificado de Livre Venda (CFS) ou um Certificado para Governo Estrangeiro (CFG), emitido pela agência regulamentar apropriada no país de origem ou num país de referência reconhecido (por exemplo, Canadá, Japão, Austrália, União Europeia e Estados Unidos). O Certificado de Livre Venda ou o Certificado para Governo Estrangeiro serve como prova de que o dispositivo médico cumpre as normas de segurança e qualidade necessárias para venda na Colômbia.
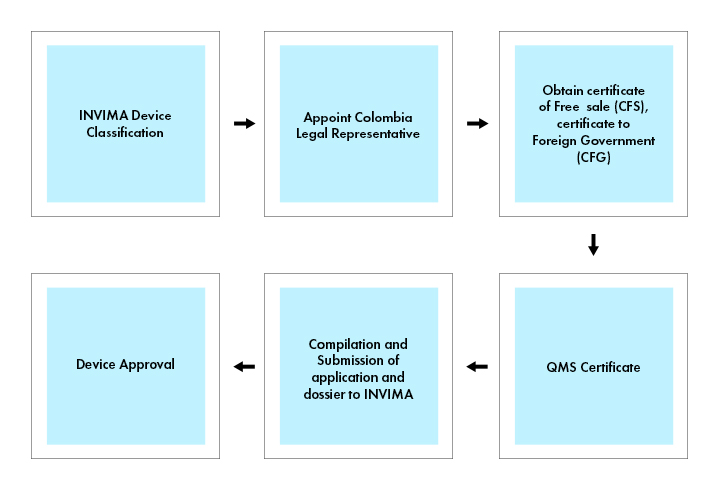
Fluxo do processo
Gestão do Ciclo de Vida do Dispositivo Pós-Aprovação
A Freyr apoia os fabricantes estrangeiros na gestão End-to-End do ciclo de vida de dispositivos médicos, incluindo atividades pós-aprovação, tais como:
- Gestão de alterações pós-aprovação - modificações às aprovações de dispositivos médicos existentes, tais como, adição de novas variantes, acessórios; adição de novas indicações de utilização, entre outras
- Manutenção das aprovações e do registo através do pagamento atempado das taxas administrativas e de registo
- Renovação de licenças
- Ligação entre o INVIMA e o fabricante
Resumo
| Classificação de Dispositivos Médicos | Novas licenças e Renovações | ||
|---|---|---|---|
| Novo registo | Alteração | Renovação | |
| Classe I | 4-6 Meses | 2-3 Meses | 4-6 Meses |
| Classe IIa | 4-6 Meses | 2-3 Meses | 4-6 Meses |
| Classe IIb | 4-6 Meses | 2-3 Meses | 4-6 Meses |
| Classe III | 4-6 Meses | 2-3 Meses | 4-6 Meses |
| Taxas de Registo | |||||
|---|---|---|---|---|---|
| Novas licenças e Renovações | Modificações Técnicas | Modificações Administrativas | |||
| Classe I e Classe IIa | Classe IIb e Classe III | Classe I e Classe IIa | Classe IIb e Classe III | Classe I e Classe IIa | Classe IIb e Classe III |
| $ 690,00 | $ 776,00 | $ 196,00 | $ 196,00 | $ 153,00 | $ 153,01 |
Experiência Freyr
- Due Diligence Regulamentar
- Classificação Oficial
- Registo de Dispositivos
- Titular do Registo na Colômbia
- Apoio à Rotulagem
- Apoio à Tradução
- Identificação e qualificação de distribuidores
- Vigilância Pós-Comercialização
- Gestão de Alterações Pós-Aprovação
- Renovação e transferência de licenças
- Submissão e ligação com o INVIMA