Evolução dos Genéricos - Visão Geral
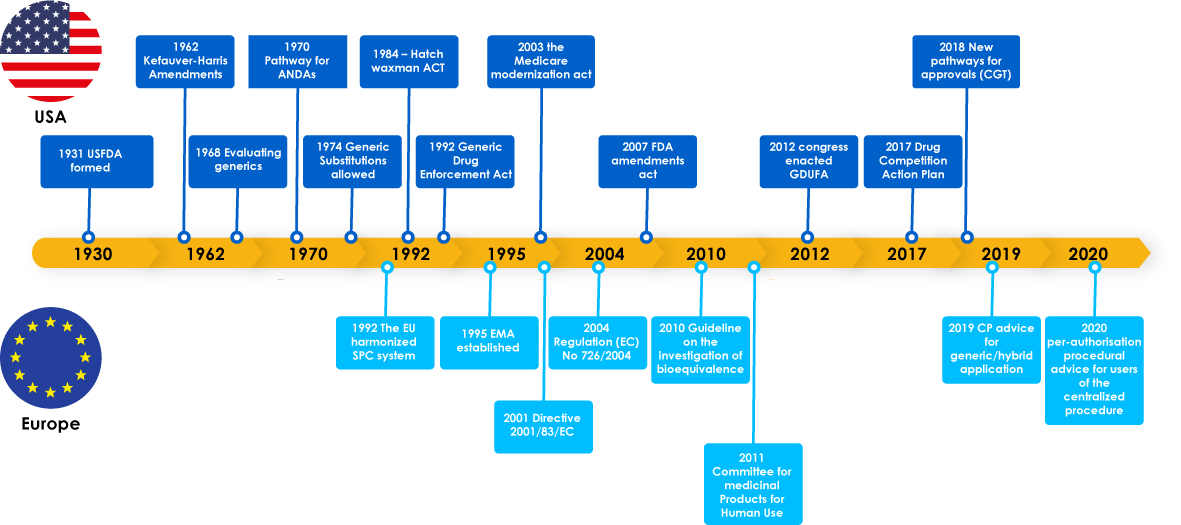
Os medicamentos genéricos alcançaram marcos importantes, incluindo leis de regulamentação para apoiar o seu desenvolvimento, o que incentivou os fabricantes a explorar o mercado de genéricos. Estas legislações também deram aos médicos confiança para prescrever um substituto para um medicamento de marca e, por fim, beneficiaram os doentes, uma vez que os fabricantes de genéricos satisfizeram necessidades cruciais de doentes em todo o mundo.
Perguntas Frequentes sobre Genéricos
P1: O que são medicamentos genéricos?
Resp: Os medicamentos genéricos são medicamentos farmacêuticos, que são cópias idênticas do medicamento original e têm o mesmo API, dosagem, uso pretendido, efeitos secundários, via de administração, riscos, segurança e potência que o medicamento inovador, mas podem diferir em algumas características, como o processo de fabrico, formulação, excipientes, cor, sabor e embalagem. Por outras palavras, um medicamento genérico é terapeuticamente equivalente a um medicamento de marca e, portanto, pode ser substituído pelo seu equivalente de marca.
P2: Porque é que os medicamentos genéricos custam menos do que um medicamento inovador?
Resp: Os medicamentos genéricos são mais económicos em comparação com o medicamento inovador, porque os medicamentos genéricos não têm de repetir os estudos pré-clínicos e clínicos dispendiosos e demorados, que são exigidos para os medicamentos inovadores demonstrarem segurança e eficácia e, em vez disso, os medicamentos genéricos precisam apenas de provar a equivalência farmacêutica para o seu produto.
Q3: Os medicamentos genéricos são tão bons como o medicamento inovador?
Resp: Sim, os medicamentos genéricos têm a mesma qualidade, eficácia e são tão seguros quanto os medicamentos de marca. O preço mais baixo destes medicamentos não indica que sejam de qualidade inferior, porque os medicamentos genéricos, tal como os medicamentos de marca, têm de passar por um rigoroso processo de aprovação para comercializar o seu medicamento e as empresas farmacêuticas são obrigadas a apresentar a submissão do medicamento genérico, demonstrando que o seu medicamento tem o mesmo benefício clínico que os medicamentos de marca e são adequados para serem utilizados como substitutos dos respetivos medicamentos de marca.
P4: Porque é que os medicamentos genéricos têm um aspeto diferente do medicamento de marca?
Resp: Os medicamentos genéricos devem ser bioequivalentes aos medicamentos de marca e ter o mesmo API que os medicamentos inovadores. No entanto, podem existir pequenas diferenças nos medicamentos genéricos relativamente à forma, rotulagem (pequenas diferenças), embalagem e ingredientes inativos, como cor, sabores e conservantes; mas a eficácia do medicamento deve permanecer a mesma.
P5: O que está envolvido na revisão e aprovação de submissões de medicamentos genéricos nos US?
Resp: Qualquer empresa farmacêutica que pretenda comercializar o seu medicamento genérico nos US deve cumprir todos os requisitos regulamentares da US FDA para a submissão de medicamentos genéricos e deve demonstrar que:
- O medicamento genérico é “equivalente farmacêutica/terapeuticamente” à marca
- O fabricante é capaz de produzir o medicamento de forma correta e consistente.
- O “ingrediente ativo” é o mesmo que o da marca.
- A quantidade certa do ingrediente ativo chega ao local no corpo onde tem efeito.
- Os ingredientes "inativos" do medicamento são seguros
- O medicamento não se degrada com o tempo.
- O recipiente em que o medicamento será enviado e vendido é adequado.
- O rótulo é o mesmo que o rótulo do medicamento de marca.
- Patentes relevantes ou exclusividades legais caducaram
P6: Cada medicamento de marca tem um medicamento genérico?
Resp: Não. Nem todos os medicamentos de marca têm uma versão genérica. Novos medicamentos são fabricados sob proteção de patente por um período de até vinte (20) anos. Isto significa que nenhum outro medicamento pode ser fabricado e comercializado durante este período, até à expiração da patente. No entanto, alguns medicamentos podem nunca ter versões genéricas para o seu produto, devido à dificuldade de fabrico ou caso o medicamento genérico possa ser considerado não lucrativo.








