MLR sobre materiais promocionais - Visão geral
O sucesso do lançamento de produtos e a entrada eficaz no mercado de Medicamentos dispositivos médicos dependem da sinergia entre equipas Assuntos Regulamentares promocionais altamente competentes Assuntos Regulamentares um processo robusto de revisão médica, jurídica e regulamentar (MLR). Esta sinergia é fundamental para garantir a conformidade total com a publicidade, a rotulagem promocional ou a divulgação de assuntos médicos não promocionais.
Evitar alegações enganosas, não comprometer a segurança dos doentes e garantir uma divulgação ética.
Minimizar os riscos associados ao incumprimento, às notificações de infração ou às sanções, bem como aos danos à reputação.
Garantir a exatidão das alegações relativas à segurança, eficácia ou desempenho do dispositivo e a sua fundamentação com evidências científicas.
Coerência e conformidade com a rotulagem aprovada do produto e com as instruções de utilização (IFU).
Cumprimento das diretrizes estabelecidas pelos organismos reguladores e dos códigos deontológicos do setor para diferentes países e regiões.
Na Freyr, os nossos especialistas em assuntos médicos e regulamentares, com uma formação clínica e biomédica sem paralelo, competência MLR e Assuntos Regulamentares promocionais em mais de 120 países, prestam apoio 24 horas por dia para garantir a conformidade total das suas promoções de marca, anúncios, campanhas de sensibilização sobre doenças ou campanhas sem referência a marcas.
Serviços
- Confirmar o cumprimento das diretrizes específicas de cada país estabelecidas por autoridades reguladoras, tais como a FDA, EMA, EU MDR, MHRA, a TGA, HSA, PMDA, ANVISA, a Health Canada e outras.
- Confirmar o cumprimento das diretrizes específicas de cada país relativas às leis anti-suborno e aos códigos de ética do setor, tais como FTC, PhRMA, EFPIA, ABPI, PAAB, TGA, Medicines New Zealand, ANVISA, ANAMED, IFPMA, AIFA, AEMPS, Mdeon e outros.
- Verificar a utilização adequada das alegações e referências. As alegações devem ser fundamentadas por referências relevantes e adequadas, bem como por evidências científicas, e a eficácia ou segurança não deve ser exagerada.
- Assegurar um equilíbrio justo na apresentação dos riscos e benefícios do produto, incluindo quaisquer efeitos secundários ou consequências potenciais da sua utilização.
- Avaliar a linguagem, as imagens e outros elementos utilizados na apresentação da informação, a fim de garantir clareza, precisão e a ausência de informações enganosas para o público-alvo.
- Verificar o alinhamento dos elementos de design e de fundo com o conteúdo, a fim de evitar discrepâncias (por exemplo, garantir que não sejam utilizadas imagens de populações pediátricas em contextos em que o produto não seja prescrito para essa população).
- Precisão das marcas comerciais e das marcas de serviço da empresa, bem como das certificações de conformidade de dispositivos, tais como a marca CE, UKCA mark, a certificação CCC e outras.
- Atuar como especialistas na matéria (SMEs) em questões regulatórias durante as reuniões da PRC.
- Orientar os pedidos de aprovação da HA, tais como o OPDP/APLP 2253 ou a análise da HA de materiais promocionais.
- Publicidade e rotulagem promocional: submissões às autoridades sanitárias, tais comoForm 2253 APLB Form 2253 FDA US ,FDA formatos manual e eCTD.
A nossa equipa é altamente inovadora e capaz de desenvolver conteúdos para qualquer plataforma ou canal; por isso, as nossas ofertas e competências não se limitam ao acima mencionado — podemos fazer muito mais!
- Analisar o conteúdo relacionado com o medicamento, incluindo indicações, posologia, instruções de utilização e mecanismo de ação, para garantir a adequação e a exatidão, em conformidade com a rotulagem aprovada do produto, as informações de prescrição (PI), SmPC, os folhetos informativos para o doente (PIL) e as instruções de utilização (IFU), e com base em evidências clínicas e científicas adequadas.
- Avaliar o alinhamento do material promocional com as diretrizes de tratamento atuais e os padrões de cuidados na área terapêutica específica
- Personalizar os pontos de controlo da revisão para se adequarem às áreas terapêuticas com diretrizes ou regulamentos para atividades promocionais, como oncologia ou doenças raras
- Garantir um "equilíbrio justo" entre a apresentação dos riscos e benefícios no material promocional, refletindo com precisão as desvantagens potenciais juntamente com as vantagens.
- Os ensaios clínicos e outros dados científicos precisos e credíveis comprovam adequadamente as alegações.
- Certifique-se de que as afirmações comparativas com outros produtos são apoiadas por dados válidos e fiáveis.
- Certifique-se de que a terminologia médica e os sinónimos são cuidadosamente selecionados para garantir uma comunicação clara.
- Certifique-se de que o público-alvo é o adequado (por exemplo, profissionais de saúde, doentes, cuidadores) e de que os materiais estão adaptados ao seu nível de compreensão e às suas necessidades.
- Colaborar com equipas multifuncionais no processo MLR (Global to Local) específico para cada país e na avaliação da situação atual do processo do Comité de Revisão Promocional (PRC), realizar análises de lacunas e identificar áreas para otimização e harmonização.
- Definição de procedimentos operacionais padrão (SOP), instruções de trabalho para MLR e indicadores-chave de desempenho (KPI) para avaliar a eficiência dos processos.
- Experiência na definição de fluxos de trabalho de processos MLR para sistemas de gestão de conteúdo de marketing (LCM), como Veeva PromoMats o MedComms.
- Facilitar a MLR e o processo de PRC para anúncios e materiais promocionais e não promocionais em sistemas LCM, como Veeva PromoMats, Veeva MedComms, Pepperflow, etc.
- Elaborar e distribuir as ordens de trabalhos das reuniões às partes interessadas, participar nas reuniões do PRC e redigir as atas e as decisões tomadas pelo PRC.
- Enviar material promocional e publicitário aos críticos de forma prioritária e atempada.
- Agendar e coordenar todas as reuniões de conceção, pré-apresentação e revisão durante a implementação com as partes interessadas.
- Acompanhar as aprovações das revisões do material e garantir que as alterações sejam incorporadas com precisão.
- Assegura que o material publicitário e promocional cumpre os critérios para ser submetido.
Revisão MLR de Materiais Promocionais
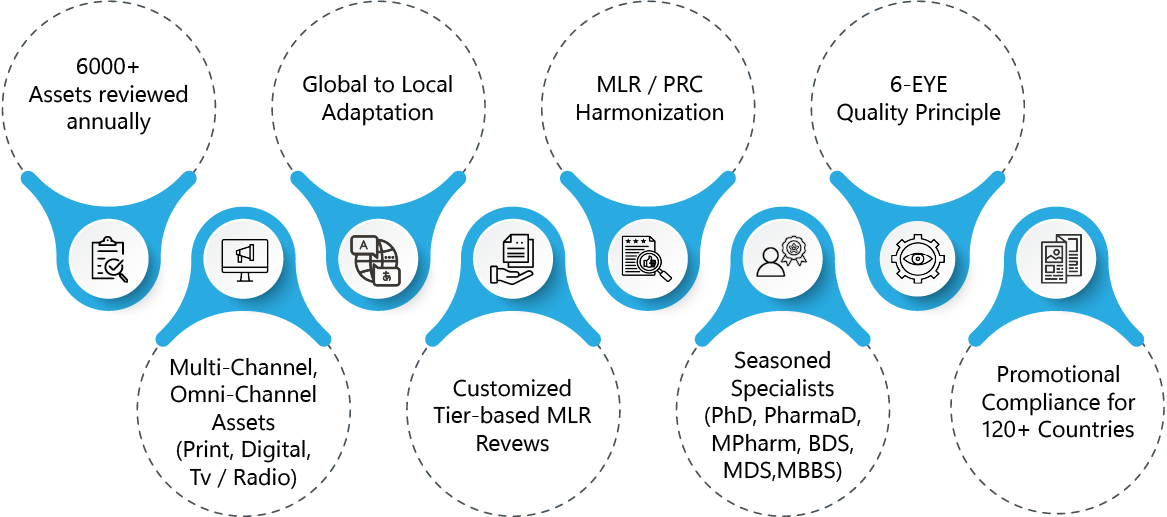
- Mais de 6000 ativos analisados anualmente para verificar MLR
- Experiência na adaptação de recursos promocionais do âmbito global ao local e na harmonização dos processos MLR
- Princípio dos 6 Olhos para um controlo reforçado da conformidade regulamentar, adaptado às complexidades da área terapêutica
- MLR possui experiência numa vasta gama de anúncios e materiais promocionais e não promocionais para diversos canais de comunicação – digital, impressão, televisão/rádio
- MLR por níveis personalizada com base na complexidade dos ativos
- Especialistas em conformidade promocional e MLR com experiência no setor e formação clínica/biomédica (PharmaD, PhD, Mpharm, BDS, MDS, MBBS)
- Consultoria estratégica e específica para cada região sobre a conformidade do material promocional em mais de 120 países.
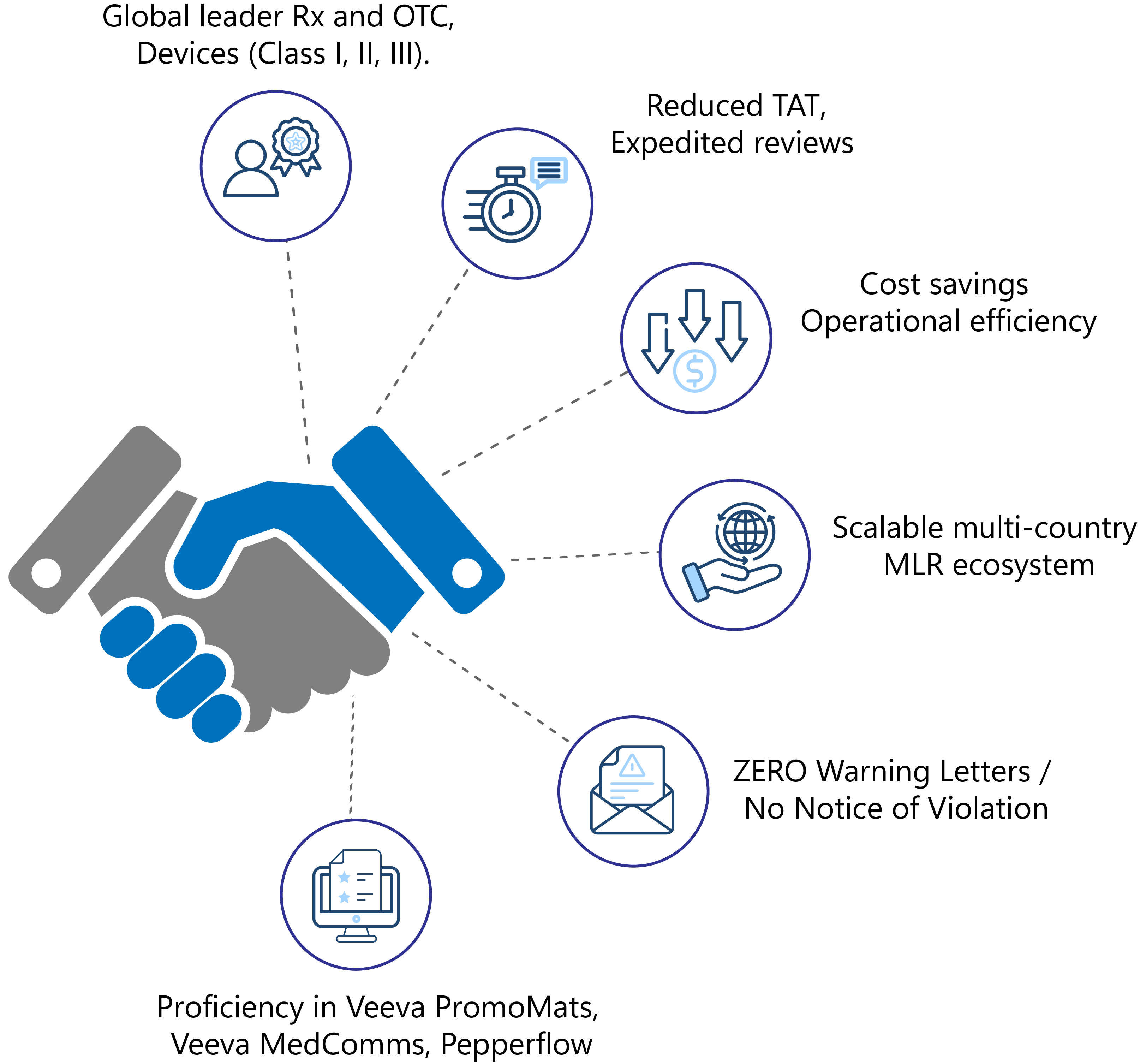
- Líder mundial nos setores farmacêutico, biofarmacêutico (medicamentos sujeitos a receita médica e OTC) e de dispositivos médicos (Classe I, II e III).
- Reduzir o tempo total do ciclo para revisão
- TAT reduzido com revisões aceleradas para cumprir prazos
- Poupanças de custos significativas e melhoria da eficiência operacional
- Ecossistema MLR escalável para vários países
- ZERO cartas de advertência/Nenhuma notificação de violação
- Domínio de sistemas de gestão de conteúdo de marketing ( MLR , como Veeva PromoMats, Veeva MedComms, Pepperflow, etc.