Visão Geral do Software como Dispositivo Médico (SaMD)
O Software como Dispositivo Médico (SaMD) é o tema mais recente e em ascensão no segmento da saúde. Espera-se que o mercado de SaMD cresça a uma Taxa de Crescimento Anual Composta (CAGR) de 10,78%, a nível global. Este crescimento é impulsionado por vários fatores, como a adoção da Internet das Coisas (IoT), as plataformas digitais de saúde e a adoção de software para monitorização contínua de parâmetros fisiológicos por prestadores de cuidados de saúde para assistência remota. No entanto, este cenário promissor também apresenta desafios únicos, sendo um deles determinar se se enquadra na categoria de dispositivo médico e se cumpre os requisitos regulamentares.
Diferentes Tipos de Produtos de Saúde Digital
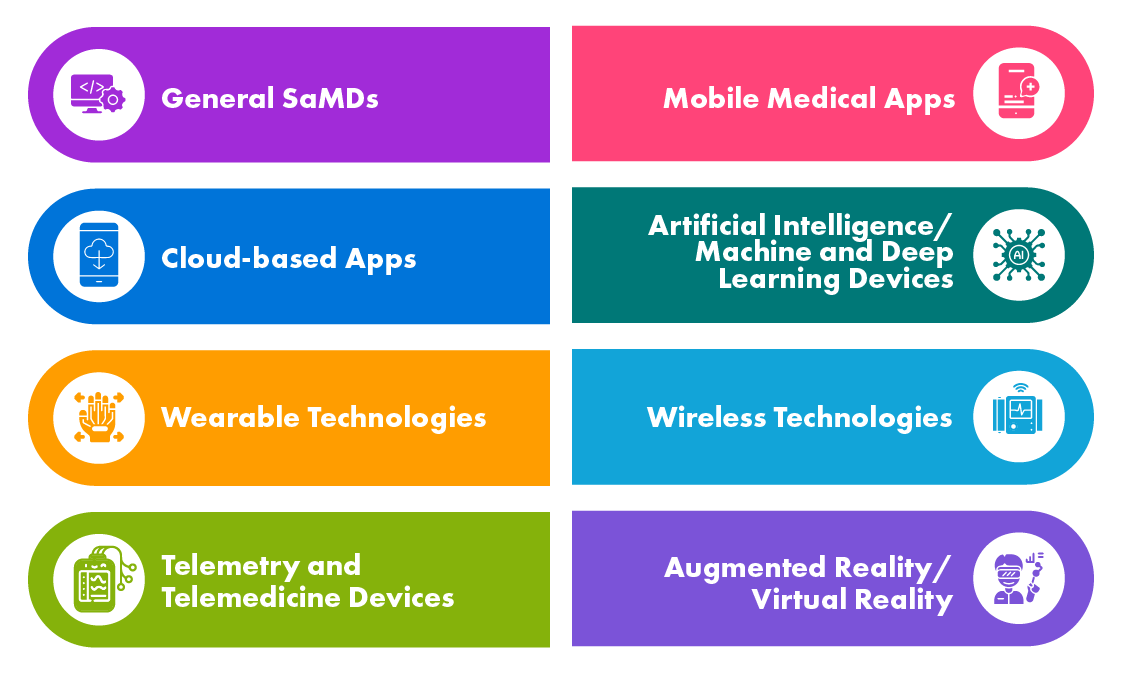
Cenário Regulamentar Global para o Registo de Software como Dispositivo Médico (SaMD)
Os SaMDs são utilizados em várias aplicações, como rastreio e diagnóstico, monitorização e alerta, gestão de doenças, etc. As Agências de Saúde dos países desenvolvidos, como a UE, os US, o Canadá e a Austrália, definiram regulamentos sobre SaMDs e algumas delas já desenvolveram documentos de orientação, enquanto outras estão em processo.
Alguns mercados regulamentados e não regulamentados consideram o software como dispositivos médicos, mas não possuem diretrizes diferenciadas e específicas para a classificação de Software como Dispositivo Médico (SaMD). Seguem as diretrizes harmonizadas internacionalmente aceites para a avaliação e aprovação do software.
Abaixo estão listadas algumas das diretrizes proeminentes disponíveis sobre Registo de Software como Dispositivo Médico (SaMD):
- Orientação IMDRF para classificação, Sistema de Gestão da Qualidade (SGQ), avaliação de cibersegurança e avaliação clínica.
- O EU MDR 2017/745 detalhou os requisitos regulamentares e a orientação para esta categoria de dispositivo.
- A orientação do MDCG sobre qualificação e classificação de SaMD, requisitos de Clinical evaluation reports (CER)/Relatórios de Avaliação de Desempenho (PER) para SaMD.
- A orientação da US FDA sobre cibersegurança, avaliação clínica e requisitos de registo para diferentes tipos de software, como sistemas de decisão, Sistema de Arquivamento e Comunicação de Imagens (PACS), aplicações móveis, etc.
- Documento de orientação da Health Canada sobre a definição e classificação de SaMD.
- Novos regulamentos da TGA para dispositivos médicos baseados em software.
O registo de SaMD noutros mercados globais deve ser tratado caso a caso e requer uma interação próxima com a respetiva Agência de Saúde para aprovação. O caminho geral seguido para o registo de SaMD inclui:
- Determinar se um determinado software se qualifica como um SaMD.
- Classificação dos dispositivos com base no risco envolvido.
- Identificar padrões aplicáveis e requisitos de dados pela Agência de Saúde em questão.
- Gerar dados conforme exigido pela respetiva Agência.
- Compilação do ficheiro técnico de acordo com o requisito do país.
- Resolução de submissões e questões até à aprovação.
- Gestão do ciclo de vida pós-aprovação.
As nossas competências
- Serviços de Inteligência Regulamentar (Relacionados com Suporte de Mercado + Rotulagem)
- Diligência Devida Regulamentar / Relatórios de Estratégia
- Qualificação e Classificação de SaMD
- Submissão de Classificação de Produto ao NB
- Análise de Lacunas
- Reuniões de Pré-Submissão com a FDA
- Identificação de Normas Aplicáveis
- Atividades de Gestão de Risco
- Apoio à Gestão de Risco
- Apoio à Rotulagem
- Criação/revisão/atualização de procedimentos/modelos específicos para SaMD
- UDI/GUDID
- Registo de produto (Registo de software)
- Registo de Estabelecimento
- Listagem de Dispositivos
- Resposta a consultas de Autoridades de Saúde — serviços de SaMD
Porquê a Freyr?
Perguntas Frequentes (FAQs)
A regulamentação de software médico é supervisionada por vários Organismos Regulamentares globais, incluindo a FDA nos Estados Unidos, a EMA na Europa e a PMDA no Japão. Estas Agências classificam o software médico com base no risco e estabelecem diretrizes para a segurança, qualidade e eficácia. É exigido o cumprimento das normas ISO, como a ISO 13485 e a 62304.
A determinação da classificação de risco de Software como Dispositivo Médico (SaMD) envolve a avaliação de fatores como o uso pretendido e o potencial de dano. Os SaMDs são classificados como dispositivos médicos tradicionais com base na importância da informação fornecida para a decisão de saúde e no estado da situação ou condição de saúde como não grave, grave e crítica. As diretrizes regulamentares e a consulta a especialistas são cruciais neste processo, garantindo a conformidade e a segurança do paciente.
SaMD refere-se a software que se destina a ser utilizado para um ou mais fins médicos, sem fazer parte de um dispositivo médico físico. Opera em plataformas de computação de uso geral, como smartphones, tablets ou computadores pessoais. Por outro lado, SiMD é um software que é um componente integral de um dispositivo médico físico, contribuindo para a sua funcionalidade e desempenho. O SiMD não pode ser utilizado de forma independente e depende do dispositivo médico associado para cumprir o seu propósito pretendido.
Um software que está incorporado como parte de um dispositivo médico de hardware e é necessário para cumprir o propósito médico pretendido NÃO é considerado um SaMD.
O cronograma para alcançar a conformidade com SaMD é influenciado pela classe de risco e pelo requisito regulamentar. Mas, com a assistência regulamentar certa, pode garantir um processo de conformidade mais suave com riscos mínimos.
Registo de Dispositivos Médicos
- Estratégia de regulamentação abrangente para SaMDs.
- Apoio de inteligência regulamentar e de mercado.
- Serviços de classificação e registo de produtos para SaMDs.
- Apoio regulamentar para documentos de desenvolvimento de produtos SaMD.
- Serviços de consultoria sobre estudos de avaliação clínica de SaMD.
- Gestão de alterações pós-aprovação.
- Serviço de representação local.

- Estratégia de regulamentação abrangente para SaMDs.
- Apoio de inteligência regulamentar e de mercado.
- Serviços de classificação e registo de produtos para SaMDs.
- Apoio regulamentar para documentos de desenvolvimento de produtos SaMD.
- Serviços de consultoria sobre estudos de avaliação clínica de SaMD.
- Gestão de alterações pós-aprovação.
- Serviço de representação local.









