Visão Geral do eSTAR da FDA
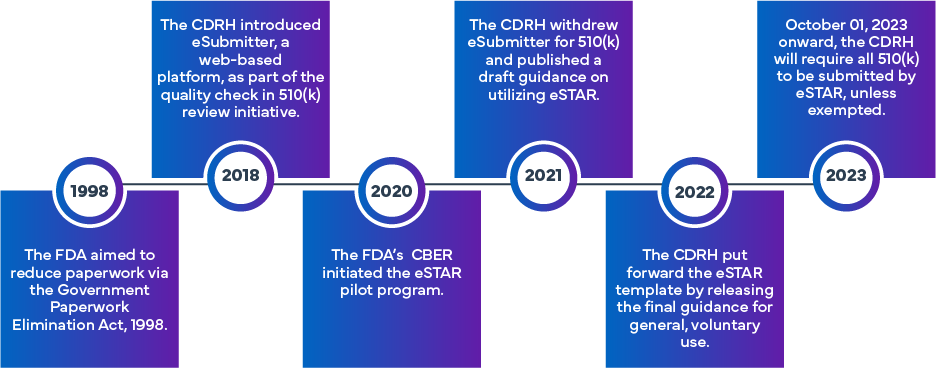
A iniciativa FDA foi concebida para aumentar a eficiência e a uniformidade na preparação e avaliação dos pedidos FDA (k), De Novo e PMA FDA . Com base na abordagem inicial do eSubmitter, que envolvia a apresentação eletrónica de pedidos relativos a dispositivos médicos e de diagnóstico in vitro (IVD), o programa eSTAR foi criado, tirando partido da experiência anterior FDA. A FDA num programa diferente denominado Programa-Piloto de Modelos e Recursos de Submissão Eletrónica (eSTAR). As submissões 510(k) são obrigatoriamente feitas através do eSTAR desde 1 de outubro de 2023; as submissões De Novo (salvo isenção) são obrigatoriamente feitas através do eSTAR desde 1 de outubro de 2025. Os modelos estão disponíveis para online , embora exijam a utilização de credenciais FDA para o processo de submissão propriamente dito.
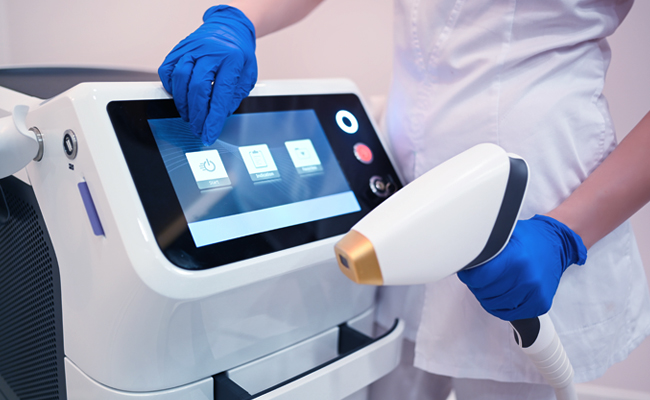
O que é o eSTAR da FDA?
O eSTAR é um modelo PDF interativo concebido para facilitar a preparação de um pedido abrangente de autorização pré-comercialização de dispositivos médicos junto da FDA Além disso, os requerentes podem utilizar o eSTAR para enviar respostas aos pedidos de informações adicionais FDA. O seu objetivo é melhorar a qualidade dos pedidos relativos a diversos dispositivos médicos, garantindo que os requerentes forneçam dados completos e de alta qualidade para a análise pré-comercialização FDA.
Ao adotarem o formato eSTAR, os requerentes podem ter a certeza de que os seus pedidos estão completos, o que, por sua vez, permitirá à FDA análises pré-comercialização de forma mais eficiente e garantir o acesso atempado a dispositivos médicos seguros e eficazes. O modelo eSTAR está disponível gratuitamente e pode ser utilizado por todos os requerentes de dispositivos médicos para submissões 510(k) e De Novo, bem como voluntariamente para submissões Q e submissões complementares de Notificação de 30 Dias de PMA à FDA. Existem dois tipos de modelos eSTAR – um para dispositivos médicos e outro para IVDs. O PreSTAR beta evoluiu; utilize os modelos de submissão Q mais recentes através do Portal de Colaboração com o Cliente (CCP) do CDRH. O modelo eSTAR 6.0 para De Novo/510(k) não-IVD foi lançado em outubro de 2025.
Características e Limitações das Submissões eSTAR
Embora o programa eSTAR ofereça um formulário PDF interativo concebido para ajudar os requerentes na elaboração de submissões completas de dispositivos médicos e IVD, este apresenta vantagens e desvantagens. Os requerentes devem compreender estes benefícios e limitações, com base nos quais podem fazer escolhas bem informadas sobre a integração do eSTAR no seu processo de submissão. Na tabela abaixo, exploraremos os atributos e restrições do programa eSTAR.

Considerações para uma Utilização Eficaz do eSTAR
Uma característica vantajosa do modelo eSTAR, que contribui para a otimização do processo de submissão, é a sua incorporação automatizada de regulamentos pertinentes e normas reconhecidas para citação. Isto não só acelera o processo de submissão ao reduzir a entrada manual de dados, como também atenua a possibilidade de erros humanos que possam ocorrer durante a introdução de regulamentos e normas. Através de uma construção guiada para cada secção de submissão, a utilização do eSTAR no processo de submissão pode ser facilmente simplificada.
- A FDA sugere o Adobe Acrobat Pro ou o Foxit PDF Editor para editar modelos eSTAR.
- O eSTAR inclui certos formulários integrados, eliminando assim a necessidade de preenchimento separado. Estes abrangem o Formulário 3514 (a folha de rosto da submissão) e o Formulário 3881 (indicações de utilização). Além disso, a declaração verdadeira e precisa, que anteriormente era exigida em papel timbrado da empresa, está agora integrada no eSTAR.
- O eSTAR suporta vários formatos de anexo além de apenas PDFs, como folhas de cálculo Excel e ficheiros de vídeo (mp4).
- Não são permitidos ficheiros em formatos com macros e executáveis.
- O tamanho total do ficheiro PDF eSTAR, juntamente com os seus anexos, não deve exceder 1GB, uma vez que ficheiros maiores que 4GB não serão aceites.
- Se os seus ficheiros eletrónicos excederem os limites técnicos, pode enviar a submissão digital para o Centro de Controlo de Documentos (DCC) do CDRH por correio.
Boas Práticas para a Preparação de Submissões eSTAR
Seguir algumas das melhores práticas para a preparação de submissões eSTAR pode ajudar os requerentes a otimizar o processo de submissão e a melhorar as suas hipóteses de um resultado bem-sucedido. Apresentamos algumas das melhores práticas:
- Siga as FDA :A FDA orientações para ajudar os requerentes a utilizarem com sucesso o modelo eSTAR. Seguir estas orientações garante que os pedidos apresentados estejam em conformidade com os requisitos e as expectativas FDA.
- Garantir a exaustividade:O modelo eSTAR orienta os candidatos através das informações essenciais para a apresentação da candidatura. Os candidatos devem fornecer todos os dados exigidos para minimizar as possibilidades de lacunas ou pedidos de informações adicionais.
- Manter a consistência:O modelo eSTAR promove a uniformidade no conteúdo e na estrutura dos pedidos 510(k). A estrutura orientada para cada secção do pedido ajuda a extrair informações sobre um dispositivo médico.
- Dê prioridade à clareza:forneça informações claras e concisas nos pedidos apresentados no eSTAR para facilitar um processo de análise ágil. Esse nível de detalhe e precisão minimiza atrasos e erros, garantindo também o acesso atempado aos pedidos de autorização pré-comercialização de dispositivos médicos.
- Precisão garantida:a verificação automática das informações em cada secção dos envios do eSTAR ajuda a reduzir os atrasos na análise e a minimizar possíveis falhas.
Significado da Codificação por Cores na Submissão FDA eSTAR
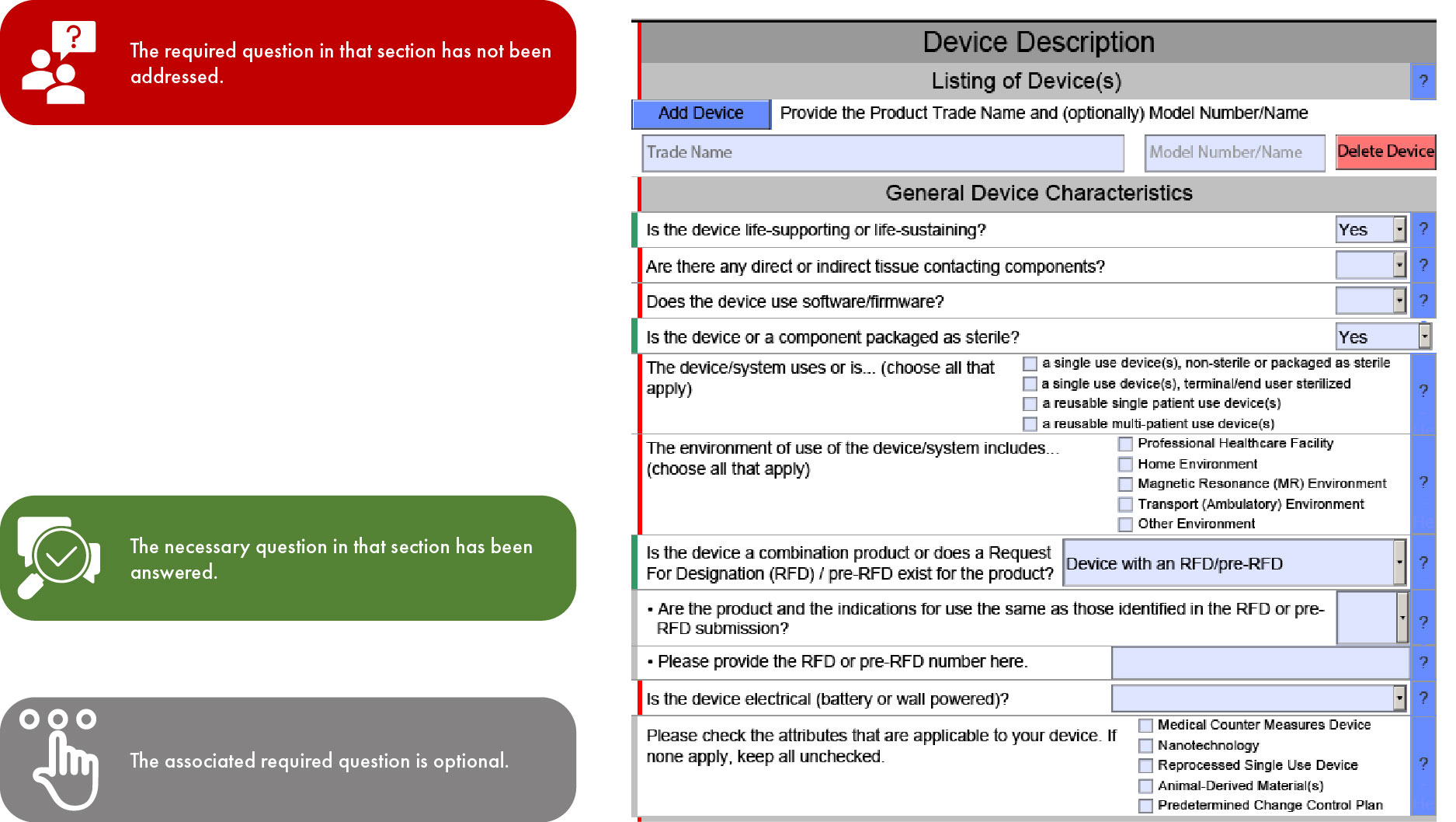
O eSTAR será obrigatório para os pedidos 510(k) a partir de 1 de outubro de 2023 e para os pedidos De Novo a partir de 1 de outubro de 2025; a progressão do modelo pelas secções é determinada pelo tipo de pedido. Este tipo de simplificação facilita uma análise mais rápida por parte daFDA US , minimizando assim as inconsistências e omissões no seu pedido. No entanto, é importante notar que a FDA atrasar a sua análise se faltarem traduções para inglês da documentação fornecida.

Alinhe os Seus Anexos
Examine o modelo eSTAR antecipadamente para compreender como os anexos são divididos e garantir que os seus documentos se alinham com as secções de anexos. Este passo é crucial, especialmente para empresas com submissões 510(k) anteriores, uma vez que a sua abordagem atual à organização de documentos poderá exigir ajustes. Poderá também implicar a extração de conteúdo dos anexos.
- O eSTAR exige anexos concisos, que diferem das submissões tradicionais.
- Espere vários anexos, potencialmente dezenas deles.
- Os anexos permitem a inclusão de dados como folhas de cálculo Excel, ficheiros de vídeo MP4, documentos Word, ficheiros JPEG, etc.
- O eSTAR requer números de página para as informações dos anexos, mas não sugere a utilização de uma lista de verificação de recusa de aceitação para as orientações da FDA.
Modelos: estão disponíveis os modelos da versão 6.0 mais recente ; a versão 5 é aceitável para submissões em curso: fda.
O Futuro do eSTAR
Prevê-se que o eSTAR seja atualizado após a finalização de documentos de orientação aplicáveis abrangentes. Com estas atualizações, o fabricante pode consultar as versões mais recentes emitidas pela US FDA.
A Health Canada (HC) introduziu uma iniciativa-piloto para utilizar o eSTAR para dispositivos de Classe III e IV. Existe a conjectura de que outras nações poderão seguir o exemplo do Canadá ao tornar a adoção do eSTAR discricionária, particularmente dentro do consórcio IMDRF. No entanto, deve-se notar que não houve declarações explícitas nesse sentido.
Porquê escolher a Freyr?
A Freyr possui uma vasta experiência adquirida através do seu envolvimento em inúmeros projetos focados em submissões à FDA no passado. Ao apresentar duas vias para auxiliar proativamente a indústria na aceleração das submissões 510(k) e De Novo, a Freyr oferece uma gama de serviços ao cliente, que abrangem uma lista abrangente de documentos essenciais de submissão e informações necessárias, a realização de análises de lacunas meticulosas na documentação, a compilação de submissões via eSTAR, e a finalização do pacote de submissão pré-mercado à FDA. Além disso, a Freyr estende o seu apoio a atividades pós-submissão, como o fornecimento de informações adicionais e a revisão das respostas da indústria a quaisquer pedidos de informações suplementares feitos pela FDA.
Como pode a Freyr ajudar?
A Freyr oferece apoio que pode ser útil para preparar as submissões 510(k) e De Novo. Os serviços incluem:
- Apoio ao Percurso Regulatório: Isto envolve a identificação do código do produto, nome e número da regulamentação, potenciais dispositivos precedentes/de referência, testes de desempenho, bem como as normas aplicáveis e documentos de orientação pertinentes ao dispositivo específico em questão.
- Apoio à Q-submission (Pré-submissões): Isto envolve ajudá-lo a esclarecer questões relacionadas com os pré-requisitos de uma submissão pré-comercialização, organizar a submissão, preparar-se para uma reunião com a FDA, interagir com a FDA durante a reunião de forma interativa e redigir as atas da reunião.
A Experiência no Programa FDA eSTAR
- Estratégia regulamentar abrangente da FDA.
- Identificação do dispositivo precedente.
- Estabelecer equivalência substancial com dispositivo predicado.
- Análise de Lacunas para conformidade com a FDA.
- Compilação de vinte e uma (21) secções do ficheiro técnico 510(k).
- Publicação e criação do eCopy.
- Validação e submissão do eCopy.
- Serviços de ligação para aprovação de dispositivos.
- A resolução da resposta RTA e das deficiências.
- Serviços de consultoria para a resolução de deficiências.
- Registo de Dispositivos e manutenção da base de dados FURLS.