Garantir a conformidade total com os regulamentos e o registo de dispositivos médicos do Reino Unido
Os fabricantes estrangeiros devem cumprir o Regulamento de Dispositivos Médicos do Reino Unido de 2002 (na sua versão alterada). Todos os dispositivos médicos e dispositivos de diagnóstico in vitro (IVD) devem ser registados junto da MHRA da sua comercialização no Reino Unido. Os fabricantes não britânicos são obrigados a nomear um Responsável no Reino Unido (UKRP) para os representar. A MHRA requisitos rigorosos em matéria de documentação, rotulagem e notificação de vigilância, a fim de garantir a segurança dos doentes e a rastreabilidade dos produtos.
Orientar-se entre os novos requisitos propostos no resultado da consulta para o Reino Unido pode revelar-se complexo no que diz respeito à marcação UKCA, aos requisitos em matéria de dados e às expectativas pós-comercialização. Muitas empresas enfrentam desafios relacionados com dossiers técnicos incompletos, classificações divergentes dos dispositivos e um conhecimento limitado do Sistema Online de Dispositivos (DORS). As atualizações regulamentares e a evolução MHRA complicam ainda mais o planeamento e a afetação de recursos.
A Freyr simplifica todas as etapas da entrada no mercado britânico. Tratamos dos pedidos de DORS, atuamos como seu UKRP, garantimos que a documentação esteja pronta e colmatamos as lacunas de conformidade durante a transição da marcação CE para a UKCA. Os nossos especialistas em regulamentação orientam-no nas mudanças MHRA , ajudando-o a obter um acesso ao mercado em conformidade, atempado e económico.
Processo passo a passo para o registo de dispositivos médicos no Reino Unido
O registo de um dispositivo médico no Reino Unido envolve várias etapas definidas. Eis como a Freyr gere todo o processo por si:
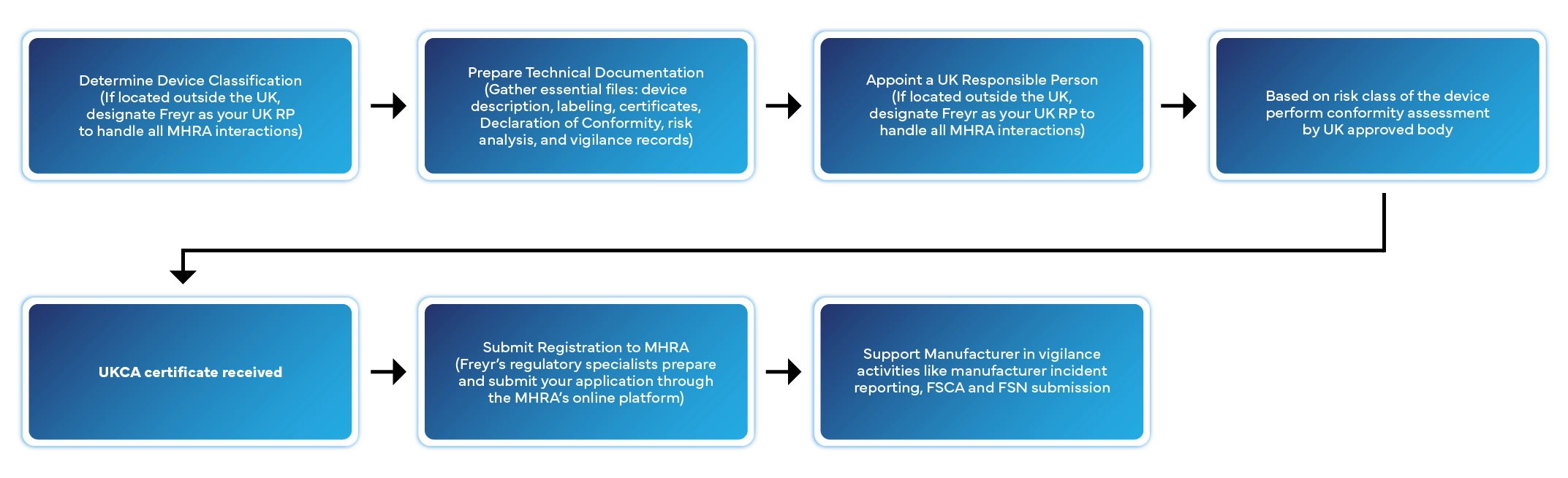
Prazo de processamento habitual: 2 a 6 semanas, dependendo da classe do dispositivo e da completude da documentação.
Principais ofertas da Freyr Medical Device UK
Registo de dispositivos A Freyr gere todo MHRA através da plataforma DORS, garantindo submissões em conformidade, dados precisos e aprovações atempadas para todas as categorias de dispositivos.
Responsável no Reino Unido Na qualidade de seu UKRP designado, a Freyr representa-o perante a MHRA, trata de toda a comunicação e assegura o cumprimento contínuo da regulamentação e a monitorização da vigilância.
TF / Compilação de Dossiers A Freyr compila fichas técnicas e dossiês que cumprem os requisitos regulamentares do Reino Unido para a marcação UKCA, garantindo a preparação para auditorias, inspeções e apresentações.
Apoio ao SGQ Prestamos assistência na implementação e manutenção de Sistemas de Gestão da Qualidade ISO 13485, adaptados às MHRA do MDR do Reino Unido e MHRA .
Apoio à Redação de Documentação Regulamentar A Freyr oferece serviços especializados de elaboração de CERs, planos de PMS, PSURs e documentação de gestão de riscos, garantindo clareza técnica e rigor regulamentar.
Rotulagem e Conformidade A nossa equipa garante que a sua rotulagem, instruções de utilização e embalagem cumprem os requisitos de rotulagem e linguísticos da certificação UKCA, mantendo a consistência e a conformidade.
Vigilância pós-comercialização A Freyr apoia as atividades de vigilância pós-comercialização, incluindo a notificação de eventos adversos, o envio de relatórios de vigilância e MHRA , com vista a garantir a manutenção do acesso ao mercado.
Oferta de serviços da Freyr UK Responsible Person (UKRP)
A Freyr atua como seu UKRP Autorizado UKRP, garantindo o cumprimento integral do Regulamento de Dispositivos Médicos do Reino Unido de 2002 MHRA. Representamos a sua empresa a nível local no Reino Unido e tratamos de toda a comunicação com a MHRA.
- Registo de dispositivos junto MHRA
A Freyr atua como a sua Pessoa Responsável no Reino Unido (UKRP) designada para gerir todo o processo MHRA através da plataforma DORS, garantindo que todos os dispositivos sejam corretamente registados, verificados e aptos para venda no Reino Unido. - Documentação e Garantia de Conformidade
Os nossos especialistas em regulamentação asseguram que a sua Declaração de Conformidade, documentação técnica e certificações de produtos estejam disponíveis e mantêm uma cópia para disponibilizar a documentação à MHRA, mediante solicitação. - Resposta a MHRA
A Freyr trata diretamente de todas as comunicações e esclarecimentos com a MHRA seu nome, garantindo respostas oportunas e precisas a consultas regulamentares ou análises pós-comercialização. - Vigilância e Comunicação de Incidentes
Na qualidade de seu UKRP, a Freyr atua como principal ponto de contacto para questões relacionadas com a segurança. Coordenamos a comunicação entre fabricantes, profissionais de saúde, doentes e a MHRA eventos adversos, garantindo a notificação adequada e a implementação de medidas corretivas. - Preparação para inspeções e auditorias
A Freyr mantém toda a documentação e correspondência necessárias para MHRA e auditorias MHRA . A nossa equipa garante que os dossiers técnicos, a rotulagem e os registos pós-comercialização estejam prontamente disponíveis.
Agende uma reunião com os nossos especialistas hoje
Porquê colaborar com a Freyr?
- Conhecimento End-to-end , que vai desde o registo pré-comercialização até à vigilância pós-comercialização, gerindo todas as fases do processo de conformidade.
- Um histórico comprovado com mais de 1500 registos de dispositivos concluídos com sucesso em diversas categorias.
- Presença local no Reino Unido, com especialistas em regulamentação no terreno em Reading, apoiados por equipas de prestação de serviços a nível global.
- Um plano de transição personalizado que oferece apoio estratégico para a transição da certificação CE para a UKCA de forma harmoniosa e económica.
- Comunicação transparente através do contacto direto com MHRA atualizações proativas sobre a conformidade aos clientes.
- Com a confiança de marcas globais, a Freyr presta serviços a mais de 470 fabricantes em todo o mundo como seu parceiro em matéria de regulamentação.
Perguntas Frequentes (FAQs)
01. Qual é o processo de registo de dispositivos médicos no Reino Unido?
O processo de registo de dispositivos médicos no Reino Unido implica notificar a MHRA Agência Reguladora de Medicamentos e Produtos de Saúde) sobre o seu dispositivo antes de este ser comercializado na Grã-Bretanha. Os fabricantes devem fornecer os dados da empresa, a classificação do dispositivo e a documentação técnica. Os fabricantes não sediados no Reino Unido devem também nomear um Responsável no Reino Unido (UK RP) para tratar do registo e das comunicações relativas à conformidade contínua.
02. Quem deve nomear um Responsável no Reino Unido (UK RP)?
Qualquer fabricante com sede fora do Reino Unido deve nomear um Responsável no Reino Unido antes de colocar os dispositivos no mercado britânico. O Responsável no Reino Unido atua como ponto de contacto regulamentar do fabricante, garantindo que toda a documentação técnica, declarações e MHRA sejam devidamente mantidas. Os fabricantes com sede no Reino Unido podem interagir diretamente com a MHRA um Responsável no Reino Unido.
03. Que documentação é necessária para MHRA ?
A MHRA documentação essencial, incluindo a Declaração de Conformidade, a descrição e classificação do dispositivo, os dados do fabricante e as informações de rotulagem. No caso de dispositivos de maior risco, os dossiers técnicos e as evidências clínicas também podem ser analisados. Dispor de documentação completa e pronta para auditoria garante aprovações mais rápidas e inspeções pós-comercialização mais tranquilas por parte da MHRA dos representantes autorizados.
04. Quanto tempo demora o processo MHRA ?
Normalmente, MHRA demora entre 2 a 6 semanas, dependendo da classe do dispositivo, da exaustividade da documentação e da existência ou não de um Responsável no Reino Unido. Os dispositivos simples da Classe I podem ser processados mais rapidamente, enquanto os produtos complexos ou de maior risco podem demorar mais tempo devido à validação adicional dos dados e às revisões da documentação técnica.
05. Qual é a diferença entre a marcação CE e a marcação UKCA?
A marcação CE atesta a conformidade com os regulamentos da União Europeia, enquanto a marcação UKCA (UK Conformity Assessed) se aplica aos dispositivos comercializados na Grã-Bretanha. Desde o Brexit, a marcação UKCA substituiu a CE no mercado britânico, embora a marcação CE continue a ser aceite temporariamente. A Irlanda do Norte continua a reconhecer as marcações CE e CE UKNI ao abrigo das regras de alinhamento da UE.
06. Quais são as responsabilidades pós-comercialização após o registo?
Após o registo, os fabricantes e os responsáveis no Reino Unido devem realizar a vigilância pós-comercialização, comunicar incidentes adversos, informar MHRA alterações no produto ou na rotulagem e renovar os registos, conforme necessário. Devem também conservar a documentação técnica durante, pelo menos, 10 anos. Estas atividades garantem a conformidade contínua e salvaguardam a saúde dos doentes ao longo de todo o ciclo de vida do dispositivo.
07. Com que frequência devem ser atualizadas as informações MHRA ?
As informações de registo devem ser atualizadas imediatamente sempre que houver uma alteração na classificação do dispositivo, na rotulagem, no local de fabrico ou na entidade responsável. A MHRA a Pessoa Responsável no Reino Unido ou o fabricante procedam a atualizações imediatas, a fim de manter registos de mercado precisos. As auditorias internas regulares ajudam a garantir que os seus dados se mantêm atualizados e em conformidade com a evolução da regulamentação.
08. Quais são as sanções aplicáveis em caso de incumprimento dos MHRA ?
O incumprimento dos requisitos de registo de dispositivos médicos ou dos requisitos pós-comercialização no Reino Unido pode resultar em advertências regulamentares, retirada do produto do mercado, multas ou ações judiciais. A MHRA tem competência para suspender ou revogar a autorização de comercialização. Uma abordagem proativa em matéria de conformidade e a nomeação de um Responsável pelo Produto qualificado no Reino Unido ajudam os fabricantes a evitar sanções e a manter a continuidade da comercialização.
09. De que forma a Freyr simplifica o registo de dispositivos médicos no Reino Unido?
A Freyr oferece end-to-end , desde a função de Responsável no Reino Unido (UKRP) até MHRA , documentação técnica e conformidade contínua. Os nossos consultores experientes simplificam o processo, reduzem os prazos de aprovação e ajudam a garantir o acesso contínuo ao mercado.













