Visão Geral do Relatório de Validade Científica (SVR)
O Relatório de Validade Científica (SVR) possui uma importância primordial no âmbito do Relatório de Avaliação de Desempenho (PER) para Dispositivos Médicos de Diagnóstico In Vitro (IVDs), conforme o Regulamento (UE) 2017/746 relativo aos Dispositivos Médicos de Diagnóstico In Vitro (EU IVDR). O SVR desempenha um papel crucial na validação científica do desempenho analítico e clínico do dispositivo, garantindo a segurança e eficácia dos dispositivos médicos disponíveis no mercado. No processo de avaliação da conformidade prescrito pelo EU IVDR, os fabricantes são obrigados a apresentar um PER, que deve incluir um SVR, a um organismo notificado para demonstrar a segurança e o desempenho do dispositivo antes da sua introdução no mercado da UE.
Relatórios de Validade Científica para Submissão ao EU IVDR
- Análise e Conclusões
O que constitui o conteúdo do Relatório de Validade Científica (SVR)?
A validade científica de um analito significa a associação de um analito a uma condição clínica ou a um estado fisiológico. A validade científica de um IVD baseia-se principalmente numa ou numa combinação das seguintes fontes:
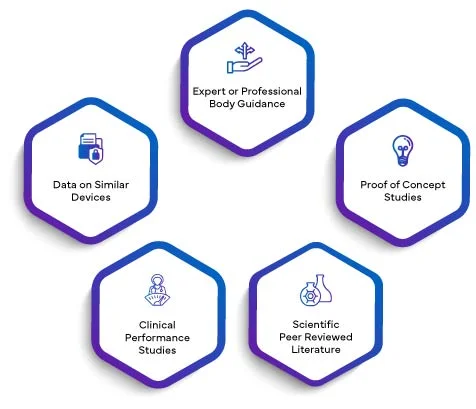
Os dados de todos os pontos acima, conforme aplicável, serão redigidos num relatório de validade científica. Ao integrar o SVR no PER, os fabricantes elevam a sua avaliação de desempenho a um patamar superior de credibilidade. A validade científica estabelecida através do SVR confere ao PER uma base robusta, melhorando a sua qualidade e significado gerais. Isto, por sua vez, inspira confiança nos organismos reguladores, profissionais de saúde e utilizadores finais, garantindo que o desempenho do IVD é meticulosamente avaliado e validado de acordo com os rigorosos requisitos do Regulamento (UE) 2017/746 relativo aos dispositivos médicos para diagnóstico in vitro.
A Freyr oferece assistência abrangente na preparação de um Relatório de Validade Científica (SVR) robusto para IVDs, capacitando-o a navegar com confiança no panorama regulamentar e a introduzir sem problemas dispositivos IVD seguros e eficazes no mercado.
Relatório de Validade Científica
- Plano de transição para conformidade com o IVDR.
- Relatório de Validade Científica (SVR) baseado em literatura e/ou dados internos.
- Relatórios de Desempenho Clínico (CPR) com base na literatura e/ou dados internos.
- Relatórios de Desempenho Analítico (APR)
- Evidência Clínica ou Relatórios de Avaliação de Desempenho conforme o IVDR.
- Plano de Avaliação de Desempenho.
- Protocolos e relatórios de Acompanhamento do Desempenho Pós-Comercialização (PMPF).
- Protocolos e relatórios de Vigilância Pós-Comercialização (PMSR).
- Redação/Revisão de outros documentos, como folheto informativo/IFU, Instruções de Referência Rápida (QRI), manual de operação/utilizador, etc.

- Conformidade assegurada com os regulamentos aplicáveis mais recentes.
- Equipa de especialistas qualificados
- Soluções Personalizadas às suas necessidades
- Gestão de Recursos Regulatórios/Serviços de Aumento de Pessoal
- Contributos multifuncionais de especialistas em Dispositivos Médicos para cumprir os requisitos.

Perguntas Frequentes
01. O que é um Relatório de Validade Científica (RVC) ao abrigo do IVDR da UE?
O Relatório de Validade Científica (RVC) documenta as provas que ligam um analito a uma condição clínica ou estado fisiológico e é uma parte fundamental do Relatório de Avaliação de Desempenho (RAD) exigido pelo Regulamento (UE) 2017/746 relativo aos Dispositivos Médicos para Diagnóstico in Vitro (IVDR) para dispositivos IVD. Demonstra que a justificação científica do dispositivo é sustentada por literatura ou dados de estudo, garantindo a segurança e a eficácia do dispositivo.
02. Porque é que o RVC é crítico na Avaliação de Desempenho para IVDs?
O RVC é crítico na Avaliação de Desempenho porque estabelece a validade científica do IVD, demonstrando a associação entre o analito e a condição clínica ou estado fisiológico. Fornece a base científica para a finalidade prevista do dispositivo e sustenta as alegações de desempenho clínico. Um RVC robusto fortalece o Relatório de Avaliação de Desempenho (RAD) global, permitindo que os Organismos Notificados avaliem se a utilização do dispositivo é clinicamente justificada, segura e está em conformidade com o Regulamento relativo aos Dispositivos Médicos para Diagnóstico in Vitro.
03. Que tipos de provas apoiam a validade científica num RVC?
A validade científica é tipicamente estabelecida através de múltiplas fontes de provas, tais como literatura revista por pares, estudos clínicos, dados de comparação de dispositivos e referências de ponta estabelecidas que ligam de forma robusta o analito à condição clínica.
04. Como é que o RVC difere dos Relatórios de Desempenho Analítico e Clínico?
O RVC foca-se em estabelecer a justificação científica para a associação de um analito a uma condição clínica, enquanto os Relatórios de Desempenho Analítico avaliam a precisão da medição e os Relatórios de Desempenho Clínico avaliam os resultados de desempenho no mundo real. Juntos, estes formam o RAD completo.
05. Quando devem os fabricantes começar a planear o RVC?
Os fabricantes devem planear o RVC numa fase inicial do desenvolvimento, idealmente em conjunto com o planeamento da avaliação de desempenho, para alinhar o contexto clínico, a estratégia de revisão da literatura e as expectativas regulamentares, minimizando o retrabalho e garantindo um suporte de dados robusto.
06. Quais são os desafios comuns na preparação de um Relatório de Validade Científica?
Os principais desafios incluem a definição do contexto clínico pretendido, a seleção de literatura relevante, a garantia da qualidade das provas e a síntese de conclusões que justifiquem claramente a validade científica para o escrutínio regulamentar. São frequentemente necessárias estratégias especializadas e técnicas de revisão sistemática.
07. Como é que o RVC apoia as submissões regulamentares aos Organismos Notificados?
Um RVC bem elaborado eleva a qualidade do Relatório de Avaliação de Desempenho, articulando claramente as provas e o raciocínio, facilitando assim uma avaliação da conformidade mais fluida e aumentando a confiança dos revisores regulamentares na base científica do IVD.
08. Porque é que a Freyr é considerada um parceiro líder para serviços de Relatório de Validade Científica?
A Freyr traz uma profunda experiência regulamentar e uma abordagem estruturada à preparação do RVC ao abrigo do IVDR da UE, permitindo que os fabricantes abordem com confiança os requisitos complexos de provas, ao mesmo tempo que reduzem o risco de atrasos na submissão. A entrega comprovada em diversos portefólios de IVD sublinha o papel da Freyr como um parceiro de confiança na excelência regulamentar.








