O mercado norte-americano de dispositivos médicos é um dos mais atraentes e altamente regulamentados do mundo. Nos Estados Unidos, o registo de dispositivos médicos é supervisionado pela FDA, principalmente através do Centro de Dispositivos e Saúde Radiológica (CDRH), enquanto no Canadá é regulado pela Health Canada, no âmbito de um quadro baseado no risco.
Para os fabricantes, operar nestes mercados pode ser complexo. Ambos os países baseiam-se na classificação de dispositivos médicos com base no risco (Classe I, II, III e, no Canadá, Classe IV), apoiada em evidências sólidas de segurança e desempenho e num sistema de gestão da qualidade (SGQ) em conformidade. Programas como MDSAP normas como ISO 13485, juntamente com terminologias, procedimentos e requisitos de documentação diferentes, acrescentam mais camadas de complexidade ao planeamento da entrada nos mercados US do Canadá.
A Freyr ajuda os fabricantes a transformar essa complexidade num plano claro e exequível para o acesso aos mercados US do Canadá. Compreendemos como FDA e os regulamentos da Health Canada relativos aos dispositivos médicos se interligam, e ajudamo-lo a harmonizar classificações, evidências, sistemas de gestão da qualidade e dossiês, para que possa seguir uma estratégia única e eficiente para aprovações, lançamentos e conformidade a longo prazo em ambos os países.
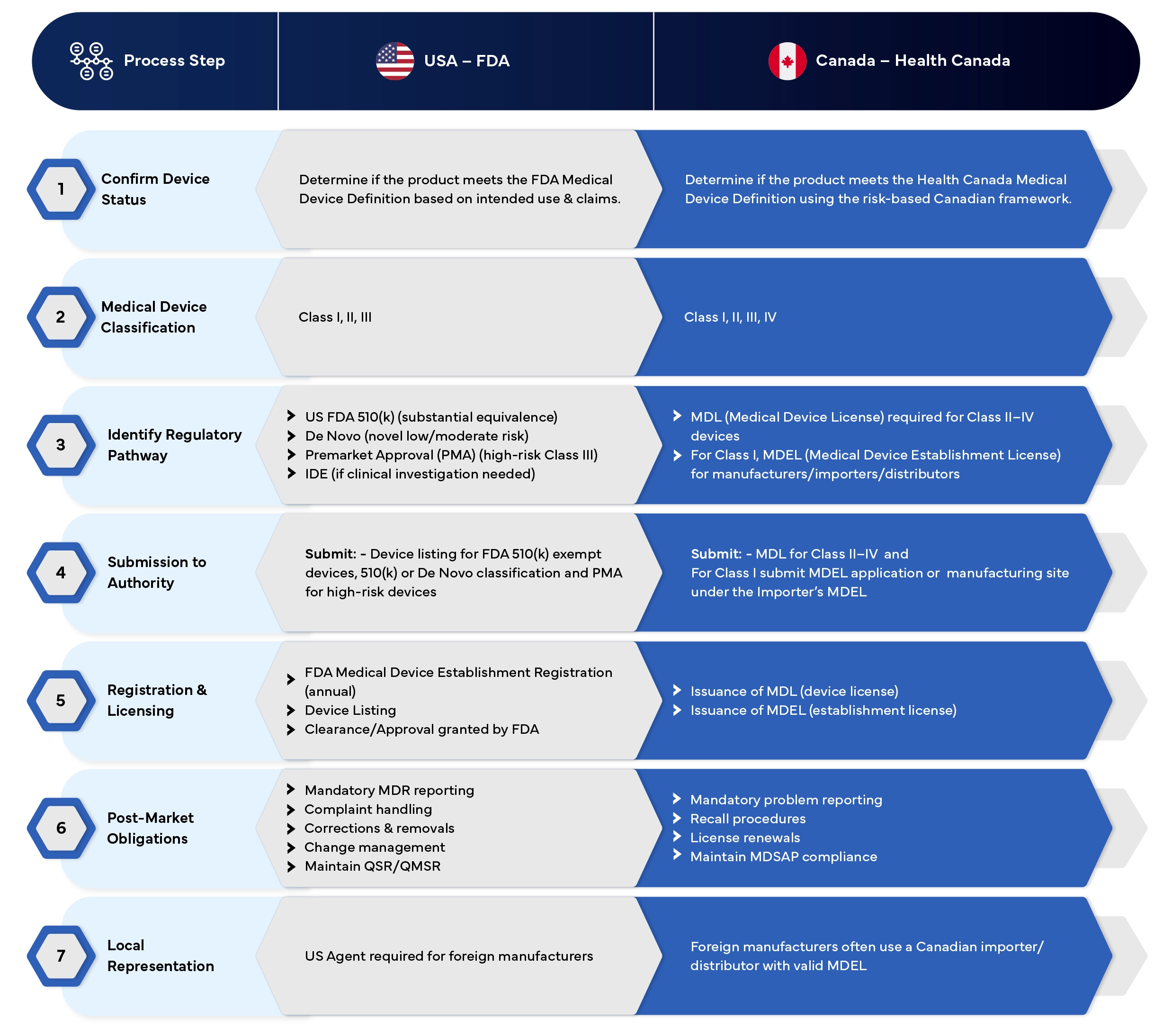
EUA vs Canadá
Processo de registo de dispositivos médicos - Tabela comparativa
Serviços de Registo de Dispositivos Médicos da Freyr
Registo de Dispositivos Médicos nas Américas
- Apoio de Inteligência Regulamentar e de Mercado
- Classificação de Produtos conforme os requisitos regulamentares
- Registo de Dispositivos Médicos nos US – 513 (G) & (Via Correta entre 510 (K)/De-NOVO/PMA/IDE)
- Reunião pré-submissão com as agências de saúde
- Apoio Regulamentar para Documentos de Produto, como o Design History File (DHF)
- Análise de Lacunas dos Documentos Técnicos e dos Sistemas de Boas Práticas de Fabrico (BPF).
- Apoio Regulamentar para a Compilação de Dossiê Técnico, conforme exigido pela respetiva Via de Registo
- Estratégia de Conformidade do Sistema de Qualidade USFDA (21 CFR 820)
- Serviços de conformidade com o Programa de Auditoria Única de Dispositivos Médicos (MDSAP)
- Registo de Dispositivos Médicos no Canadá – Registo de Licença de Dispositivo Médico (MDL) e Licença de Estabelecimento de Dispositivos Médicos (MDEL)
- Ligação e apoio à Agência de Saúde
- Representação no País – Serviços de Agente US e Pessoa Responsável Sanitária
- Atividades de Conformidade Pós-Aprovação

- Submissões bem-sucedidas para várias classes de dispositivos, desde software até suturas
- Acesso a afiliados locais para enfrentar os desafios da autoridade e requisitos específicos de idioma
- Pessoal dedicado e especializado para prestar apoio regulamentar a Dispositivos Médicos e IVD
- Modelo custo-eficaz para apoio de representação no país ou legal
- Entregámos com sucesso vários projetos nos EUA e no Canadá
- Com sede nos EUA.

Porquê colaborar com a Freyr?
- Experiência regulamentar End-to-end América End-to-end , abrangendo desde as notificações pré-comercialização (pedidos de autorização) junto FDA da Health Canada até à vigilância pós-comercialização e à conformidade ao longo do ciclo de vida do produto.
- Sucesso comprovado em mais de 1500 registos de dispositivos médicos a nível mundial, abrangendo dispositivos das Classes I a III nos US dispositivos das Classes I a IV no Canadá.
- Presença no terreno através dos serviços US e do apoio regulatório no Canadá, com o apoio de equipas de especialistas distribuídas por todo o mundo para uma execução sem falhas.
- Estratégia integrada US o Canadá que simplifica os requisitos em matéria de evidências, documentação e qualidade, com vista a reduzir custos, duplicações e prazos de aprovação.
- Interação direta com FDA a Health Canada, garantindo uma comunicação clara, respostas atempadas e um alinhamento proativo com as expectativas regulamentares.
- Contamos com a confiança de mais de 470 fabricantes de dispositivos médicos em todo o mundo, desde startups a empresas globais, como seu parceiro regulatório de longa data na América do Norte.












