Conformidade com o quadro regulamentar e de registo de dispositivos médicos na UE
A União Europeia representa um dos mercados de dispositivos médicos mais regulamentados e comercialmente atraentes do mundo. Com 27 member states, 3 EEA e a Turquia, o mercado da União funciona ao abrigo de um ecossistema regulamentar harmonizado, definido EU MDR 745/2017 EU MDR para dispositivos médicos e pelo Regulamento (UE) n.º 746/2017 (IVDR) para diagnósticos in vitro, garantindo normas uniformes de segurança e desempenho em todas as categorias de produtos. Para colocar legalmente um dispositivo no mercado da União Europeia, os fabricantes devem obter a marcação CE, que confirma a conformidade com a regulamentação aplicável com base na classificação de risco do dispositivo e na via de avaliação da conformidade. O incumprimento destes requisitos pode resultar em consequências graves, incluindo a recolha do produto, a apreensão na alfândega, a suspensão da certificação ou a perda total do acesso ao mercado.
Ao abrigo do atual regime regulamentar:
- A marcação CE é obrigatória para todos os dispositivos médicos e dispositivos de diagnóstico in vitro antes de poderem ser comercializados.
- O registo de dispositivos na EUDAMED está a ser introduzido por fases, e vários módulos já estão ativos para utilização obrigatória.
- A nomeação de um Representante Autorizado Europeu (EAR) é obrigatória para qualquer fabricante sediado fora daEEA.
- As regras de classificação mais rigorosas do MDR/IVDR exigem documentação técnica sólida, evidências clínicas ou de desempenho e um acompanhamento contínuo ao longo do ciclo de vida.
A Freyr apoia os fabricantes ao longo de todo este processo, facilitando uma entrada harmoniosa e em conformidade no mercado da União Europeia. Desde o desenvolvimento de uma estratégia de marcação CE e a elaboração da documentação técnica até à gestão dos pedidos junto dos organismos notificados e ao desempenho das funções de seu representante autorizado na UE, a Freyr garante a conformidade total com os regulamentos MDR/IVDR e um acesso sem obstáculos a todos member states da UE,EEA e à Turquia.
Processo passo a passo para a conformidade com a UE
O acesso ao mercado de um dispositivo médico e de um dispositivo de diagnóstico in vitro (IVD) no mercado da UE envolve várias etapas definidas. Eis como a Freyr gere todo o processo por si:
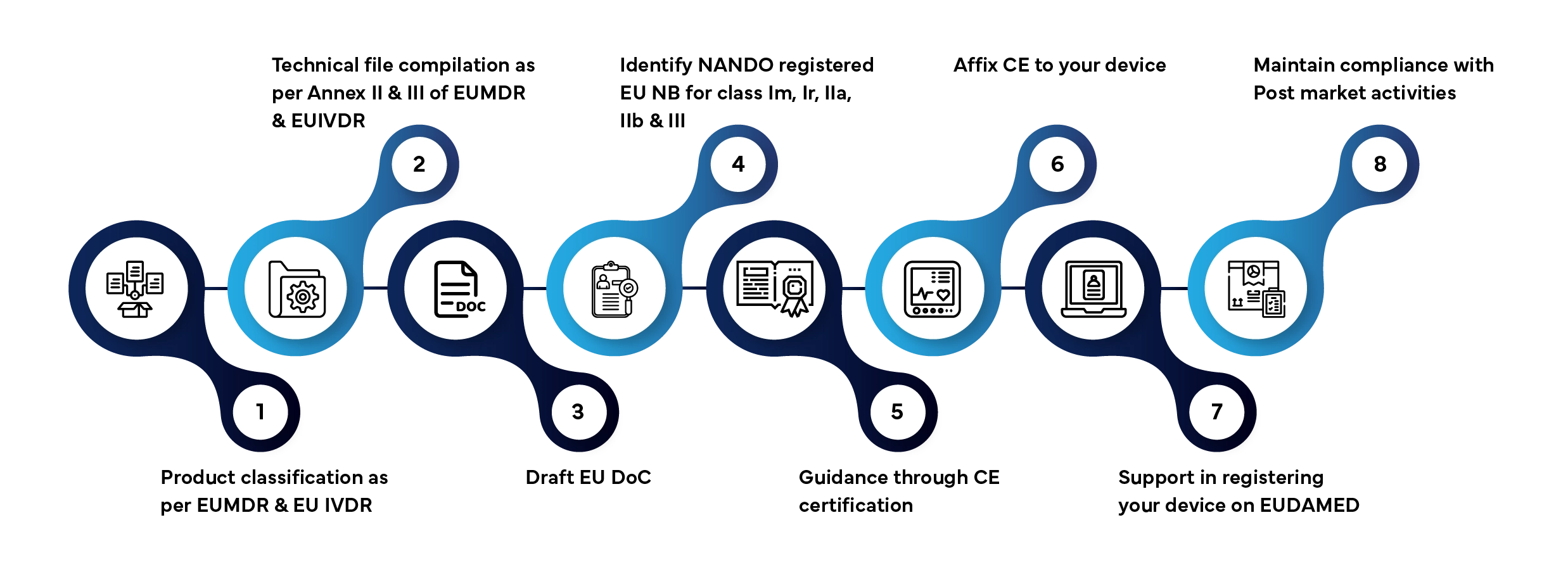
Prazo de processamento habitual: 3 a 12 meses, dependendo da classe do dispositivo e da disponibilidade da documentação.
Principais ofertas da Freyr Medical Device na UE
- Estratégia Regulamentar e Transição para o MDR/IVDR – Elaboramos planos de ação end-to-end , adaptados ao EU MDR ao IVDR EU MDR , garantindo uma transição harmoniosa dos regimes das diretivas e o alinhamento com os atuais requisitos da UE.
- Documentação Técnica e Avaliação da Conformidade – A nossa equipa presta apoio no desenvolvimento, revisão e apresentação dos seus Dossiers Técnicos / Dossiers de Projeto, presta assistência nas interações com os Organismos Notificados e gere a marcação CE, o apoio aos testes de segurança e desempenho dos dispositivos e os processos de conformidade.
- Avaliação clínica/de desempenho: A Freyr oferece serviços especializados de elaboração de CERs, PERs, planos PMCF, PSURs, SVR, CPR para dispositivos de diagnóstico in vitro (IVD), documentação de risco e conteúdos de avaliação biológica, garantindo clareza técnica e rigor regulamentar em todas as classes de dispositivos.
- Apoio ao registo UDI e EUDAMED – Asseguramos que o seu sistema de Identificação Única de Dispositivos (UDI) está em conformidade e prestamos assistência no registo na base de dados europeia de dispositivos EUDAMED e na gestão do ciclo de vida associada.
- Representante Autorizado Europeu (EAR) e Representação Local – Para fabricantes fora daEEA, atuamos como o seu Representante Autorizado Europeu (EAR) e prestamos apoio em matéria de conformidade nos member states da UE.
- Vigilância pós-comercialização (PMS) – A Freyr apoia-o no estabelecimento, implementação e manutenção de sistemas de PMS, incluindo o Plano de Vigilância Pós-Comercialização (PMSP), Relatório de Vigilância Pós-Comercialização (PMSR), Relatório Periódico de Atualização de Segurança (PSUR), planos de Acompanhamento Clínico/de Desempenho Pós-Comercialização (PMCF), relatórios de vigilância, FSCAs, FSNs e CAPAs, garantindo a manutenção contínua da marcação CE e o acesso sustentável ao mercado, em conformidade com o ciclo de vida do produto.
- Registo de dispositivos com marcação CE: A Freyr gere todo o processo de registo da marcação CE na UE, prestando apoio na avaliação da conformidade, elaborando documentos de submissão em conformidade, colaborando com os organismos notificados e garantindo aprovações atempadas em todas as categorias de dispositivos médicos e de diagnóstico in vitro.
- Apoio ao SGQ: Prestamos apoio à implementação e manutenção de Sistemas de Gestão da Qualidade ISO 13485, alinhados com os requisitos de qualidade e segurança EU MDR e com as expectativas dos organismos notificados.
- Conformidade da rotulagem: A nossa equipa garante que a sua rotulagem, instruções de utilização, embalagem e símbolos cumprem os requisitos do MDR/IVDR e os requisitos linguísticos multilingues da UE, mantendo a consistência e a conformidade nos 27 member states da UE.
Oferta de serviços de Representante Autorizado na UE (EAR)
Registo de dispositivos junto das autoridades da UE
Para os fabricantes não pertencentes à UE, a Freyr atua como Representante Autorizado na UE (EAR) nomeado, em conformidade com os requisitos do MDR/IVDR. Enquanto entidade sediada na Alemanha, a Freyr presta apoio nas atividades de registo de dispositivos junto da autoridade competente alemã relevante e mantém os registos regulamentares exigidos. Para Member States restantes Member States da UE, a Freyr presta apoio regulamentar, conforme aplicável, para ajudar a garantir a conformidade dos dispositivos e facilitar a sua colocação no mercado da União.
Documentação e Garantia de Conformidade
Os nossos especialistas em regulamentação verificam se a sua Declaração de Conformidade (DoC), os Certificados CE e os Dossiers Técnicos estão completos, atualizados e em conformidade com o MDR/IVDR. A Freyr garante que tudo está totalmente preparado para a avaliação da conformidade e a apresentação dos pedidos de marcação CE.
Resposta a pedidos de informações das autoridades competentes
Se necessário, a Freyr trata de toda a comunicação direta e dos pedidos de esclarecimento das autoridades competentes da UE ou dos organismos notificados em seu nome, garantindo respostas oportunas e precisas e ajudando a evitar atrasos nas aprovações ou nas revisões regulamentares pós-comercialização.
Vigilância e comunicação de incidentes
Na qualidade de seu EAR, a Freyr atua como principal ponto de contacto para as comunicações relacionadas com a segurança. Sempre que necessário, coordenamos as notificações de incidentes, as ações corretivas de segurança no terreno (FSCA) e os relatórios de vigilância entre o fabricante, os profissionais de saúde e as autoridades, a fim de garantir uma resposta adequada e o cumprimento da regulamentação.
Preparação para inspeções e auditorias
A Freyr mantém toda a documentação, correspondência e registos obrigatórios para auditorias e inspeções das autoridades. A nossa equipa garante que a documentação técnica, a rotulagem e os registos pós-comercialização estejam prontamente disponíveis e em total conformidade com os requisitos do MDR/IVDR.
Porquê colaborar com a Freyr?
- Conhecimento End-to-end , que vai desde o registo pré-comercialização até à vigilância pós-comercialização, gerindo todas as fases do processo de conformidade.
- Um histórico comprovado com mais de 2000 registos de dispositivos concluídos com sucesso em diversas categorias.
- Uma forte presença da UE com sede na Alemanha (EAR), complementada por especialistas em regulamentação no terreno em Reading e apoiada pelas equipas globais de implementação da Freyr.
- Um plano de transição personalizado que oferece apoio estratégico para obter a certificação CE de forma harmoniosa e económica.
- Equipas de entrega multirregionais com apoio no terreno através das operações da Freyr na UE, sediadas na Alemanha.
- Experiência comprovada na conformização com o MDR/IVDR e na transição de dispositivos antigos
- Gestão transparente do projeto com comunicação direta com o organismo notificado












