Visão Geral do Registo de Dispositivos Médicos nos EAU
Os Emirados Árabes Unidos (EAU), uma nação membro proeminente do GCC, possuem um sistema de saúde avançado. O seu potencial de mercado é comprovado e está em constante crescimento, regido pelo Departamento de Controlo de Medicamentos do Ministério da Saúde e Prevenção (MOHAP). A governação centralizada e as barreiras linguísticas são grandes obstáculos para o registo de dispositivos médicos nos EAU, juntamente com as complexidades linguísticas e a falta de canais de comunicação eficientes com as Autoridades de Saúde.
Autoridade Regulamentar: Departamento de Controlo de Medicamentos do Ministério da Saúde e Prevenção (MOHAP)
Regulamento: Diretriz de Registo de Dispositivos Médicos nos EAU
Via Regulamentar: Registo de produtos
Representante Autorizado: É necessário um Representante Autorizado Local dos EAU
Requisito de SGQ: ISO 13485:2016
Avaliação de Dados Técnicos: Comité de Registo de Dispositivos Médicos
Validade da Licença: 5 Anos
Requisitos de Rotulagem: Anexo 2 (2.5) das Diretrizes de Registo de Dispositivos Médicos dos EAU
Formato de Submissão: Documento
Idioma: Inglês
Classificação de Dispositivos Médicos dos EAU
Os EAU têm Regras de Classificação separadas para Dispositivos Médicos e IVDs. As regras de classificação de dispositivos médicos dos EAU estão em linha com as regras de classificação das Diretivas de Dispositivos Médicos da UE. A classe de dispositivos de acordo com as regras de classificação dos EAU é a seguinte:
| Critérios de Risco | Classe de Dispositivo Médico |
|---|---|
| Baixo Risco | I |
| Risco Baixo a Moderado | IIa |
| Risco Moderado – Elevado | IIb |
| Alto Risco | III |
| Critérios de Risco | Classe de IVD |
|---|---|
| Baixo Risco Individual e Baixo Risco para a Saúde Pública | A |
Risco Individual Moderado e/ou Baixo Risco para a Saúde Pública | B |
Alto Risco Individual e/ou Risco Moderado para a Saúde Pública | C |
| Alto Risco Individual e Alto Risco para a Saúde Pública | D |
Representante Autorizado Local dos EAU
Fabricantes estrangeiros, sem escritório físico, devem nomear um Representante Local (LR) para atuar em seu nome. O representante local deve ser licenciado pelo Ministério da Saúde como um armazém médico ou escritório científico (no caso de escritório científico, as atividades de importação e distribuição devem ser realizadas por um Armazém Médico Licenciado nomeado). Os requerentes podem nomear o seu distribuidor como Representante Local. No entanto, ter um Representante Local independente, sem interesse comercial, proporcionaria a flexibilidade necessária para nomear vários distribuidores nos EAU. Os detalhes tanto do LR como do distribuidor devem ser fornecidos durante o registo do dispositivo.
Processo de classificação oficial com o MoHAP dos EAU
O MoHAP dos EAU introduziu um serviço de classificação oficial, particularmente útil quando não tem a certeza se o seu produto requer registo. Este serviço classifica produtos de todos os tipos e formas com base na sua apresentação, composição, utilização e design. Os requisitos podem variar dependendo da natureza do produto, da classe de risco e do estado regulamentar.
A carta de classificação indica se um produto precisa de ser registado junto do MOHAP. Se o registo for necessário, o produto deve ser registado de acordo com a classe identificada na carta de classificação. Esta carta é válida por três anos a partir da data de emissão.
Os resultados da classificação oficial podem ser:
- Não requer registo no MOHAP
- Aprovado pelo MOHAP dos EAU como dispositivo médico, restrito a uso profissional
- Aprovado pelo MOHAP dos EAU como dispositivo médico de venda livre
Registo de Dispositivos Médicos dos EAU
Certos Dispositivos que não requerem registo de produto ou listagem prévia ou aprovação para importação. Tais produtos isentos de registo ou listagem devem solicitar e obter uma licença de importação para serem comercializados nos EAU.
Para outros dispositivos, as importações não serão autorizadas a menos que uma pré-aprovação para a importação da remessa seja emitida pelo DRCD. Tais dispositivos devem ser listados ou registados para importação nos EAU.
Listagem de Dispositivos: Geralmente, os produtos utilizados em hospitais sob supervisão profissional e os dispositivos de Classe I não são submetidos a uma avaliação detalhada e devem ser listados. Um Certificado de Listagem será emitido pela agência. Os dispositivos, após a listagem, devem obter uma licença de importação para comercializar os dispositivos nos EAU.
Registo de Dispositivos: A atividade de Registo inclui o Registo do Local e do Produto.
- Registo do Local:O local de fabrico deve ser registado, se o dispositivo fabricado nesse Local estiver a ser importado para os EAU pela primeira vez. Para os dispositivos subsequentes fabricados no mesmo local, apenas o registo do dispositivo será suficiente, e o registo do local não é necessário.
- Registo do Dispositivo:Estes dispositivos estão sujeitos a revisão pelo comité técnico que, após aprovação, concederá um certificado de licença.
Fluxo do processo
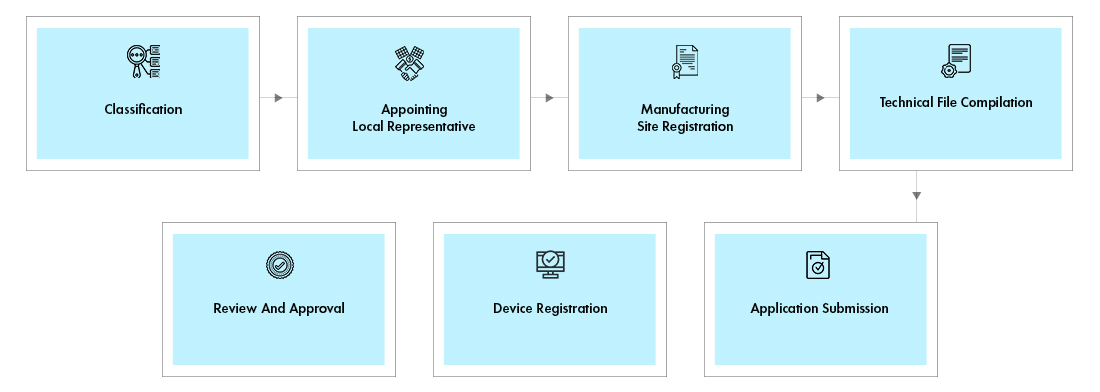
Gestão do Ciclo de Vida do Dispositivo Pós-Aprovação
- Gestão de alterações pós-aprovação - modificações às aprovações existentes de Dispositivos Médicos, tais como, adição de novas variantes, acessórios; adição de novas indicações de utilização, entre outras
- Manutenção das aprovações e do registo através do pagamento atempado das taxas administrativas e de registo
- Renovação de licenças
- Ligação entre o Ministério da Saúde e o fabricante
- Gestão da Importação
Com um centro de entrega exclusivo no Dubai, a Freyr detém uma posição de autoridade no mercado de dispositivos médicos dos EAU e descreve a classificação dos dispositivos, além de descodificar os regulamentos de orientação para uma melhor conformidade. Apoiamos os clientes na compilação de documentos de acordo com as normas e, assim, garantimos aprovações rápidas. A Freyr oferece uma gama completa de serviços regulamentares relacionados com a comercialização bem-sucedida de dispositivos.
Resumo
| Tipo de Dispositivo | Listagem de Dispositivos | Registo de Dispositivos | Licença de Importação |
|---|---|---|---|
Dispositivo Isento de Aprovação Pré-Importação (Conforme listado no Anexo 3) | N/A | N/A | SIM |
| SIM | N/A | SIM |
| Todos os Outros Dispositivos | N/A | SIM | SIM |
Experiência Freyr
- Inteligência Regulatória
- Due Diligence Regulamentar
- Classificação Formal de Dispositivos Médicos
- Registo de Dispositivos
- Representação Autorizada nos EAU
- Apoio à Tradução
- Apoio à Rotulagem
- Identificação e qualificação de distribuidores
- Gestão de Alterações Pós-Aprovação
- Renovação e transferência de licenças
- Desalfandegamento