Descrição do Trabalho (SOW) para a apresentação de dispositivos médicos ativos e não ativos ao abrigo do procedimento 510(k) – Visão geral
Na Freyr, a nossa equipa de especialistas compila e sintetiza meticulosamente as informações mais recentes e essenciais para os seus pedidos de 510(k), abrangendo tanto dispositivos médicos ativos como não ativos. Isto garante que dispõe dos conhecimentos necessários para navegar com confiança pelo quadro regulamentar. Desde esclarecer as diferenças entre dispositivos ativos e não ativos até aprofundar as complexidades da submissão 510(k), criámos um extenso repositório de recursos para sua consulta principal. Embarque numa jornada para dominar a submissão 510(k) de dispositivos médicos ativos e a submissão 510(k) de dispositivos médicos não ativos com o nosso guia completo.
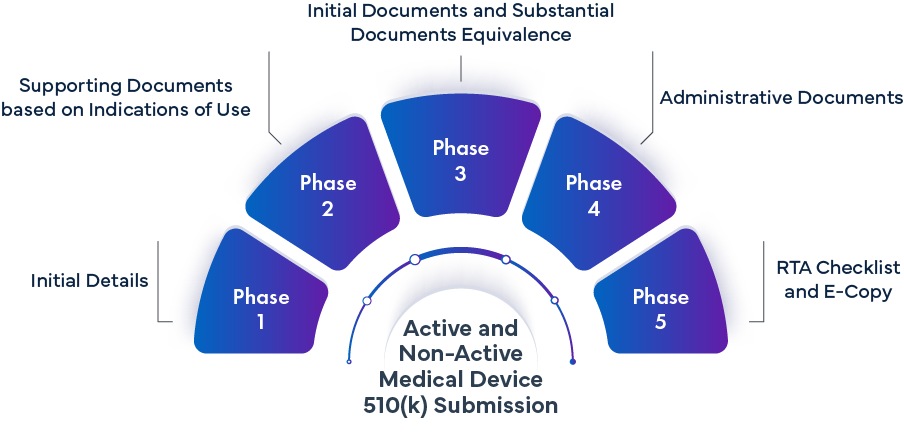
Fase -1 Detalhes Iniciais | ||
|---|---|---|
Requisitos | Âmbito do Candidato 510(k) | Âmbito da Freyr |
| Utilização prevista |
|
|
| Declaração de Indicações de Utilização (Formulário 3881) |
|
|
| Descrição do Dispositivo |
|
|
| Normas e Orientações |
|
|
| Dispositivo Predicado |
|
|
| Resumo do 510(k) |
|
|
Fase 2: Documentação de Apoio com base nas Indicações de Utilização | |||
|---|---|---|---|
Requisitos de Documentos. | Âmbito do Candidato 510(k) | Âmbito da Freyr | |
| 2.1 | Desenho do Dispositivo | Submeter o ficheiro de desenho do dispositivo para garantir uma representação precisa do design do dispositivo. | Iniciar um pedido formal para um Desenho de Dispositivo de um dispositivo Ativo. Rever e documentar minuciosamente as informações necessárias para a submissão 510(k). |
| 2.2 | Conceção e Desenvolvimento do dispositivo | Submeter o processo de conceção e desenvolvimento do dispositivo Ativo, abrangendo toda a informação e documentação relevante. | Submeter um pedido para a conceção e desenvolvimento de um dispositivo ativo. Rever e documentar minuciosamente todas as informações necessárias em preparação para a submissão 510(k). |
| 2.3 | Ficha de Dados de Segurança do Material | Fornecer as Fichas de Dados de Segurança de Materiais (MSDS) para os componentes essenciais do dispositivo ativo, garantindo informações abrangentes sobre a sua segurança e composição. | Enviar um pedido para uma Ficha de Dados de Segurança de componentes cruciais do dispositivo Ativo. Rever e documentar minuciosamente todas as informações necessárias em preparação para a submissão 510(k). |
| 2.4 | Fluxograma de Fabrico | Fornecer um Fluxograma de Fabrico que detalhe o processo de produção do dispositivo ativo, apresentando uma representação visual das etapas de fabrico e da sua sequência. | Apresentar um pedido da Ficha de Dados de Segurança (MSDS) dos componentes essenciais para o dispositivo ativo. Rever e documentar minuciosamente todas as informações necessárias em preparação para a submissão 510(k). |
| 2.5 | Descrição do Dispositivo | Fornecer detalhes abrangentes, incluindo: o Uma visão geral do dispositivo. o Funções e modos de funcionamento o Diagramas de blocos. o Fotografias, cabos e acessórios relevantes o Interoperabilidade do dispositivo. o Descrição da fonte de alimentação. | Submeter um pedido de informações detalhadas sobre o dispositivo. Rever e documentar minuciosamente todas as informações necessárias em preparação para a submissão 510(k). |
| 2.6 | Rotulagem Proposta | Fornecer as Instruções de Utilização (IFU), o Manual do Utilizador e qualquer material promocional associado para o dispositivo ativo. | Apresentar um pedido das Instruções de Utilização (IFU), do Manual do Utilizador e de qualquer material promocional, se disponível. Rever as IFU, o Manual do Utilizador e o material promocional fornecido pelo requerente. Documentar as IFU, o Manual do Utilizador e o material promocional para efeitos de submissão 510(k). |
| 2.7 | Embalagem e Transporte | Fornecer os planos e relatórios de estudo para a validação de embalagem e transporte. | Submeter um pedido para o plano e relatórios de estudo relativos à Validação de Embalagem e Transporte. Rever os planos e relatórios de estudo para a Validação de Embalagem e Transporte e fornecer quaisquer correções ou feedback necessários. |
| 2.8 | Esterilização (Se a esterilidade for aplicável) | Fornecer os planos e relatórios de estudo para a Validação de Esterilização. | Submeter um pedido para o plano e relatórios de estudo da Validação de Esterilização. Rever e documentar minuciosamente todas as informações necessárias em preparação para a submissão 510(k). |
| 2.9 | Testes de Desempenho _ Bancada | Iniciar um pedido formal para os planos e relatórios dos Estudos de Bancada de testes de desempenho, descrevendo os requisitos e objetivos específicos a serem abordados | Submeter um pedido para os planos e relatórios do Estudo de Bancada do dispositivo ativo para testes de desempenho. Rever e documentar minuciosamente todas as informações necessárias em preparação para a submissão 510(k). |
Documentação de Suporte para Compatibilidade Eletromagnética e Segurança Elétrica | |||
| 2.10 | Características do Dispositivo Relacionadas com a EMC e Ambientes de Utilização Previstos | Fornecer detalhes sobre as Características do Dispositivo Relacionadas com EMC e os Ambientes de Utilização Prevista, incluindo: o Uma visão geral do dispositivo. o Funções e modos de funcionamento. o Diagramas de blocos. o Fotografias, cabos e acessórios relevantes. o Interoperabilidade do dispositivo. o Descrição da fonte de alimentação, incluindo a viabilidade de utilizar o dispositivo médico com alimentação interna durante o carregamento. o Ambientes em que o dispositivo médico se destina a ser utilizado. o Descrição de qualquer tecnologia sem fios (se aplicável) para considerações adicionais relativas a dispositivos médicos com capacidade sem fios. o Descrição de quaisquer emissores de RF internos no dispositivo médico que poderiam causar perturbações eletromagnéticas. o Abordar emissores eletromagnéticos (EM) comuns, bem como emissores médicos únicos.
| Submeter um pedido de informações relativas às características do dispositivo relacionadas com EMC e aos ambientes de utilização prevista. Rever e documentar minuciosamente todas as informações necessárias em preparação para a submissão 510(k). |
| 2.11 | Avaliação de Risco | Fornecer um Plano de Gestão de Risco que inclua uma avaliação de risco demonstrando uma mitigação eficaz de riscos, juntamente com um relatório abrangente de gestão de risco que abranja todos os elementos de risco. Fornecer o documento revisto com as correções e melhorias sugeridas | Submeta um pedido para o Ficheiro de Gestão de Risco e solicite a documentação do Plano de Gestão de Risco e do Relatório, incluindo a identificação de perigos de risco, a avaliação de risco e a demonstração de mitigação de risco adequada. O Relatório de Gestão de Risco deve cobrir todos os elementos de risco, preferencialmente com secções separadas para maior clareza. Fornecer um modelo do Plano de Gestão de Risco e do Relatório de Gestão de Risco que abranja todos os riscos relacionados com o dispositivo, mediante pedido do requerente. Rever os dados no Processo de Gestão de Risco, incluindo o Plano e o Relatório partilhados pelo requerente, e fornecer sugestões para correções necessárias para garantir uma documentação abrangente para a submissão 510(k). Rever e documentar minuciosamente todas as informações necessárias em preparação para a submissão 510(k). |
| 2.12 | Norma de Consenso | Fornecer a confirmação das normas de consenso relevantes e uma explicação de quaisquer desvios das normas reconhecidas pela FDA. | Submeter um pedido para as normas de consenso aplicáveis relacionadas com EMC e segurança elétrica para o dispositivo Ativo. Documentar as normas de consenso confirmadas para o dispositivo ativo para efeitos de submissão 510(k). |
| 2.13 | Critérios de Aprovação/Reprovação de Desempenho Essencial e Imunidade | Apresentar o plano de estudo e os relatórios dos testes de Desempenho Essencial e Imunidade realizados no dispositivo ativo, em conformidade com as normas reconhecidas pela FDA. | Apresentar uma requisição para o plano de estudo e os relatórios dos testes de Desempenho Essencial e Imunidade realizados no dispositivo ativo, em conformidade com as normas reconhecidas pela FDA. Rever e documentar minuciosamente todas as informações necessárias em preparação para a submissão 510(k). |
| 2.14 | Configuração e Funções Testadas de Dispositivos Médicos | Fornecer a Configuração do Dispositivo Médico e as Funções Testadas para o dispositivo ativo, abrangendo os seguintes detalhes: o Fornecer uma descrição abrangente do dispositivo médico em teste, incluindo informações detalhadas sobre a sua configuração, funções, modos e as definições específicas que foram testadas. o A descrição do dispositivo em teste deve abranger o nome do dispositivo médico, o número do modelo e indicar se o dispositivo é o dispositivo médico final pronto para produção atualmente em análise. | Submeter um pedido para a configuração e funções de teste do dispositivo médico ativo. Rever e documentar minuciosamente todas as informações necessárias em preparação para a submissão 510(k). |
| 2.15 | Resultados dos Testes de EMC | Fornecer o plano de estudo e o relatório dos testes de EMC (Compatibilidade Eletromagnética) em conformidade com a norma de consenso reconhecida pela FDA recomendada para o dispositivo ativo. | Iniciar um pedido formal para o plano de estudo e o relatório dos testes de EMC, alinhado com a norma de consenso reconhecida pela FDA recomendada para dispositivos ativos. Rever e documentar minuciosamente todas as informações necessárias em preparação para a submissão 510(k). |
Fase 3 – Documentos Iniciais e Documentos de Equivalência Substancial | |||
|---|---|---|---|
Requisitos de Documentos. | Âmbito do Candidato 510(k) | Âmbito da Freyr | |
| 3.1 | Folha de Rosto de Submissão para Revisão Pré-Comercialização do CDRH (Formulário FDA 3514) | - | Preencher o Formulário FDA 3514 utilizando os detalhes fornecidos pelo requerente. |
| 3.2 | Resumo e Certificação da Classe III | - | Este passo não é necessário se os estudos clínicos não forem exigidos. |
| 3.3 | Certificação Financeira ou Declaração de Divulgação | - | Este passo não é necessário se os estudos clínicos não forem exigidos. |
| 3.4 | Resumo Executivo | - | Desenvolver um modelo e preparar meticulosamente o documento. Fornecer justificações para quaisquer discrepâncias observadas entre o dispositivo proposto e o dispositivo de referência. Estudo comparativo entre o dispositivo proposto e o dispositivo de referência, com criação de um modelo e preparação do documento correspondente. |
| 3.5 | Discussão de Equivalência Substancial | - | Desenvolver um modelo e preparar meticulosamente o documento. Estudo comparativo entre o dispositivo proposto e o dispositivo de referência, com criação de um modelo e preparação do documento correspondente. |
Fase 4 – Documentos Administrativos | |||
|---|---|---|---|
Requisitos de Documentos. | Âmbito do Candidato 510(k) | Âmbito da Freyr | |
| 4.1 | Carta de Apresentação 510(k) | Assine o documento impresso em papel timbrado da empresa e providencie o envio de uma cópia impressa por correio para o escritório US. Fornecer uma cópia digital da carta de apresentação 510(k) assinada para inclusão na documentação 510(k) | Preparar um modelo abrangente que inclua todos os detalhes necessários para a carta de apresentação e fornecê-lo ao requerente. Instruir o requerente a usar o seu papel timbrado oficial e garantir que a carta de apresentação seja assinada por uma pessoa autorizada |
| 4.2 | Declaração de Veracidade e Exatidão | Garantir que o documento seja assinado pela pessoa de contacto designada na empresa e fornecido em conformidade. | Desenvolver um modelo abrangente que contenha todo o conteúdo necessário a ser incluído no documento de submissão. |
| 4.3 | Declarações de conformidade e Relatório de síntese | Garantir que o documento seja assinado pela pessoa de contacto designada na empresa e fornecido em conformidade. | Desenvolver um modelo abrangente para listar e preparar sistematicamente os documentos necessários. |
| 4.4 | MDFUSC (Formulário FDA 3601) | Submeter o pagamento exigido à FDA antes da submissão formal do processo 510(k). | Gerar uma folha de rosto da taxa de utilizador e um Número de Identificação Pessoal (PIN) único especificamente para a submissão do dispositivo médico. |
Fase 5 – Lista de Verificação RTA e Cópia Eletrónica | |||
|---|---|---|---|
Requisitos de Documentos. | Âmbito do Candidato 510(k) | Âmbito da Freyr | |
| 5.1 | Lista de Verificação RTA | Aprovação para a Verificação da Lista de Verificação RTA (Pronto para Aceitar), indicando que todos os requisitos foram cumpridos com sucesso | Desenvolver um modelo personalizado de Lista de Verificação RTA, adaptado ao tipo específico de submissão. Preencher a lista de verificação preenchendo meticulosamente todos os campos obrigatórios e garantindo que os documentos mencionados são devidamente submetidos à FDA e partilhados com o requerente. |
| 5.2 | Cópia Eletrónica | Aprovação da documentação contida na Pasta de Submissão Final, significando a sua conformidade com todos os requisitos e normas necessários. | Organizar as secções da pasta de submissão em conformidade com a Orientação da FDA e partilhá-las prontamente com o requerente. Converter a pasta de submissão numa cópia eletrónica para acesso e revisão convenientes. Submeta a cópia eletrónica da submissão ao Agente US designado. |
Registo de Dispositivos Médicos
- Estratégia Regulamentar abrangente da US FDA
- Identificação de Dispositivo Predicado
- Estabelecer Equivalência Substancial com Dispositivo Predicado
- Análise de Lacunas para Conformidade com a US FDA
- Compilação de 21 secções do Ficheiro Técnico 510(k)
- Publicação e criação de eCopy
- Validação e submissão de eCopy
- Serviços de Coordenação para Aprovação de Dispositivos
- Tratamento da resposta RTA e das deficiências
- Serviços de consulta para abordar deficiências
- Registo de Dispositivos e manutenção da base de dados FURLS

- Gerimos muitos registos 510(k) de diversas categorias de dispositivos
- Equipa especializada para a compilação de 510(k) de acordo com os requisitos da Notificação Pré-Comercialização (510(k)) da FDA dos US
- Apoio adicional para gerir questões 510(k)
- Aconselhamento sobre o tipo adequado de 510(k) de acordo com os requisitos de submissão 510(k) da FDA dos US para o dispositivo
- Submissão atempada dos resultados
- Atualizado com as novas alterações da US FDA

