Visão Geral do Registo de Dispositivos Médicos na Argentina
A Argentina é um dos países da América Latina em rápido desenvolvimento que oferece oportunidades para empresas de dispositivos médicos, com um sistema de saúde conhecido pela sua dedicação à segurança do paciente e a serviços médicos de alta qualidade. O registo de dispositivos médicos na Argentina é supervisionado pela autoridade regulamentar – a Administração Nacional de Medicamentos, Alimentos e Dispositivos Médicos (ANMAT).

Autoridade Regulamentar: Administração Nacional de Medicamentos, Alimentos e Dispositivos Médicos (ANMAT)
Regulamentos: Disposição 2318/2002 e Disposição 727/2013
Via Regulamentar: Sistema Eletrónico de Notificação de Dispositivos Assistido por Web (WAND)
Representante Autorizado: Representante Autorizado Argentino (AAR)
Requisito de QMS: ISO 13485 (ANMAT MDS), e MDSAP (Membro Afiliado)
Avaliação de Dados Técnicos: Administração Nacional de Medicamentos, Alimentos e Dispositivos Médicos (ANMAT)
Requisitos de Rotulagem: Anexo III.B da Disposição 2318/2002 e Anexo V da Disposição 727/2013.
Formato de Submissão: Eletrónico (portal HELENA)
Idioma: Espanhol
Classificação de Dispositivos Médicos na Argentina
No processo regulamentar da ANMAT, o primeiro passo para determinar o caminho do registo e a conformidade com os regulamentos da Argentina é determinar a classificação do dispositivo médico. Na Argentina, os dispositivos são classificados em quatro (04) classes com base no risco (Classe I-IV).
| Classe de Dispositivo Médico | Critérios |
|---|---|
| Classe I | Baixo Risco |
| Classe II | Risco Baixo - Moderado |
| Classe III | Risco Alto - Moderado |
| Classe IV | Alto Risco |
| Classe de IVD | Critérios |
|---|---|
| Classe A | Diagnóstico de doenças não infeciosas ou não transmissíveis. |
| Classe B | Diagnóstico de doenças infeciosas, exceto as pertencentes à Classe C. |
| Classe C | Diagnóstico de doenças infeciosas sexualmente transmissíveis, ou transmitidas pelo sangue ou seus derivados, bem como para a identificação de grupos sanguíneos. |
| Classe D | Para autoavaliação. |
Representante Autorizado Argentino (AAR)
O titular do registo de qualquer dispositivo médico na Argentina é legalmente responsável pelo registo e comercialização do dispositivo no país. Este pode ser o fabricante do dispositivo, ou pode ser um representante autorizado local (AAR) na Argentina a atuar em nome do fabricante.
Todos os dispositivos médicos comercializados na Argentina devem ser registados na ANMAT. O processo de registo pode ser complexo e demorado, pelo que é frequentemente recomendado que os fabricantes estrangeiros nomeiem um AAR para os auxiliar.
Registo de Dispositivos Médicos ANMAT
O processo de registo de dispositivos médicos da ANMAT é semelhante aos processos brasileiros de notificação e registo, com o grau de escrutínio envolvido para a aprovação a aumentar com base na classificação do dispositivo (Classe I, II, III e IV). Todos os fabricantes de dispositivos médicos devem também cumprir o ANMAT-MDS, que é o equivalente argentino do BGMP e está também em conformidade com a ISO 13485:2016.
Fluxo do processo
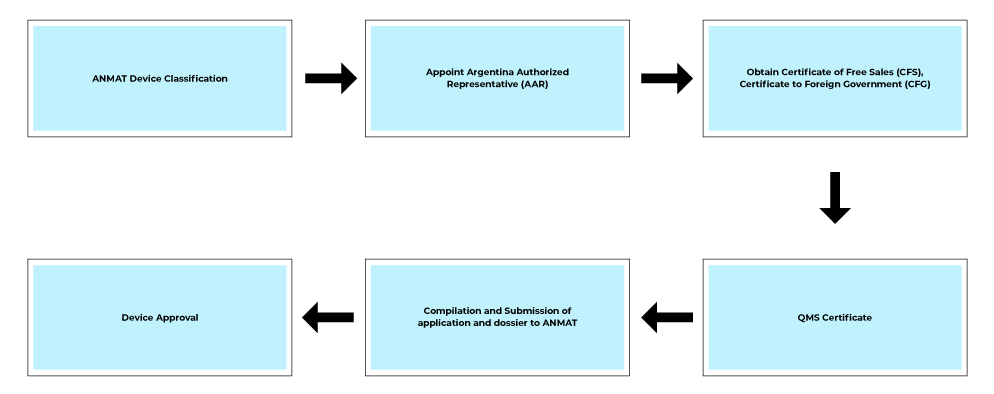
Serviços Pós-aprovação
A Freyr apoia fabricantes estrangeiros com a gestão End-to-End do ciclo de vida de dispositivos médicos, incluindo atividades pós-aprovação, tais como –
- Gestão de alterações pós-aprovação – modificações às aprovações existentes de dispositivos médicos, como a adição de novas variantes, acessórios e a adição de novas indicações de uso, entre outras.
- Manutenção de aprovações e registos através do pagamento atempado de taxas administrativas e de registo.
- Renovação de licenças.
- Atuação como intermediário entre a ANMAT e o fabricante.
- Notificação de eventos adversos.
- Gestão de importação.
A Freyr auxilia os fabricantes na identificação da classificação do dispositivo como primeiro passo. A Freyr ajuda os clientes a navegar pelo percurso regulamentar e a obter certificações, ajudando a retificar os problemas regulamentares envolvidos. Com experiência comprovada no lançamento de numerosos dispositivos na região, a Freyr oferece serviços regulamentares End-to-End para dispositivos médicos.
Resumo
| Classe de Dispositivos | Via de Registo (Notificação ou Registo Completo) | Prazos da Agência de Saúde | Validade do Registo (anos) |
|---|---|---|---|
| Dispositivos de Classe I | Registo completo | 4-6 meses | 5 anos |
| Dispositivos de Classe II | Registo completo | 4-6 meses | 5 anos |
| Dispositivos de Classe III | Registo completo | 6-8 meses | 5 anos |
| Dispositivos de Classe IV | Registo completo | 6-8 meses | 5 anos |
*Tenha em atenção que fatores como limitações de largura de banda, atualizações regulamentares e outras variáveis podem levar a extensões nos prazos da Autoridade de Saúde.
Experiência Freyr
- Serviços de Relatórios de Inteligência Regulatória.
- Serviços de Classificação Oficial.
- Compilação de Documentos Técnicos.
- Serviços de Registo de Dispositivos.
- Serviços de Representante Autorizado na Argentina (AAR).
- Serviços de Importação.
- Licenças de Funcionamento e Autorizações.
- Serviços de Tradução.
- Serviços de Rotulagem e Artwork.
- Serviços de Identificação e Qualificação de Distribuidores.
- Vigilância Pós-Comercialização.
- Serviços de Renovação e Transferência de Licenças.
