Visão Geral do Registo de Dispositivos Médicos no Egito
Desde setembro de 2018, o registo de dispositivos médicos tornou-se obrigatório no Egito. A indústria de dispositivos médicos no país tem registado um crescimento consistente, tornando-se um mercado atrativo para fabricantes e distribuidores. Com uma avaliação de 4,0 mil milhões de dólares em 2021, prevê-se que o mercado egípcio de dispositivos médicos atinja uma Taxa de Crescimento Anual Composta (CAGR) superior a 3% de 2022 a 2027. A importação satisfaz em grande parte a procura de dispositivos médicos no Egito, dada a produção local relativamente baixa. Notavelmente, o mercado egípcio de dispositivos médicos é o segundo maior na região do Médio Oriente e Norte de África (MENA). Esta visão geral explora aspetos chave do processo de registo egípcio, oferecendo informações sobre o quadro regulamentar e os requisitos para trazer dispositivos médicos inovadores para a vanguarda do setor da saúde do Egito.
Autoridade de Regulamentação: Autoridade Egípcia de Medicamentos (EDA)
Regulamentação: Lei Egípcia de Dispositivos Médicos Lei n.º 10 de 2003
Percurso de Regulamentação: Registo de Produto (Normal e Via Rápida) e Classificação Oficial
Representante Autorizado Local no Egito: Titular de Registo Egípcio (ERH)
Requisito de QMS: ISO 13485
Avaliação de Dados Técnicos: O Centro de Política e Planeamento de Medicamentos (DPPC) e a Administração Central de Assuntos Farmacêuticos (CAPA).
Validade da Licença: Dez (10) anos
Formato de Submissão: Em Papel e Eletrónico
Tradução: Documentos Traduzidos em Árabe e Inglês
Classificação de Dispositivos Médicos
No Egito, a classificação de dispositivos médicos alinha-se com o sistema europeu de classificação, que categoriza os dispositivos médicos com base na sua utilização pretendida e nos riscos potenciais associados à sua utilização. Os fabricantes devem identificar a classificação correta dos seus dispositivos para garantir a conformidade com os requisitos regulatórios e obter as aprovações necessárias para a comercialização e distribuição no Egito.
Classes de Dispositivos Médicos
| Classe | Risco |
|---|---|
| Classe I | Baixa |
| Classe IIa | Baixo-Médio |
| Classe IIb | Médio-Alto |
| Classe III | Elevada |
Representante Autorizado Local do Egito
As empresas de dispositivos médicos sediadas fora do Egito devem designar um Agente Local denominado “Titular de Registo Egípcio (ERH)” para gerir a submissão de pedidos de registo e dossiês à EDA em seu nome. O ERH funciona como um elo de ligação entre o fabricante e a autoridade regulamentar, garantindo a preparação e submissão precisas de toda a documentação necessária e verificando se o dispositivo médico cumpre os padrões de segurança, qualidade e eficácia da EDA. Além disso, o ERH é responsável por preservar a documentação de registo, comunicar incidentes ou recolhas e garantir a conformidade contínua com todas as normas e regulamentos aplicáveis durante todo o ciclo de vida do dispositivo. O Titular de Registo Egípcio (ERH) é inteiramente responsável por assegurar o registo de um dispositivo médico junto da EDA, particularmente na Administração Central de Dispositivos Médicos. Este papel envolve garantir a conformidade do dispositivo com os requisitos regulamentares da EDA para comercialização e distribuição no Egito.
Registo de Dispositivos Médicos
A obtenção da autorização de introdução no mercado para um dispositivo médico no Egito engloba várias etapas, incluindo a preparação da documentação necessária, a submissão da submissão à EDA, a adesão aos requisitos de classificação e sistema de qualidade, a nomeação de um ERH, se necessário, e o cumprimento das obrigações pós-comercialização. O processo de registo é crucial para garantir que os dispositivos médicos se alinham com os padrões de segurança, qualidade e eficácia prescritos estabelecidos pela Autoridade Regulamentar Egípcia. A documentação necessária pode diferir com base na via de registo escolhida, mas geralmente abrange o seguinte:
- Certificado CE (se aplicável).
- Certificado de Livre Venda (CFS).
- Certificação ISO 13485.
- Declaração de Conformidade (DOC).
Fluxo do Processo
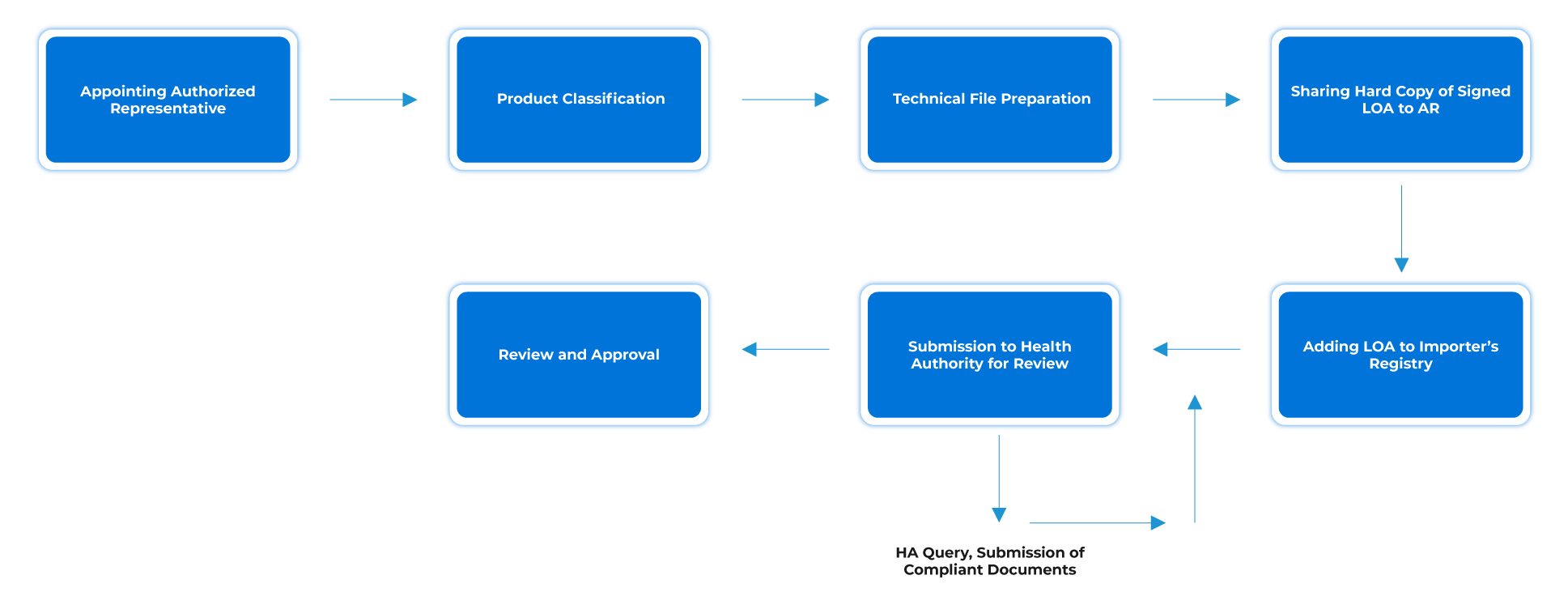
Gestão do Ciclo de Vida do Dispositivo Pós-aprovação
A Freyr oferece apoio abrangente a fabricantes estrangeiros na gestão de todo o ciclo de vida dos dispositivos médicos no Egito, incluindo atividades pós-aprovação:
- Gestão de alterações pós-aprovação, abordando modificações às aprovações existentes de dispositivos médicos, como a adição de novas variantes, acessórios e indicações de utilização.
- Manutenção da ISO 13485:2016.
- Certificação CE.
- Atuar como intermediário entre o Organismo Notificado (ON) e o fabricante.
- Um sistema de vigilância implementado para monitorizar a segurança do dispositivo médico após a concessão da Autorização de Introdução no Mercado.
- Fornecer atualizações periódicas relativamente à segurança e eficácia do dispositivo médico, bem como quaisquer alterações no estado regulamentar noutras jurisdições.
- Renovação da Autorização de Introdução no Mercado, dependendo do tipo de dispositivo e da regulamentação, após um determinado período.
A gestão eficaz da Vigilância Pós-Comercialização (PMS) no Egito implica navegar habilmente pelos quadros regulamentares estabelecidos pela EDA. Os novos participantes no mercado que enfrentam estas complexidades e que não possuem um parceiro regulamentar estabelecido podem aproveitar os extensos serviços regulamentares oferecidos pela Freyr. Estes serviços contribuem para um processo de aprovação contínuo para dispositivos médicos no Egito, garantindo a conformidade contínua com o cenário regulamentar e a dinâmica do mercado em constante evolução.
Registo de Dispositivos Médicos no Egito: Especialização
- Inteligência Regulatória.
- Due Diligence Regulatória.
- Classificação de Dispositivos Médicos.
- Registo de Dispositivos.
- Titular do Registo Egípcio.
- Apoio à Tradução.
- Redação Médica.
- Apoio à Rotulagem.
- Identificação e Qualificação de Distribuidores.
- Gestão de Alterações Pós-Aprovação.
- Renovação e Transferência de Licença.
- Desalfandegamento.

