Visão Geral do Registo de Dispositivos Médicos em Israel
A indústria de dispositivos médicos de Israel está a registar um crescimento e inovação sustentados, tornando-se um centro para tecnologias de saúde de ponta. O registo de dispositivos médicos é crucial para as empresas que entram neste mercado dinâmico. Esta visão geral explora os aspetos chave do processo de registo em Israel, oferecendo informações sobre o quadro regulamentar e os requisitos para colocar dispositivos médicos inovadores na vanguarda do setor da saúde de Israel.
Autoridade Regulamentar: A Divisão de Dispositivos Médicos do Ministério da Saúde israelita (AMAR).
Regulamentação: Lei de Dispositivos/Equipamentos Médicos de 2012
Via Regulamentar: Registo de Produto
Representante Autorizado Local em Israel: Titular do Registo em Israel (IRH)
Requisito de QMS: ISO 13485
Avaliação de Dados Técnicos: O Departamento de Dispositivos Médicos do Ministério da Saúde
Validade da Licença: Cinco (05) anos
Formato de Submissão: Em Papel e Eletrónico
Tradução: Documentos Traduzidos para Hebraico
Classificação de Dispositivos Médicos
A Lei e os Regulamentos de Equipamentos Médicos para o Registo de Equipamentos Médicos em Israel não especificam um sistema de classificação de risco. Em vez disso, Israel alinha a sua classificação de dispositivos médicos com as normas internacionais, particularmente as delineadas pelos países do Global Harmonization Task Force (GHTF). Em alternativa, a classificação de risco de um dispositivo num país reconhecido é adotada para o registo em Israel. Este processo de classificação considera tipicamente a utilização pretendida, o nível de risco e outros fatores que podem afetar a segurança e a eficácia dos dispositivos médicos.
Classes de Dispositivos Médicos
| Classe | Risco |
|---|---|
| Classe I | Baixa |
| Classe II | Baixo-Médio |
| Classe III | Elevada |
Alterações Propostas às Vias de Registo
As modificações propostas aplicam-se aos dispositivos de Classe I e Classe II, enquanto o sistema de registo para dispositivos de Classe III permanece inalterado.
- Os dispositivos de Classe I podem ser imediatamente registados através de autodeclaração.
- Para dispositivos de Classe II, embora as declarações e os documentos técnicos sejam necessários, a AMAR pode acelerar o processo para catorze (14) dias para aqueles considerados de risco baixo-médio. Isto aplica-se se o fabricante possuir duas (02) autorizações de países reconhecidos e fornecer seis (06) meses de dados de mercado. Alternativamente, para dispositivos de Classe II com apenas a aprovação 510(k) da US FDA e seis (06) meses de dados do mercado dos US, o tempo de processamento da AMAR é acelerado para sessenta (60) dias.
Representante Autorizado Local Israelita
As empresas de dispositivos médicos sediadas fora de Israel devem designar um Titular de Registo Israelita (IRH) para facilitar o registo dos seus produtos para venda no país. O IRH atua como representante local do fabricante e é encarregado de fazer a ligação com o Ministério da Saúde para garantir a adesão aos regulamentos locais. Além disso, um IRH é responsável por estabelecer e manter uma presença comercial em Israel, bem como por obter e manter uma licença comercial válida.
Registo de Dispositivos Médicos
Para registar um dispositivo médico em Israel, os fabricantes devem obter aprovação prévia num dos mercados de referência, como os EUA, Europa, Austrália, Canadá ou outros mercados importantes. Os fabricantes com aprovações existentes num dos países de referência podem utilizar esta aprovação para o mercado israelita e nomear um representante no país. Posteriormente, precisam de submeter a documentação exigida, incluindo:
- FDA 510(k)/Carta de Aprovação Pré-Comercialização/CE.
- Certificado para Governo Estrangeiro (CFG)/Certificado de Livre Venda (CFS).
- ISO 13485 ou Outra Certificação Reconhecida de Boas Práticas de Fabrico (BPF).
- Validação e Certificação do Instituto de Normas de Israel (Se necessário).
Fluxo do Processo
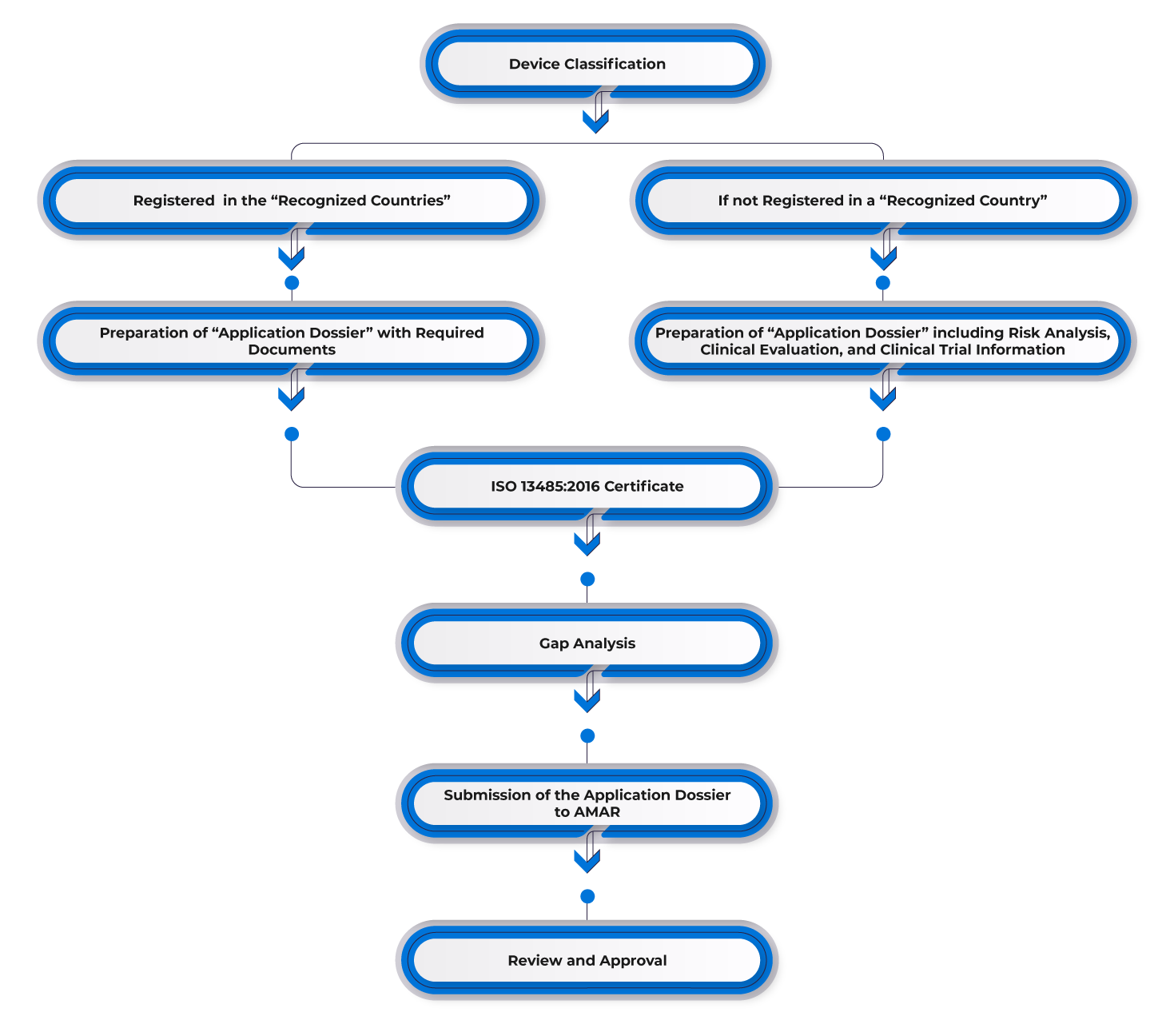
Gestão do Ciclo de Vida do Dispositivo Pós-aprovação
A Freyr oferece apoio abrangente a fabricantes estrangeiros na gestão de todo o ciclo de vida de dispositivos médicos em Israel, incluindo atividades pós-aprovação:
- Gestão de alterações pós-aprovação, abordando modificações às aprovações existentes de dispositivos médicos, como a adição de novas variantes, acessórios e indicações de utilização.
- Manutenção da ISO 13485:2016 e da certificação CE.
- Renovação de licenças.
- Atuar como intermediário entre o Organismo Notificado (ON) e o fabricante.
Navegar pelas complexidades dos organismos de autorização e cumprir múltiplos conjuntos de regulamentos para aprovações de dispositivos pode ser desafiador. Obter aprovações de vários países GHTF e aderir a regulamentos estaduais exige conhecimento aprofundado em Assuntos Regulamentares. Para os novos participantes no mercado que enfrentam estas complexidades sem um parceiro em Assuntos Regulamentares estabelecido, a Freyr oferece serviços End-to-End em Assuntos Regulamentares, simplificando o processo de aprovação para dispositivos médicos em Israel.
Registo de Dispositivos Médicos no Egito: Especialização
- Classificação de Dispositivos Médicos em Israel.
- Titular do Registo em Israel (IRH).
- Registo de Dispositivos em Israel.
- Consulta de Gestão de Risco ISO 14971:2019.
- Conformidade com a ISO 13485:2016.
- Revisão, Compilação e Submissão do Dossiê de Conceção.
- Registo de Dispositivos Médicos através do Sistema de Registo online.
- Relatório de Estratégia Regulamentar para Dispositivos Médicos.
- Apoio a Testes - Biocompatibilidade, Segurança Elétrica, Mecânica e Desempenho.
- Apoio à Conformidade da Rotulagem.
- Apoio a GMP.
- Apoio à Vigilância Pós-Comercialização (PMS).

