Visão Geral do Registo de Dispositivos Médicos na Nova Zelândia
Os dispositivos médicos na Nova Zelândia são regulados pela Autoridade de Segurança de Medicamentos e Dispositivos Médicos da Nova Zelândia (Medsafe), de acordo com os Regulamentos de Medicamentos de 1984, a Lei de Medicamentos de 1981 e os Regulamentos de Medicamentos (Base de Dados de Dispositivos Médicos) de 2003. Embora a aprovação pré-comercialização não seja necessária, é obrigatório listar os produtos na base de dados do sistema de Notificação Eletrónica Assistida por Web de Dispositivos (WAND) no prazo de 30 dias após o lançamento comercial. A Medsafe pode solicitar documentação que comprove a segurança e eficácia, como a certificação de organismos reconhecidos, como um Organismo Notificado da UE ou a Health Canada.
A equipa de especialistas em regulamentação de dispositivos médicos da Freyr traz uma experiência considerável em orientar empresas de dispositivos médicos através do processo de registo Medsafe para dispositivos médicos na Nova Zelândia.

Autoridade Regulamentar: Autoridade de Segurança de Dispositivos Médicos (Medsafe)
Regulamento:The Medicines (Database of Medical Devices) Regulations, 2003
Medicines Act 1981
Medicines Regulation 1984
Via Regulamentar: Sistema Eletrónico de Notificação de Dispositivos Assistido por Web (WAND)
Representante Autorizado: Patrocinador de Dispositivo Médico
Requisito de SGQ: Certificação ISO 13485:2016
Avaliação de Dados Técnicos: Autoridade de Segurança de Dispositivos Médicos (Medsafe)
Validade da Licença: Os registos de dispositivos na Nova Zelândia não expiram. Dispositivos considerados uma ameaça grave para o público podem ser retirados do mercado.
Requisitos de Rotulagem: Regulamento 12(4) dos Regulamentos de Medicamentos de 1984 e GHTF/SG1/N43:2005
Formato de Submissão: Sistema Eletrónico de Notificação de Dispositivos Assistido por Web (WAND)
Idioma: Inglês
Classificação de Dispositivos Médicos na Nova Zelândia
Na Nova Zelândia, os dispositivos médicos são classificados por risco nas Classes I, IIa, IIb, III e AIMD, de acordo com os critérios do Fórum Internacional de Reguladores de Dispositivos Médicos (IMDRF). Esta classificação afeta o nível de controlo regulamentar necessário. A classificação baseia-se em características como a finalidade prevista do dispositivo, a duração do contacto com o corpo, a invasividade e se é ativo ou inativo. Os dispositivos de classe superior estão sujeitos a uma supervisão regulamentar mais rigorosa. A Medsafe é a entidade reguladora na Nova Zelândia que supervisiona estas classificações e regulamentos.
| Classificação de Dispositivos Médicos da Medsafe, exceto IVD | Risco |
|---|---|
| Classe I Básica | Baixo Risco |
| Medição de Classe I | Baixo Risco |
| Classe I estéril | Baixo Risco |
| Classe IIa | Risco baixo a médio |
| Classe IIb | Risco médio-alto |
| Classe III e Dispositivo médico implantável ativo (AIMD) | Risco elevado |
| Classificação de IVD da Medsafe | Risco |
|---|---|
| A partir de julho de 2014, a Medsafe não reconhece qualquer sistema de classificação de risco para IVD. Todos os IVD notificados ao WAND devem utilizar o código de classificação de risco do IVD. O Diretor-Geral de Saúde autorizou a isenção para IVD de acordo com o Anexo 1, parágrafo (i) do Regulamento de Medicamentos (Base de Dados de Dispositivos Médicos) de 2003. Mas os fornecedores de IVD podem notificar voluntariamente os seus dispositivos à base de dados. | |
Representante Autorizado/Patrocinador de Dispositivos Médicos
O Representante Autorizado é designado como Sponsor e atua como intermediário entre o fabricante e a Medsafe. Os Sponsors atuam como representantes regulamentares para produtos comercializados na Nova Zelândia, submetendo submissões WAND e atuando como o principal ponto de contacto entre o fabricante e a Medsafe para todos os assuntos relacionados com o produto. Além disso, a Medsafe responsabiliza o Sponsor pelos esforços de vigilância.
Registo de Dispositivos Médicos da Nova Zelândia
O registo de dispositivos médicos, o procedimento na Nova Zelândia e o procedimento de registo WAND na Nova Zelândia variam consoante a classe do dispositivo.
Dispositivos de Classe I - É exigida uma declaração de conformidade do fabricante para equipamentos de Classe I não estéreis e não medidores; no entanto, raramente é apresentada a um organismo regulador. Em vez disso, o patrocinador (ou fornecedor) deve introduzir os detalhes do dispositivo na base de dados Web Assisted Notification of Devices (WAND) como parte do processo de notificação da Medsafe.
Dispositivos de Outras Classes
Na Nova Zelândia, os patrocinadores ou fornecedores são responsáveis por garantir que os dispositivos médicos cumprem normas como a ISO 13485:2016. A submissão direta de uma Declaração de Conformidade, certificação QMS ou prova de fabrico à Medsafe não é tipicamente exigida. No entanto, a retenção desta documentação é crucial para comprovar a conformidade mediante solicitação.
A Medsafe prioriza a vigilância pós-comercialização em detrimento de uma aprovação pré-comercialização detalhada para dispositivos médicos. Embora as auditorias não sejam realizadas rotineiramente durante a fase de notificação, a Medsafe pode iniciá-las para dispositivos de maior risco ou na sequência de atividades de vigilância e relatórios de eventos adversos, garantindo a segurança e conformidade contínuas.
Uma vez que um dispositivo é notificado através da base de dados WAND, pode ser comercializado na Nova Zelândia, desde que o fornecedor cumpra consistentemente os regulamentos da Medsafe. Isto exige conformidade contínua, particularmente com os padrões de monitorização pós-comercialização e notificação de incidentes. Os especialistas em dispositivos médicos da Freyr apoiam serviços relacionados com a navegação nestes requisitos regulamentares, garantindo que as empresas mantêm a conformidade ao longo de todo o ciclo de vida do produto.
Fluxo do processo
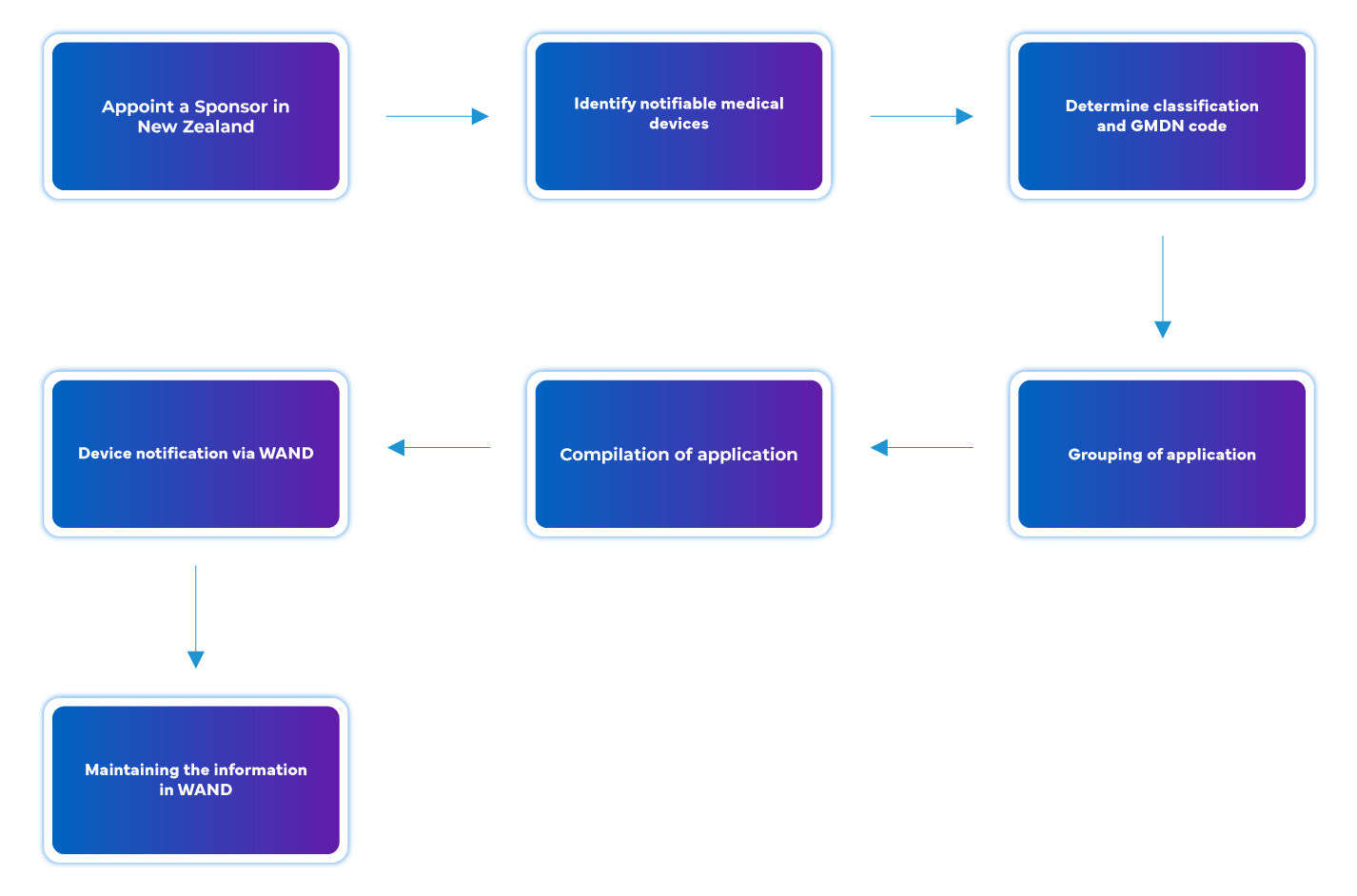
Gestão do Ciclo de Vida do Dispositivo Pós-Aprovação
A Freyr apoia fabricantes estrangeiros na gestão End-to-End do ciclo de vida de dispositivos médicos, incluindo atividades pós-aprovação, através da notificação às Autoridades da Nova Zelândia via WAND, tais como –
- Gestão de alterações pós-aprovação – modificações às aprovações existentes de Dispositivos Médicos, como a adição de novas variantes, acessórios; adição de novas indicações de utilização, entre outras.
- Manutenção das aprovações e registos.
Com uma equipa de profissionais de regulamentação, a Freyr oferece um apoio abrangente aos fabricantes para manter os padrões de qualidade e segurança exigidos para a aprovação no mercado. Os especialistas em inteligência regulamentar da empresa monitorizam meticulosamente as atualizações nos regulamentos, garantindo que os clientes estejam bem informados sobre as ações necessárias para manter a conformidade dos seus produtos com os padrões atuais.
Resumo
| Risco | Classe de Dispositivo | Auditoria QMS | Via Regulamentar | Prazos da Medsafe | Validade do Registo (anos) |
|---|---|---|---|---|---|
| Baixo Risco | Classe I Básica | Conformidade ISO 13485:2016 Nota: A Medsafe não exige auditorias QMS, mas recomenda vivamente seguir a ISO 13485:2016 para qualidade e segurança. A Medsafe tem autoridade para realizar auditorias QMS para qualquer classe de dispositivo se surgirem preocupações de segurança ou qualidade. | Listagem WAND (Notificação) | 1 semana |
Sem datas de validade |
| Baixo Risco | Classe I com função de medição | Listagem WAND (Notificação) | |||
| Baixo Risco | Classe I estéril | Listagem WAND (Notificação) | |||
| Risco baixo a médio | Classe IIa | Listagem WAND (Notificação) | |||
| Risco médio-alto | Classe IIb | Listagem WAND (Notificação) | |||
| Risco elevado | Classe III | Listagem WAND (Notificação) |
Nota: De acordo com a legislação atual, os registos de dispositivos na Nova Zelândia não expiram, mas os dispositivos considerados como apresentando um risco inaceitável para o público podem ser retirados do mercado. No entanto, a legislação atual poderá ser revista até 2026/2027.
Experiência Freyr
- Apoio completo ao registo de dispositivos médicos.
- Apoio LR
- Listagem WAND
- Apoio à Rotulagem
- Gestão de Alterações Pós-Aprovação
- Transferência de Licença
- Serviços de submissão e ligação com a WAND

