
Visão Geral do Registo de Dispositivos Médicos no Vietname
O mercado de Dispositivos Médicos do Vietname está a crescer e é atualmente um dos setores em expansão no país. Os Dispositivos Médicos no país são regulados pelo Department of Medical Equipment and Health Works (DMEHW), sob a alçada do Ministério da Saúde. Os fabricantes estrangeiros devem nomear um Representante Local Autorizado no Vietname para os auxiliar no processo de registo de dispositivos médicos no Vietname.
Autoridade Regulamentar: Department of Medical Equipment and Health Works (DMEHW)
Regulamento: Decreto n.º 98/2021/ ND-CP
Representante Autorizado: Representante Local Autorizado no Vietname
Requisito de SGQ: ISO 13485:2016
Avaliação de Dados Técnicos: Department of Medical Equipment and Construction (DMEC) of MoH
Requisitos de Rotulagem: Decreto n.º 111/2021
Formato de Submissão: Online- Prazos: 15 - 60 dias
Idioma: Inglês e Vietnamita
Classificação de Dispositivos Médicos no Vietname
Os dispositivos são classificados em 4 classes (A, B, C e D), que também são categorizadas em dois grupos: o grupo 1 (Classe A) e o grupo 2 (Classes B, C e D). A classificação formal está disponível junto do Departamento de Equipamentos Médicos e Obras de Saúde do Vietname (DMEHW).
| Grupo | Classe | Risco |
|---|---|---|
Grupo 1 | Classe A | Nível de risco baixo |
Grupo 2 | Classe B | Nível de risco médio-baixo |
Classe C | Nível de risco médio-alto | |
Classe D | Nível de risco elevado |
Representante Local Autorizado no Vietname
A nomeação de um agente vietnamita fiável e capaz para fabricantes estrangeiros é crucial, uma vez que este deve assumir os serviços de garantia oferecidos pelo fabricante como parte da venda do dispositivo. A tradução para vietnamita é obrigatória para entrar na região, o que, na prática, pode ser um desafio.
A Freyr oferece suporte regulamentar abrangendo toda a gama de atividades, como a obtenção do Número de Reconhecimento de Livre Venda envolvido na aprovação de Dispositivos Médicos pelas autoridades. Também fornecemos suporte linguístico especializado para manter intacta a perspetiva regulamentar da tradução. Atendemos às necessidades pós-aprovação dos clientes para manter a conformidade ao longo do ciclo de vida do produto no Vietname.
Registo de Dispositivos Médicos no Vietname
Todos os produtos das Classes A e B irão necessitar de uma Licença de Autorização de Colocação no Mercado (MA). Os dispositivos das Classes A e B serão sujeitos a uma rápida revisão administrativa pelo Departamento de Saúde da província onde o Titular do Registo está localizado.
Os dispositivos das Classes C e D irão agora necessitar de solicitar uma licença de Autorização de Colocação no Mercado (MA). As licenças MA manter-se-ão válidas por tempo indeterminado.
Fluxo do processo
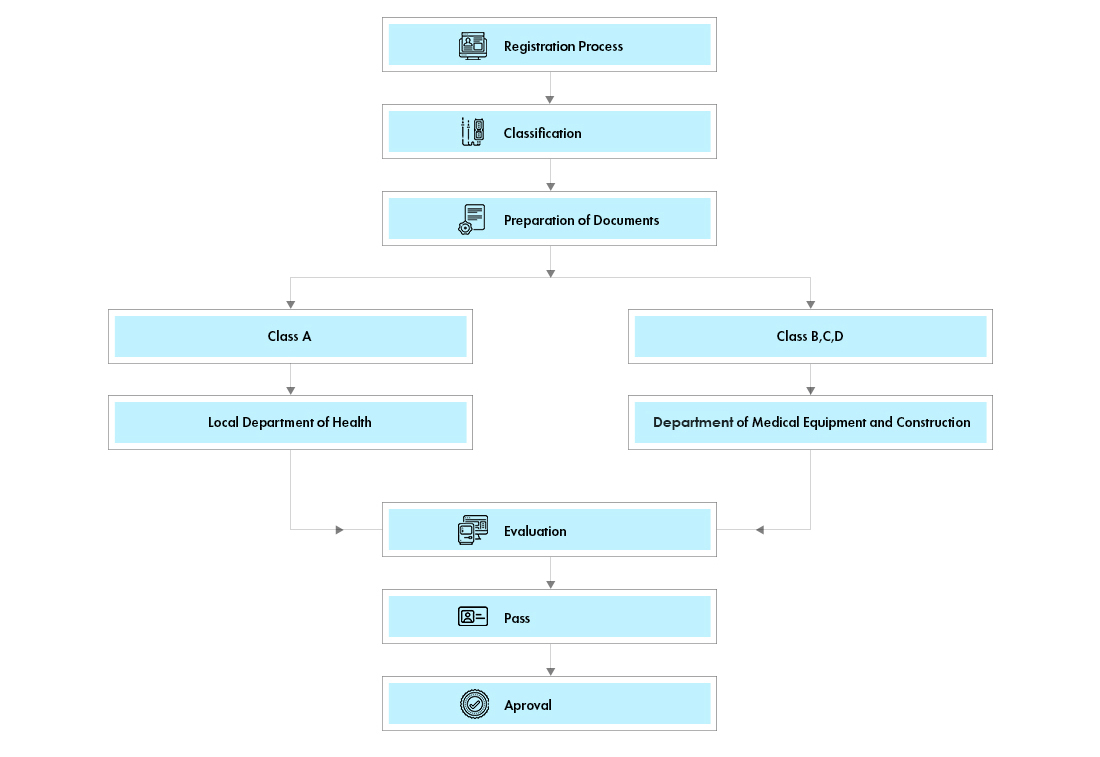
Gestão do Ciclo de Vida do Dispositivo Pós-Aprovação
A Freyr apoia os fabricantes estrangeiros na gestão End-to-End do ciclo de vida de dispositivos médicos, incluindo atividades pós-aprovação, tais como:
- Gestão de alterações pós-aprovação - modificações às aprovações existentes de Dispositivos Médicos, tais como, adição de novas variantes, acessórios; adição de novas indicações de utilização, entre outras
- Manutenção das aprovações e do registo através do pagamento atempado das taxas administrativas e de registo
- Renovação de licenças
- Coordenação entre o DMEHW e o fabricante
- Gestão de importação
Resumo
Grupo | Classe | Risco | Via Regulamentar | Prazos | Validade |
|---|---|---|---|---|---|
Grupo 1 | Classe A | Nível de risco baixo | Declaração de norma aplicável | 15 - 60 dias | Ilimitada |
Grupo 2 | Classe B | Nível de risco médio-baixo | Certificado de registo de livre venda | 15 - 60 dias | 5 Anos |
Classe C | Nível de risco médio-alto | Certificado de registo de livre venda | 15 - 60 dias | 5 Anos | |
Classe D | Nível de risco elevado | Certificado de registo de livre venda | 15 - 60 dias | 5 Anos |
Experiência Freyr
- Due Diligence Regulamentar
- Classificação Oficial
- Registo de Dispositivos
- Licença de Importação
- Apoio à Rotulagem
- Apoio à Tradução
- Identificação e qualificação de distribuidores
- Vigilância Pós-Comercialização
- Gestão de Alterações Pós-Aprovação
- Renovação e transferência de licenças
- Submissão e coordenação
- Desalfandegamento


