Die Konformitätsbewertungsstelle (CAB) führt die Konformitätsbewertung verschiedener Akteure im Lieferkettensystem für Medizinprodukte durch. Die Konformitätsbewertungsstelle (CAB), Malaysia, führt umfassende Audits durch und bewertet alle anwendbaren Elemente, die von der Medical Device Authority (MDA), Malaysia, festgelegt wurden, und überprüft die Produktkonformität mit den relevanten Standards.
Dieser Teil der Blogreihe erläutert Ihnen die Rolle der CABs bei der Registrierung und Zulassung von Medizinprodukten in Malaysia. Sie erhalten auch Einblicke in die Anforderungen der MDA an die CAB-Zertifizierung, die im ersten Teil behandelt wurden.
Die Konformitätsbewertung ist eine systematische und fortlaufende Prüfung von Nachweisen und Verfahren, um die Sicherheit, Leistung, den Nutzen und das Risiko von Medizinprodukten zu gewährleisten. Sie stellt auch die Einhaltung der wesentlichen Grundsätze für Sicherheit und Leistung (EPSP) sowie der Anforderungen des Medizinproduktegesetzes 2012 (Act 737) durch die Herstellung sicher. Die Klassifizierung eines Medizinprodukts bestimmt die durchzuführenden Konformitätsbewertungsverfahren. Die Konformitätsbewertung wird strenger, je höher das Risiko des Medizinprodukts ist; daher ist die Risikobewertung von Medizinprodukten erforderlich.
Die CABs führen verschiedene Arten von Bewertungen durch, abhängig von den Geschäftstätigkeiten der Organisation und dem jeweiligen Anwendungsbereich. Dazu gehören:
- Bewertung der technischen Dokumentation
- Bewertung von QMS-Systemen für die Einhaltung der ISO 13485
- Zertifizierung nach den Guten Vertriebspraktiken für Medizinprodukte (GDPMD)
- Vollständige Konformitätsbewertung für die Registrierung von Medizinprodukten
- Vereinfachte Verifizierung für die Registrierung von Medizinprodukten
Die CABs spielen eine entscheidende Rolle für jeden Akteur im Lieferkettensystem, einschließlich Hersteller von Medizinprodukten, Importeure, Händler, Bevollmächtigte (AR) und andere.
Importeure, Händler und Bevollmächtigte müssen ihre Betriebsstätten bei der MDA registrieren lassen, um ihre Tätigkeiten ausüben zu können. Die GDPMD-Zertifizierung ist eine wesentliche Voraussetzung, die zusammen mit dem Antrag auf Betriebserlaubnis einzureichen ist. Die CABs führen die Konformitätsbewertung der Qualitätssysteme dieser Unternehmen durch, um die Einhaltung der von der MDA festgelegten GDPMD-Vorschriften zu überprüfen, bevor sie das Zertifikat ausstellen. Diese Bewertung umfasst die Überprüfung der technischen Dokumentation sowie die Vor-Ort-Prüfung der Einrichtungen.
Die Hersteller von Medizinprodukten sind ebenfalls auf die CABs angewiesen, um ihre Produkte bei der MDA, Malaysia, registrieren zu lassen. Die inländischen Hersteller müssen ihre Produktionsstätten bei der MDA registrieren lassen, wobei die CAB involviert ist.
Zusätzlich zur Registrierung der Betriebsstätte spielen die CABs auch eine Rolle bei der Registrierung von Medizinprodukten bei der MDA. Medizinprodukte mit Zulassungen aus Referenzländern unterliegen der Überprüfung durch die CAB, während Produkte ohne Zulassungen aus Referenzländern einer vollständigen Bewertung durch die CAB unterzogen werden müssen.
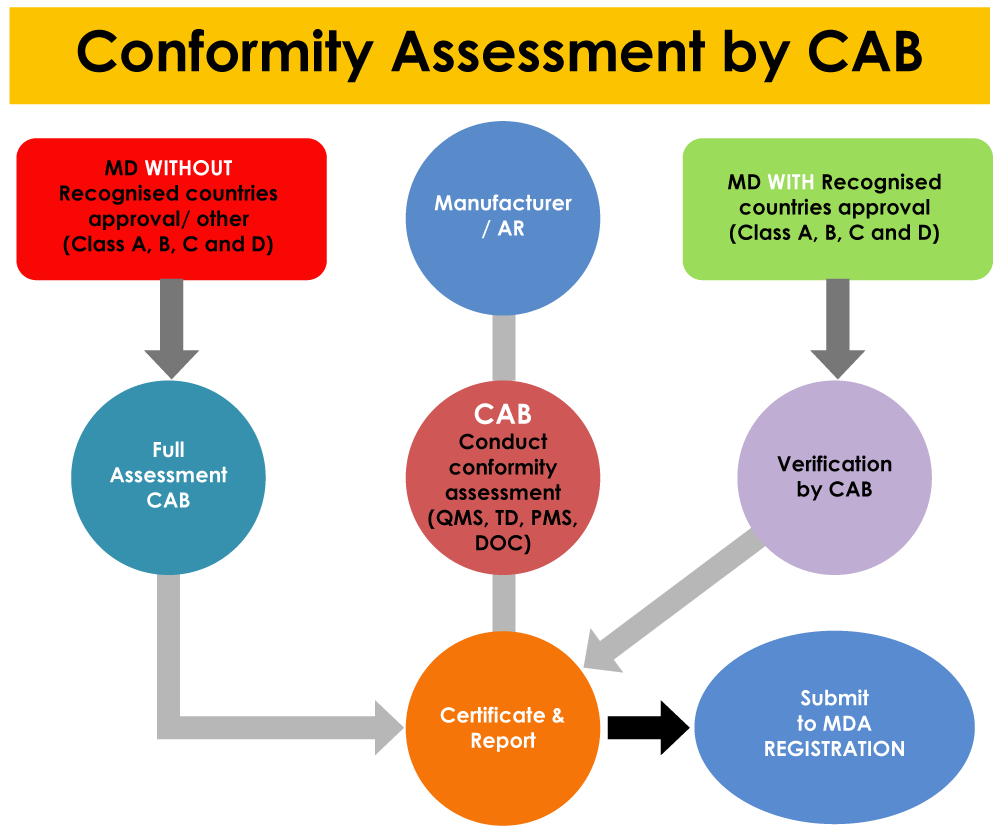
Werden Nichtkonformitäten im QMS, PMS-System und im vollständigen Produktdossier (einschließlich jedes einzelnen Prüfberichts) festgestellt, besteht eine hohe Wahrscheinlichkeit, dass der Antrag von der CAB abgelehnt wird.
Lesen Sie Teil 1 des Artikels, um die Anforderungen und Genehmigungsverfahren der MDA für die CAB-Zertifizierung kennenzulernen.
Möchten Sie Ihr Medizinprodukt oder IVD auf dem malaysischen Markt einführen? Möchten Sie weitere Einblicke in die Rollen und Verantwortlichkeiten der CABs bei der Produktregistrierung erhalten? Kontaktieren Sie einen Regulierungsexperten. Bleiben Sie informiert. Bleiben Sie konform.









