Die Anwendung von Softwaretechnologien in verschiedenen Bereichen des Gesundheitswesens, einschließlich der Diagnose oder Behandlung von Krankheiten, nimmt in einem noch nie dagewesenen Tempo zu. Die globalen Behörden für Medizinprodukte überarbeiten ihre Vorschriften und Leitlinien, um diesen boomenden Gerätetechnologien Rechnung zu tragen. In Australien ist die Therapeutic Goods Administration (TGA) die Regulierungsbehörde, die für die Überwachung von Medizinprodukten, einschließlich Software und mobilen Anwendungen, zuständig ist. Im Januar 2021 veröffentlichte die TGA den ursprünglichen Entwurf der Vorschriften für Medizinproduktesoftware, der im Februar 2021 überarbeitet wurde. Am 27. Juli 2021 veröffentlichte die TGA ein detailliertes Flussdiagramm, das die häufigsten Unklarheiten anspricht, die Gerätehersteller und Regulierungsexperten im Zusammenhang mit der Klassifizierung von Medizinproduktesoftware haben könnten.
Die TGA klassifiziert Software im Bereich der Medizinprodukte als Software als Medizinprodukt (SaMD), als in ein Medizinprodukt eingebettete Software (SiMD) und als Software, die Medizinprodukte steuert. Laut TGA ist der Begriff Software als Medizinprodukt (oder SaMD) jede Software, die auf einem Laptop, Smartphone oder Tablet funktionieren kann und deren bestimmungsgemäßer Zweck unter die Normen eines Medizinprodukts fällt. Im Gegensatz dazu ist SiMD eine Software, die ein integraler Bestandteil eines Geräts ist und im Allgemeinen für die präzise Funktion des Geräts wichtig ist. Einige Software steuert die Medizinprodukte entweder physisch oder über drahtlose Verbindungen wie Bluetooth, Wi-Fi usw. Die TGA reguliert alle drei (03) Arten von Software.
Einige Medizinproduktesoftware ist von der TGA-Regulierung für Software als Medizinprodukt ausgeschlossen oder ausgenommen. Dies basiert auf den Prinzipien der Angleichung der Regulierung an internationale Vorschriften und der Verringerung des Aufwands durch die Nichtregulierung von Produkten, bei denen kein großes Sicherheitsrisiko besteht und geeignete Strukturen oder Rahmenbedingungen für die Produkt- oder Systemkontrollen bereits vorhanden sind.
| Ausgenommene Software-Geräte | Ausgeschlossene Software-Geräte |
|---|---|
Z.B.: Einige klinische Entscheidungsunterstützungssysteme , die drei Hauptkriterien erfüllen: 1. Wenn die Software nicht dazu bestimmt ist, ein medizinisches Bild zu analysieren oder zu verarbeiten. 2. Die Software ist nur dazu bestimmt, dem medizinischen Fachpersonal Unterstützung/Empfehlungen zu geben. 3. Die Software ist nicht dazu bestimmt, das klinische Urteilsvermögen des Fachpersonals zu ersetzen. | Produkte, die nicht in die Kategorie der Medizinprodukte fallen und keinen TGA-Regulierungsanforderungen unterliegen, werden als ausgeschlossene Software-Geräte bezeichnet. Z.B.:
|
Die TGA hat die Regulierung von Medizinprodukten überarbeitet, die Software umfassen, die andere Medizinprodukte extern oder intern steuert oder mit ihnen interagiert, sowie Software, die (eigenständig) als Medizinprodukt fungiert. Die wesentlichen Änderungen umfassen die Einführung neuer Klassifizierungsregeln, die Klärung der Abgrenzung regulierter Softwareprodukte; die grundlegenden Prinzipien wurden aktualisiert, um die Anforderungen an softwarebasierte Medizinprodukte zu präzisieren.
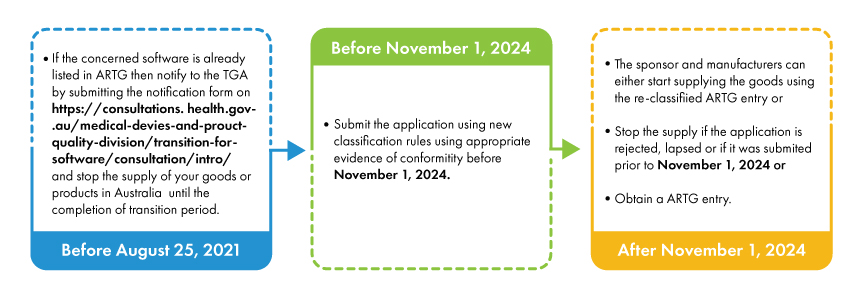
Mit der Einführung neuer Klassifizierungsregeln werden einige softwarebasierte Medizinprodukte in höhere Risikoklassen eingestuft und müssen entsprechende Konformitätsbewertungsverfahren durchlaufen. Die Sponsoren und Hersteller solcher höher klassifizierten Produkte müssen vor dem 25. Februar 2021 im ARTG (Australian Register of Therapeutic Goods) gelistet sein. Hersteller und Sponsoren, die sich bereits vor dem 25. Februar 2021 bei der TGA beworben haben, müssen ein Benachrichtigungsformular bei der TGA einreichen.
Klassifizierung von Medizinproduktesoftware in Australien:
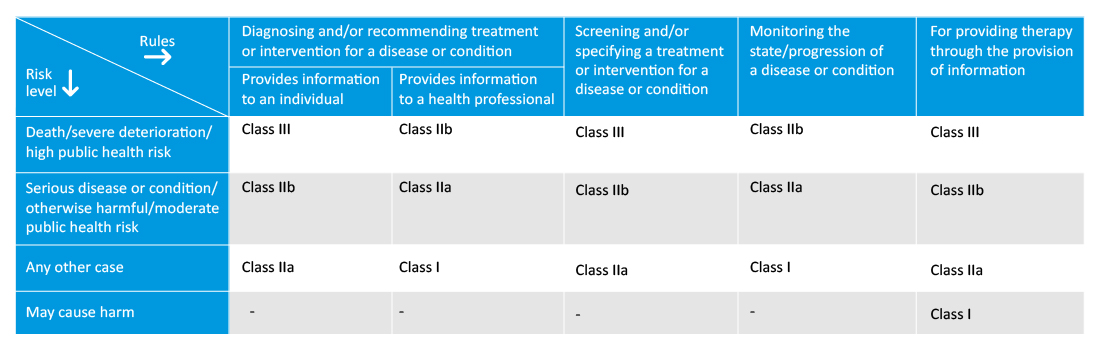
Hersteller müssen den bestimmungsgemäßen Zweck der SaMD angeben, was bei der weiteren Klassifizierung und den Konformitätsbewertungsverfahren helfen wird. Die neue Regulierung führt auch neue Klassifizierungsregeln für programmierte und programmierbare Medizinprodukte oder Software-Medizinprodukte ein, wobei die Klasse der Software von der Schwere der überwachten/behandelten Krankheit abhängt.
![]()
Änderungen der grundlegenden Prinzipien:
Nachfolgend sind die Änderungen der grundlegenden Prinzipien aufgeführt, die ab dem 25. Februar 2021 für das softwarebasierte Medizinprodukt.
Die von der TGA vorgenommenen Änderungen in den Softwarevorschriften können die Hersteller entlasten, indem sie die Einstufung ihrer Software als reguliert oder nicht reguliert erleichtern und bei der fristgerechten Erstellung der für die TGA-Konformitätsbewertung erforderlichen Dokumente unterstützen.
Nachdem alle Szenarien entschlüsselt wurden, möchten Sie Ihre Software mit weniger Aufwand im Australian Register of Therapeutic Goods (ARTG) listen lassen? Für die ARTG-Listung von Medizinprodukten, IVDs oder SaMDs wenden Sie sich an einen Experten. Bleiben Sie informiert. Bleiben Sie konform.