Ein „Referenzprodukt“ ist ein Medizinprodukt, das zuvor von der US Food and Drug Administration (US FDA) zugelassen wurde und bereits auf dem Markt ist. Es dient als Referenzpunkt für neue Medizinprodukte, die eine Zulassung über den 510(k)-Zulassungsweg der FDA anstreben.
Das betreffende Produkt muss nachweislich mindestens so sicher und wirksam sein wie das Referenzprodukt, sowohl hinsichtlich seiner Zweckbestimmung als auch seiner technologischen Eigenschaften. Dieser Vergleich wird als “Bestimmung der wesentlichen Gleichwertigkeit” bezeichnet.
Ein neues Produkt muss nicht identisch mit dem Referenzprodukt sein, damit es als wesentlich gleichwertig mit diesem gilt.
Wie Sie ein Referenzprodukt identifizieren?
Die Datenbank der FDA bietet für jede Geräteklassifizierung einen dreistelligen Produktcode. Die FDA 510(k)-Datenbank enthält Informationen zu allen Geräten, die über den 510(k)-Prozess zugelassen wurden. Sobald Sie den dreistelligen Produktcode besitzen, erhalten Sie eine Liste aller Produkte, Unternehmen und Handelsnamen von Wettbewerbern oder potenziellen Wettbewerbern, die Sie überprüfen möchten. Anschließend können Sie eine detaillierte Analyse und einen Vergleich durchführen, um ein Vergleichsprodukt (Predicate Device) einzugrenzen.
Unten sehen Sie ein Flussdiagramm, das den Prozess der Identifizierung und Eingrenzung eines Vergleichsprodukts (Predicate Device) darstellt.
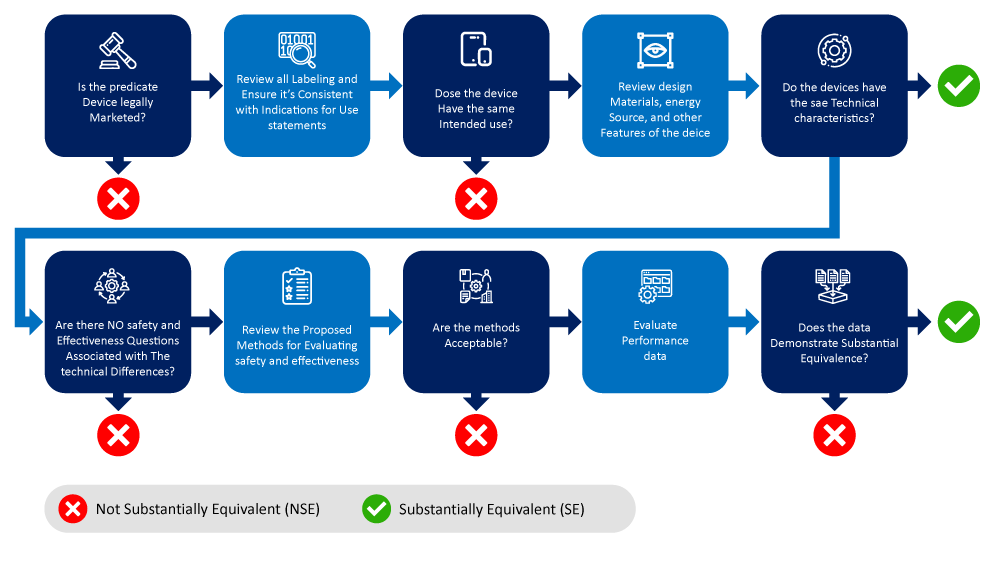
Faktoren, die bei der Bestimmung des Referenzprodukts zu berücksichtigen sind
- Zweckbestimmung: Die Zweckbestimmung des Referenzprodukts sollte der des neuen Produkts ähneln. Wenn das neue Produkt beispielsweise zur Herzüberwachung eingesetzt werden soll, sollte auch das Referenzprodukt ein Herzüberwachungsgerät sein.
- Technologische Eigenschaften: Das Referenzprodukt sollte hinsichtlich der technologischen Eigenschaften mit dem neuen Produkt identisch sein. Beispielsweise sollten Design, verwendete Materialien und die Funktionsweise ähnlich sein.
- Biokompatibilität: Biokompatibilitätsbewertungen eines Medizinprodukts oder einer Komponente sollten sich nicht nur auf die im Produkt und bei der Herstellung verwendeten Rohmaterialien beschränken, sondern auch zusätzliche Chemikalien berücksichtigen. Dieser Faktor gilt jedoch nicht für IVDs.
- Neueste Technologie: Das Referenzprodukt sollte nicht veraltet sein und die neueste Medizintechnik repräsentieren.
Das Referenzprodukt ist ein Schlüsselfaktor bei der Entscheidung, ob ein neues Medizinprodukt über den 510(k)-Weg auf den Markt gebracht werden kann. Die Wahl des falschen Referenzprodukts könnte zu einem teureren und zeitaufwändigeren Zulassungsprozess führen, während die Wahl des richtigen Referenzprodukts dazu beitragen kann, die Kosten und den Zeitaufwand für die Markteinführung eines neuen Medizinprodukts zu reduzieren. Ist das Referenzprodukt nicht geeignet, kann dies zu Verzögerungen und zusätzlichen Kosten führen.
Für Unterstützung beim 510(k)-Einreichungsprozess Ihres Medizinprodukts, vereinbaren Sie einen Anruf mit den Regulierungsexperten von Freyr, die Ihnen helfen können, die Verfahren zu meistern. Bleiben Sie informiert. Bleiben Sie konform.









