
510(k) ist eine prämarket-Einreichung bei der FDA, um zu zeigen, dass das zu vermarktende Produkt ebenso sicher und wirksam ist, das heißt, im Wesentlichen gleichwertig mit einem bereits legal vermarkteten Produkt (Prädikatprodukt). Für Produkte mit moderatem Risiko ist eine 510(k)-Meldung erforderlich, die eine Minderheit von Produkten der Klasse I und III sowie eine Mehrheit von Produkten der Klasse II umfasst.
Es gibt drei (03) Arten von 510(k)-Programmen: Traditionell, Abgekürzt und Spezial. Der Sicherheits- und Leistungspfad wurde 2019 eingeführt und baut auf dem abgekürzten Programm auf. Das 2020 eingeführte eSTAR-Programm ermöglicht eine umfassende Einreichung von Medizinprodukten über ein interaktives PDF-Formular.
Wer benötigt eine 510(k)-Zertifizierung?
510(k) ist im Wesentlichen die Bezeichnung für das Verfahren/den Weg, den Hersteller von Medizinprodukten, die ihre Produkte mit mittlerem bis hohem Risiko in den US vermarkten möchten, durchlaufen, um nachzuweisen, dass das zu vermarktende Produkt genauso sicher und wirksam ist wie ein rechtmäßig vermarktetes Produkt.
Nachfolgend wird der Schritt-für-Schritt-Prozess zur Erlangung einer 510(k)-Zulassung detailliert beschrieben.
Schritt 1 – Identifizierung des Produktklassencodes, des Einreichungstyps und des Prädikatprodukts
- Produktcode und Verordnungsnummer identifizieren Um die 510(k)-Prüfanforderungen zu bestimmen, ist es zunächst notwendig, den Produktcode und die Verordnungsnummer zu identifizieren. Man kann eine Suche in der FDA-Datenbank starten, um die 7-stellige Verordnungsnummer zu finden, deren Identifikation der beabsichtigten Verwendung des betreffenden Produkts entspricht.
- Der FDA-Produktcode besteht aus drei (03) Buchstaben. Informationen zur Produktklassifizierung, Verordnungsbeschreibung und GMP-Anforderungen können mit diesem Code gefunden werden.
- Auswahl des Einreichungstyps Ein Antragsteller kann einen der drei (03) zuvor genannten Einreichungstypen wählen. Traditional 510(k) ist für Ersteinreichungen, Special 510(k) ist für Medizinproduktehersteller, die Änderungen an einem bestehenden Produkt einreichen möchten, und Abbreviated 510(k) kann gewählt werden, wenn das Produkt etablierten freiwilligen Konsensstandards entspricht. Im Falle eines Abbreviated 510(k) muss sich der Antragsteller auf FDA-Leitfäden verlassen.
- Identifizierung des Prädikatprodukts – Ein Medizinproduktehersteller muss nachweisen, dass das Produkt, das er auf den Markt bringen möchte, denselben Verwendungszweck und dieselben technischen Eigenschaften aufweist wie das bereits rechtmäßig vermarktete Produkt, auch bekannt als Prädikatprodukt. Gibt es Unterschiede in den technischen Eigenschaften, muss der Antragsteller nachweisen, dass mit diesen Unterschieden keine Bedenken hinsichtlich Sicherheit und Wirksamkeit verbunden sind.
Schritt 2 – Vorbereitung der 510(k)-Akte
Der nächste Schritt ist die Vorbereitung der 510(k)-Antragsunterlagen, der Leitfäden und der Informationen, die auf der FDA-Website verfügbar sind. Dies umfasst die Checkliste für die Annahme für alle drei (03) Arten von 510(k)-Programmen sowie eine Microsite mit dem Titel Inhalte für 510(k), die unter anderem Informationen zu den Angaben für die Verwendungszwecke, den Vergleich der wesentlichen Gleichwertigkeit und die vorgeschlagene Kennzeichnung enthält.
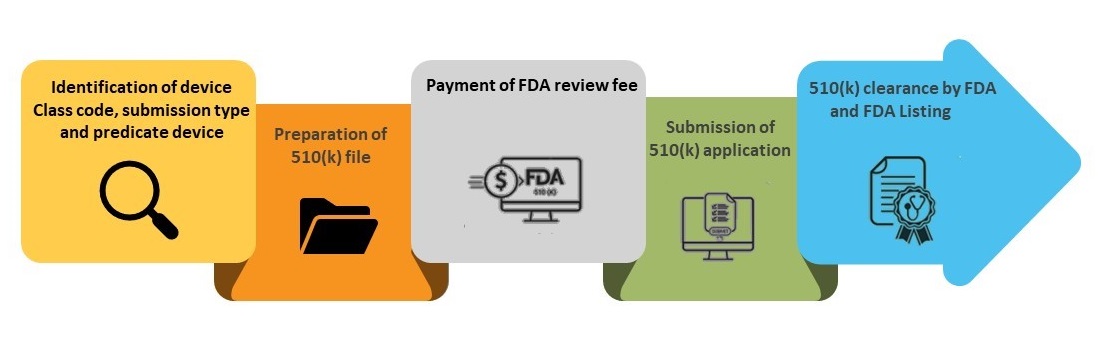
Schritte des 510(k)-Einreichungsprozesses
Schritt 3 – Zahlung der FDA-Prüfgebühr
Alle Arten von 510(k)-Anträgen unterliegen einer Benutzergebühr. Für das Geschäftsjahr 2023 beträgt die Standardgebühr für 510(k) 19.870 $. Für Unternehmen, die unter dem Centre for Diagnostics and Radiological Health (CDRH) zertifiziert sind, auch bekannt als Kleinunternehmen, beträgt die Gebühr 4.967 $. Die Gebühr kann sich im nächsten Geschäftsjahr ändern.
Schritt 4 – Einreichung des 510(k)-Antrags
Der Antragsteller kann eine elektronische Kopie (eCopy) oder eine elektronische Einreichungsvorlage und Ressource (eSTAR) als Premarket-Einreichung über das CDRH-Portal senden.
Ab dem 1. Oktober 2023 müssen alle 510(k)-Einreichungen, sofern nicht gemäß der endgültigen Leitlinie ausgenommen, als elektronische Einreichungen unter Verwendung von eSTAR erfolgen.
Nach Einreichung des 510(k)-Antrags wird eine eindeutige Kontrollnummer zugewiesen, die als „510(k)-Nummer“ oder „K-Nummer“ bekannt ist. Die FDA führt zwei Überprüfungen durch: eine, um zu überprüfen, ob die korrekte Benutzergebühr entrichtet wurde, und die zweite, um zu überprüfen, ob eine gültige eCopy oder eSTAR bereitgestellt wurde.
- Bis zum Tag 07 sendet die FDA ein Bestätigungsschreiben, falls die korrekte Benutzergebühr entrichtet und eine gültige eCopy oder eSTAR bereitgestellt wurde. Andernfalls sendet die FDA ein Schreiben zur Aussetzung des Verfahrens bei ungelösten Problemen.
- Bis zum Tag 15 führt die FDA eine Annahmeprüfung durch. Die FDA informiert den Antragsteller, ob der 510(k)-Antrag für eine inhaltliche Prüfung angenommen oder auf „Refuse to Accept (RTA)“-Status gesetzt wird.
- Bis zum Tag 60 führt die FDA eine inhaltliche Prüfung durch. Die FDA kommuniziert über eine
inhaltliche Interaktion, um mitzuteilen, dass die FDA entweder eine interaktive Prüfung fortsetzen wird oder der 510(k)-Antrag ausgesetzt und zusätzliche Informationen angefordert werden.
Schritt 5 – FDA-Freigabe und Listung in der FDA 510(k)-Datenbank
Ziel der FDA ist es, ihre Entscheidung zu den Medical Device User Fee Amendments (MDUFA) innerhalb von 90 FDA-Tagen bekannt zu geben. FDA-Tage sind die Kalendertage zwischen dem Datum des Eingangs des 510(k)-Antrags und dem Datum einer MDUFA-Entscheidung, ausgenommen die Tage, an denen der Antrag aufgrund einer Anforderung zusätzlicher Informationen ausgesetzt war. MDUFA-Entscheidungen für 510(k)-Anträge umfassen Feststellungen der wesentlichen Gleichwertigkeit (SE) oder der nicht wesentlichen Gleichwertigkeit (NSE).
Wenn eine Entscheidung getroffen wird, sendet die FDA dem Antragsteller eine Entscheidungsmitteilung per E-Mail. Ein 510(k)-Antrag, der ein SE-Entscheidungsschreiben erhält, gilt als “freigegeben”. Er wird dann zusammen mit den Indikationen für die Verwendung des Medizinprodukts und der 510(k)-Zusammenfassung oder 510(k)-Erklärung als Anhänge in der 510(k)-Datenbank aufgeführt.
Es lässt sich folgern, dass eine sorgfältige Planung und Ausführung durch eine gründliche Dokumentation und ein tiefgreifendes Verständnis des regulatorischen Umfelds entscheidend für eine erfolgreiche 510(k)-Einreichung bei der FDA sind.
Für Unterstützung beim 510(k)-Einreichungsprozess Ihres Medizinprodukts können Sie uns unter sales@freyrsoltions.com schreiben oder einen Anruf mit unseren Experten vereinbaren, die Ihnen helfen können, die Verfahren zu meistern. Bleiben Sie informiert. Bleiben Sie konform.









