
Eine effektive Kommunikation hat schon immer die Sicherheit und Qualität der Patientenversorgung gewährleistet. Im Laufe der Jahre besteht weiterhin ein unerfüllter Bedarf an der Bereitstellung von Kennzeichnungsübersetzungen für Personen, die nicht fließend Englisch sprechen. Die Nachfrage nach Produktkennzeichnungen in mehreren regionalen Sprachen ist exponentiell gestiegen, da Pharmahersteller den Wandel hin zu Lokalisierung und besserer Kommunikation vorantreiben wollen.
Die Erfüllung dieser Anforderungen wird die Patientensicherheit erhöhen und gleichzeitig die Einhaltung länderspezifischer regulatorischer Anforderungen ermöglichen. Das Fehlen wichtiger medizinischer Informationen in regionalen Sprachen stellt eine zusätzliche Belastung für Apotheker und medizinisches Fachpersonal dar, die Sprachbarriere zu überwinden.
Die Health Products Regulatory Authority (HPRA) überwacht die Einhaltung der Vorschriften in Irland. Die HPRA unterstützt und arbeitet gemeinsam mit den Interessengruppen, indem sie die Leitlinien für bewährte Verfahren zur mehrsprachigen Kennzeichnung einhält, die von der Koordinierungsgruppe für gegenseitige Anerkennung und dezentrale Verfahren – Human (CMDh) herausgegeben wurden. Darüber hinaus hat die HPRA auch bestimmte Kennzeichnungsbedingungen gelockert, darunter:
- Verwendung von mL in Irland (IE) im Vergleich zu ml in anderen EU-Staaten.
- Verwendung von Dezimalpunkten im Produktvolumen oder in der Stärke und eines Punkts in IE im Gegensatz zu einem Komma in der EU. Arzneimittelhersteller können diese Diskrepanz überwinden, indem sie den erfundenen Namen, die Stärke und die Darreichungsform in jeder Sprache als eine Einheit gruppieren.
- Verwendung eines Trennzeichens in der Produktstärke oder im Volumen – ein Punkt in der EU im Gegensatz zu einem Komma in IE. Die Verwendung von Kommas als Trennzeichen ist auf der unmittelbaren Umverpackung erlaubt, um jegliches Verwechslungsrisiko in der irischen Patientenpopulation zu vermeiden.
- Kleine Primärverpackungseinheiten, d.h. Behälter mit einer Größe von weniger oder gleich 50 ml, haben eine Platzbeschränkung und können, wo gerechtfertigt, die mindestens erforderlichen Informationen für mehr als zwei (02) Sprachen aufnehmen.
- Informationen aus Drittländern – wo immer die Bedingungen der Produktinformationen im Vereinigten Königreich und in IE ähnlich sind, sind Mehrländerpackungen akzeptabel. Zusätzliche länderspezifische Anforderungen werden in einer „blauen Box“ platziert.
- Koordinierung der Bewertung mit den anderen Member States – Mock-up-Bewertungen, die von den Member States durchgeführt werden, gewährleisten die Einhaltung der Kennzeichnungsvorschriften. Antragsteller können sich mit den Member States abstimmen, um Klarheit über die erforderlichen Änderungen vor den Einreichungen bei der HPRA zu erhalten.
- Gemeinsame Namen – Die Hervorhebung des erfundenen Namens gegenüber den Member States muss der HPRA mitgeteilt werden.
HPRA unterbreitet zusätzliche Vorschläge für mehrsprachige Kennzeichnung wie folgt:
- Informationen, die auf Englisch angegeben sind, müssen in einem Block zusammengefasst werden.
- Nennen Sie die „Blue-Box“-Anforderungen für alle Länder auf demselben Feld, wo immer mehrere Länder eine Packung teilen.
- Informationen, die sich an irische Patienten richten, müssen in einem ovalen Code klar angegeben werden.
- Antragsteller können einen perforierten Abschnitt auf der Packung anbringen, vorausgesetzt, die entfernbaren Daten sind nicht auf Englisch. Dies muss im Antrag erwähnt werden.
- Antragsteller müssen der HPRA am Ende des Prozesses ein PDF der Packungsbeilage zur Aktualisierung auf der Website einreichen.
Kriterien für eine mehrsprachige Packung:
- Der Produktname und seine Stärke müssen in allen Sprachen gleich sein.
- Die Angaben auf der Kennzeichnung und in der Packungsbeilage müssen mit den Summaries of Product Characteristics (SmPC) übereinstimmen.
- Informationen, die auf der Kennzeichnung und der Packungsbeilage gedruckt sind, müssen korrekt und lesbar sein.
- Der rechtliche Status des Arzneimittels muss in beiden Ländern ähnlich sein.
Ein Beispiel für eine mehrsprachige Verpackung ist:
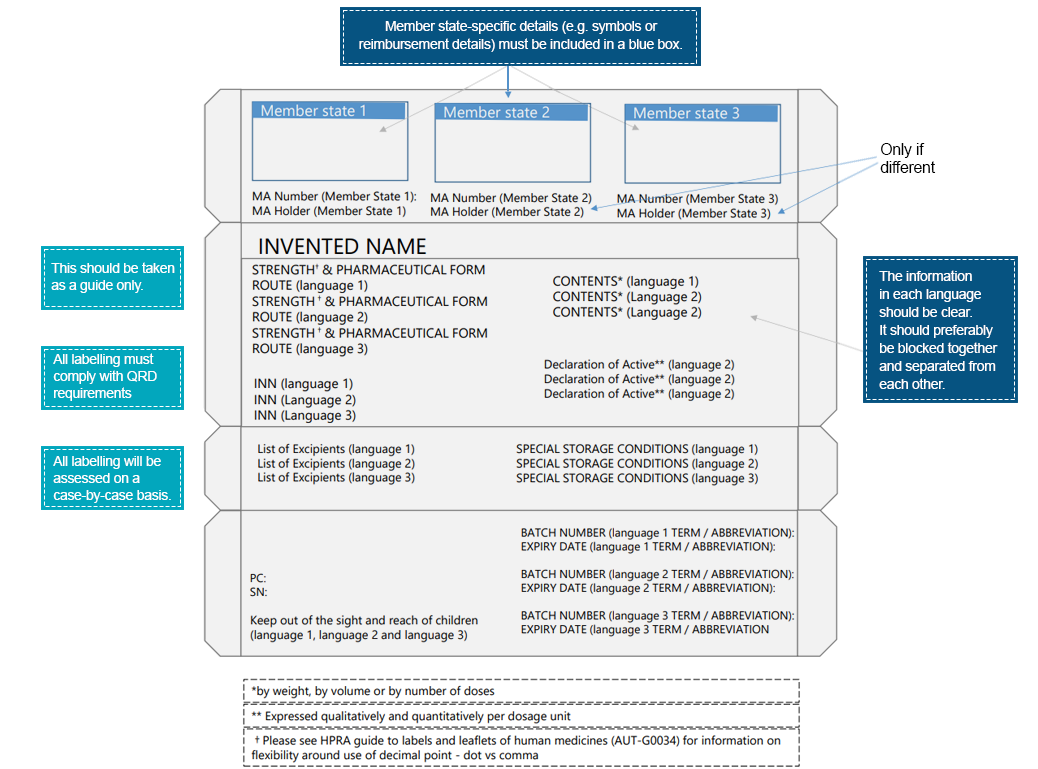
Patienten kommen mit den Arzneimittelkennzeichnungen in Kontakt, lange bevor sie mit dem Arzneimittelprodukt selbst in Berührung kommen. Solche Interaktionen unterstreichen zusätzlich die Bedeutung der Übermittlung wesentlicher Informationen über verschiedene Elemente der Arzneimittelkennzeichnung hinweg. Um eine bessere Lesbarkeit und Optimierung der Kennzeichnungselemente zu gewährleisten, müssen Pharmaunternehmen die notwendigen Maßnahmen ergreifen. Regionale Sprachen bieten ein Medium, um medizinische Anweisungen zu vermitteln, die für das Arzneimittelprodukt relevant sind und die sichere und wirksame Anwendung des verschriebenen Produkts gewährleisten. Länderspezifische Regulierungsexperten können bei der Übersetzung von Kennzeichnungsinformationen gemäß den lokalen/regionalen Vorschriften helfen. Die Experten von Freyr sind bestens gerüstet, um bei der Überbrückung von Lücken zwischen medizinischen Informationen und Sprache zu helfen. Kontaktieren Sie uns für einen konformen Kennzeichnungsprozess.










