
In der sich ständig entwickelnden Welt der Medizinprodukte ist die Einhaltung von Vorschriften keine einmalige Aufgabe, sondern eine fortlaufende Verpflichtung. Die kontinuierliche Überwachung und Aktualisierung wichtiger Berichte wie Klinischer Bewertungsberichte (CERs), Leistungsbewertungsberichte (PERs) und Periodischer Sicherheitsberichte (PSURs) sind während des gesamten Lebenszyklus eines Medizinprodukts, von der ersten Forschung bis zur Überwachung nach dem Inverkehrbringen, entscheidend. Da sich die medizinischen Fortschritte und regulatorischen Anforderungen ständig weiterentwickeln, bleibt die Gewährleistung der Sicherheit und Konformität von Medizinprodukten und IVDs durch effektives medizinisches Schreiben der Eckpfeiler für Erfolg und langfristige Lebensfähigkeit.
Betrachten wir, wie das Lebenszyklusmanagement für den Erfolg eines Medizinprodukts unerlässlich bleibt
Die Markteinführung eines Medizinprodukts ist das Ergebnis jahrelanger Bemühungen, die sich über verschiedene Phasen wie Forschung, Entwicklung, klinische Studien, regulatorische Einreichungen und die Überwachung nach dem Inverkehrbringen erstrecken. Dieser Prozess dauert viele Jahre, und in jeder Phase werden große Mengen wichtiger Daten gesammelt, die sorgfältig zusammengestellt und analysiert werden müssen, um die Sicherheit des Produkts zu gewährleisten.
Die Einhaltung von Vorschriften ist keine einmalige Angelegenheit. Ein effektives Lebenszyklusmanagement hilft, Verzögerungen zu vermeiden, die später kostspielig sein können. Solche Verzögerungen entstehen oft durch unzureichende Planung für unvorhergesehene regulatorische Änderungen oder durch Nichteinhaltung, die möglicherweise übersehen wurde. Regelmäßige Aktualisierungen kritischer Dokumente wie CERs, PERs und PSURs stellen sicher, dass Hersteller sich entwickelnden regulatorischen Anforderungen gerecht werden und die Produktsicherheit aufrechterhalten. Das Lebenszyklusmanagement gewährleistet, dass Hersteller von Anfang an jede Phase geplant haben. So können sie Fallstricke vermeiden und einen erfolgreichen Markteintritt sowie die Langlebigkeit ihrer Geräte sicherstellen.
Bleiben Sie bei der Einhaltung der Vorschriften auf dem Laufenden?
Von Bandagen bis zu Implantaten ist die Medizinprodukteindustrie ein innovativer, kreativer Sektor mit einer Fülle von Möglichkeiten. Obwohl die Hersteller den starken Wunsch haben, sichere und qualitativ hochwertige Produkte auf den Markt zu bringen, bestehen dennoch Unklarheiten. Die EU MDR ersetzte die Medizinprodukterichtlinie (MDD) und die Richtlinie über aktive implantierbare Medizinprodukte (AIMDD). Diese Verordnung wurde eingeführt, um strengere Kontrollen zu verhängen, die Patientensicherheit zu verbessern und eine größere Transparenz im Gesundheitswesen zu fördern. Es gibt viele Unsicherheiten bezüglich dieser Standards, und entscheidende Compliance-Probleme werden häufig übersehen. Medizinproduktehersteller sollten jedoch Maßnahmen ergreifen, um regulatorische Schwierigkeiten zu vermeiden.
Ein Blick auf die häufigsten Herausforderungen, mit denen Hersteller von Medizinprodukten konfrontiert sind
- Aufrechterhaltung von CAPA (Corrective and Preventive Action)
- Einhaltung der Beschwerdeverfahren
- Befolgung der Vigilanzverfahren
- Klinische Bewertung und Überwachung nach dem Inverkehrbringen
- Zusammenarbeit mit Benannten Stellen
Bewährte Verfahren, um regelkonform zu bleiben
Um diese Herausforderungen zu meistern, haben wir bei Freyr Folgendes etabliert:
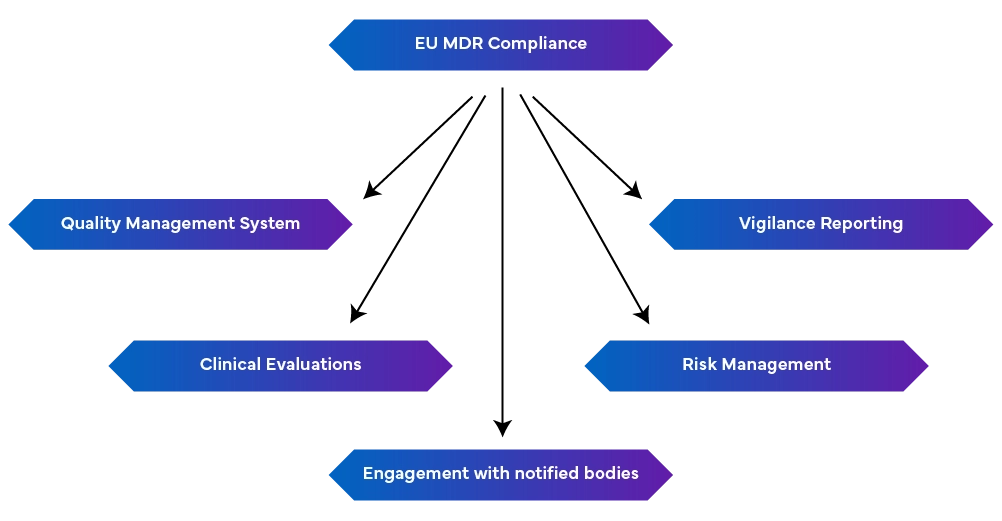
-ein robustes Qualitätsmanagementsystem (EN ISO 13485:2016): Dies umfasst Produktionsaspekte, einschließlich regulatorischer Konformität, technischer Dokumentation, EU-Konformitätserklärungen und Risikomanagement.
-Vigilanzberichterstattung: Die Vigilanzberichterstattung als fortlaufenden Prozess aufrechterhalten und nicht als einmalige Anstrengung betrachten.
- Proaktives Risikomanagement: Hierbei werden Risiken während des gesamten Produktlebenszyklus identifiziert und gemindert, indem regelmäßig Aktualisierungen vorgenommen werden, um auf neue Risiken zu reagieren.
- Durchführung klinischer Bewertungen und Überwachung nach dem Inverkehrbringen: Dies geschieht durch den Nachweis der Gerätesicherheit und -leistung mittels klinischer Daten. Bei Bedarf sollten klinische Prüfungen durchgeführt und klinische Bewertungen regelmäßig mit Daten aus der Überwachung nach dem Inverkehrbringen aktualisiert werden. Periodische Sicherheitsberichte, die die Ergebnisse zusammenfassen, sind ebenfalls erforderlich.
- Zusammenarbeit mit Benannten Stellen: Änderungen in den Vorschriften können die MDR-Anforderungen beeinflussen, weshalb es entscheidend ist, eine gute Beziehung zu Benannten Stellen zu pflegen, um schnelle Aktualisierungen und Anpassungen zu erhalten.
Wie ein Regulierungsexperte Ihnen helfen kann
Mit einer sich ständig ändernden regulatorischen Landschaft Schritt zu halten, kann schwierig sein. Lassen Sie sich daher von einem Experten durch dieses Labyrinth führen. Die Bewältigung der regulatorischen Anforderungen im Lebenszyklus eines Medizinprodukts ist nicht nur komplex, sondern auch ressourcenintensiv. Besonders für kleinere Unternehmen, deren interne Ressourcen in anderen Bereichen besser eingesetzt werden könnten, kann die Unterstützung eines externen Regulierungspartners unerlässlich sein. Diese Partner bieten spezialisiertes Wissen über sich entwickelnde Vorschriften und stellen sicher, dass Ihre wichtigen Berichte – wie CERs, PERs und PSURs – kontinuierlich aktualisiert und konform sind.
Sie können kostspielige Verzögerungen vermeiden, Nichtkonformität verhindern und Ihren Genehmigungsprozess optimieren. Zusätzlich kann ein Regulatorik-Experte maßgeschneiderte Lösungen basierend auf den spezifischen Anforderungen Ihres Produkts anbieten, um sicherzustellen, dass die Überwachung nach dem Inverkehrbringen, die Gap-Analyse und alle Compliance-Dokumentationen auf dem neuesten Stand sind. Ihre Beteiligung kann den gesamten Prozess vereinfachen, Risiken minimieren und gewährleisten, dass das Produkt die Sicherheits- und Leistungsanforderungen erfüllt.
Freyr kann Sie bei all Ihren regulatorischen Anforderungen bezüglich des Lebenszyklusmanagements unterstützen. Kontaktieren Sie uns noch heute!










