
In der heutigen, stark regulierten Pharmabranche ist die Einhaltung der Good Practice (GxP) -Vorschriften nicht nur eine gesetzliche Notwendigkeit, sondern auch eine Verpflichtung gegenüber der Patientensicherheit und der Produktqualität. Da Aufsichtsbehörden weltweit, darunter die FDA EMA, ihren Fokus verstärkt auf Herstellungskontrollen und Produktkonsistenz richten, hat sich die kontinuierliche Prozessüberprüfung (CPV) als wegweisende Methode etabliert, um GxP fortlaufende GxP über den gesamten Produktlebenszyklus hinweg sicherzustellen.
Einführung in die kontinuierliche Prozessüberwachung
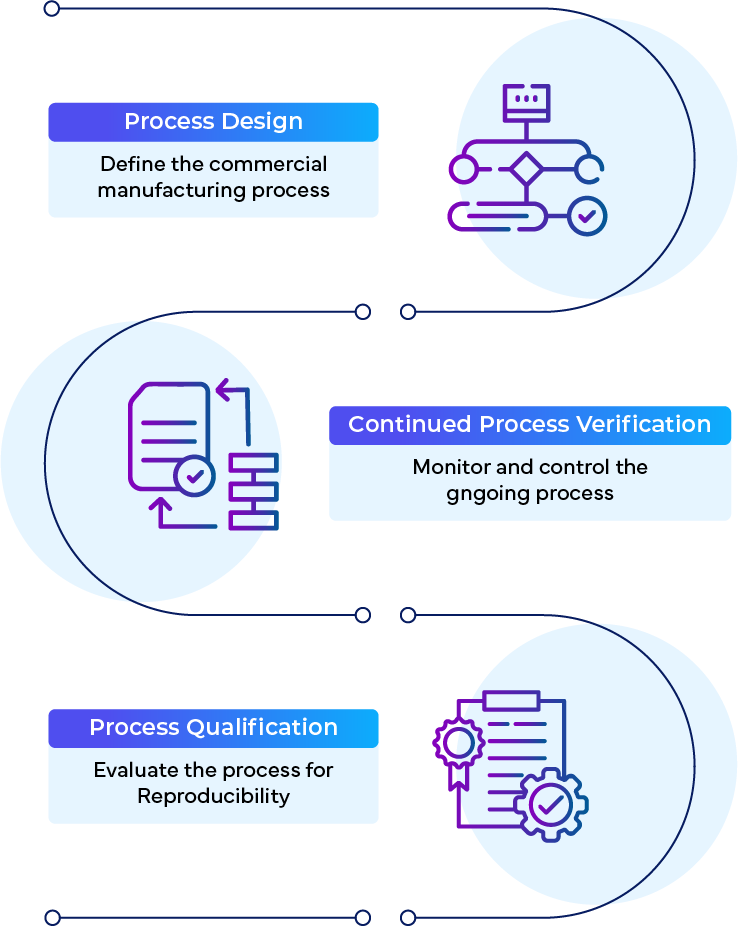
CPV ist eine (1) der drei (3) Phasen in den Leitlinien FDAzur Prozessvalidierung:
- Prozessgestaltung
- Prozessqualifizierung
- Laufende Prozessüberprüfung
Im Gegensatz zu herkömmlichen Validierungsansätzen, die sich häufig stark auf begrenzte Daten aus Chargen vor der Markteinführung stützen, legt CPV den Schwerpunkt auf die Erfassung von Echtzeitdaten und die Trendanalyse während der Routineproduktion. Dieser Wechsel von einem reaktiven zu einem proaktiven Qualitätsmanagement ermöglicht es Herstellern, Prozessabweichungen zu erkennen, Risiken frühzeitig zu minimieren und während der gesamten Marktlebensdauer des Produkts einen validierten Zustand aufrechtzuerhalten.
Warum CPV eine bahnbrechende Neuerung ist
- Echtzeit-Qualitätssicherung
Durch die Erfassung und Analyse von Daten während jedes Produktionsdurchlaufs ermöglicht CPV die sofortige Erkennung von Abweichungen. Diese Echtzeit-Einblicke ermöglichen schnellere Entscheidungen, verringern das Risiko der Auslieferung minderwertiger Produkte und verhindern kostspielige Rückrufaktionen. - Erweitert Einhaltung gesetzlicher Vorschriften
Die Aufsichtsbehörden erwarten zunehmend von Pharmaunternehmen, dass sie Lebenszyklusansätze für die Validierung umsetzen. CPV unterstützt diese Erwartung, indem es einen kontinuierlichen Kontrollstatus nachweist, sich an ICH , Q9 und Q10 anpasst und die Übereinstimmung mit globalen Compliance-Anforderungen sicherstellt.
zur Kostenoptimierung: Die Einführung von CPV erfordert zwar zunächst Investitionen in Analysetechnologien und Schulungen, führt aber letztendlich zu einer Senkung der langfristigen Kosten. Sie minimiert den Bedarf an häufigen Revalidierungen, verringert die Anzahl der Chargenausschüsse und verbessert die Produktionseffizienz.- Datengestützte Entscheidungsfindung
CPV nutzt fortschrittliche statistische Werkzeuge und Automatisierung, um riesige Datenmengen zu verarbeiten. Dieser strukturierte Ansatz für das Datenmanagement unterstützt die strategische Planung, die kontinuierliche Verbesserung und ein fundiertes Risikomanagement – die Eckpfeiler moderner Qualitätssysteme.
Bewährte Verfahren für die Umsetzung
1. Definieren Sie kritische Prozessparameter (CPPs)
Beginnen Sie damit, kritische Prozessparameter (CPPs) und kritische Qualitätsmerkmale (CQAs) auf der Grundlage historischer und experimenteller Daten zu ermitteln und festzulegen. Diese Kennzahlen bilden die Grundlage für die Echtzeitüberwachung.
2. Nutzen Sie digitale Tools und Automatisierungs
en. Integrieren Sie die CPV-Software in Ihre Fertigungssteuerungssysteme (MES) und Laborinformations- und -managementsysteme (LIMS). Durch die Automatisierung werden die Datengenauigkeit, die Datenerfassungshäufigkeit und die Trendvisualisierung verbessert.
3. Funktionsübergreifende Zusammenarbeit
Eine erfolgreiche CPV-Implementierung erfordert die Abstimmung zwischen den Teams aus den Bereichen Qualitätssicherung, Fertigung und IT. Die Festlegung einer einheitlichen CPV-Strategie gewährleistet Konsistenz und gemeinsame Verantwortung.
4. Entwicklung robuster Datenanalysemodelle
Nutzen Sie statistische Prozesskontrolle (SPC), multivariate Analysen und Algorithmen des maschinellen Lernens, um Trends zu analysieren, Abweichungen vorherzusagen und die kontinuierliche Verbesserung zu unterstützen.
5. Anpassung an regulatorische Anforderungen
Dokumentieren Sie jeden Aspekt Ihres CPV-Prozesses und stellen Sie sicher, dass Ihr System für Audits bereit ist. Passen Sie Ihre Dokumentation und Ihre Vorgehensweisen an die weltweiten regulatorischen Anforderungen an.
CPV in der Praxis: Ein Fallbeispiel
Nehmen wir ein Pharmaunternehmen, das sterile Injektionspräparate herstellt. Vor der Einführung von CPV konzentrierten sich die Validierungsmaßnahmen des Unternehmens in erster Linie auf drei (3) Chargen vor der Markteinführung. Abweichungen nach der Markteinführung blieben oft unbemerkt, bis es zu Produktbeschwerden kam.
Im Zuge der Umstellung auf CPV installierte das Unternehmen Echtzeit-Temperatur- und Drucksensoren entlang der gesamten Produktionslinie. Die Daten wurden kontinuierlich mithilfe von SPC-Diagrammen analysiert. So konnte eine geringfügige, aber wiederkehrende Abweichung beim Füllvolumen frühzeitig erkannt werden, sodass Korrekturmaßnahmen ergriffen werden konnten, bevor sich die Abweichung auf die Produktqualität auswirkte. Diese Umstellung stellte nicht nur GxP sicher, sondern reduzierte auch Ausfallzeiten und Nacharbeiten am Produkt erheblich.
Fazit
Die kontinuierliche Prozessüberprüfung ist mehr als nur eine formaler Pflicht zur Einhaltung gesetzlicher Vorschriften. Es handelt sich um einen strategischen Ansatz zur Gewährleistung einer gleichbleibenden Produktqualität, betrieblicher Effizienz und der Einhaltung sich weiterentwickelnder GxP . Mit den richtigen Werkzeugen, der richtigen Einstellung und fachkundiger Beratung können Pharmaunternehmen ihre Validierungsprogramme umgestalten und eine nachhaltige Compliance sicherstellen.
Lassen Sie sich von Freyr auf Ihrer CPV-Reise begleiten
Wir bei Freyr sind auf end-to-end Dienstleistungen end-to-end und Compliance für die Pharmaindustrie spezialisiert. Ganz gleich, ob Sie gerade erst mit der Einführung von CPV beginnen oder Ihr bestehendes System optimieren möchten – unsere Experten unterstützen Sie bei der Konzeption, Implementierung und Validierung robuster, auf Ihre Bedürfnisse zugeschnittener CPV-Rahmenwerke.
Sind Sie bereit, Ihre GxP auf ein neues Niveau zu heben? Kontaktieren Sie Freyr noch heute und erfahren Sie, wie wir Ihnen helfen können, Ihre pharmazeutischen Abläufe zukunftssicher zu machen.










