
Die Entwicklung und Zulassung von Medikamenten für Kinder ist ein entscheidender Aspekt der pädiatrischen Gesundheitsversorgung. Aufgrund ethischer und praktischer Überlegungen sind klinische Studien mit Kindern jedoch oft begrenzt. Daher spielt die Arzneimittelkennzeichnung für Kinder eine entscheidende Rolle, um die sichere und angemessene Anwendung von Medikamenten in dieser vulnerablen Bevölkerungsgruppe zu gewährleisten. In diesem Blog werden wir die Anforderungen an die pädiatrische Arzneimittelkennzeichnung in der Europäischen Union (EU) und den Vereinigten Staaten (US) vergleichen, um ein besseres Verständnis der Ähnlichkeiten und Unterschiede zwischen diesen beiden (02) regulatorischen Rahmenbedingungen zu gewinnen.
EU-Kennzeichnungsvorschriften für Pädiatrika
Die EU hat spezifische Anforderungen an die pädiatrische Kennzeichnung von Arzneimitteln. Diese Anforderungen stellen sicher, dass für Kinder bestimmte Arzneimittel angemessen getestet, zugelassen und gekennzeichnet werden, um sichere und wirksame Behandlungsoptionen für pädiatrische Patienten bereitzustellen.
Gewährleisten Sie die Arzneimittelsicherheit bei Kindern. Kontaktieren Sie uns
Gewährleisten Sie jetzt die Arzneimittelsicherheit bei Kindern
Hier sind einige Aspekte der EU-Anforderungen an die pädiatrische Kennzeichnung:
- Pädiatrische Prüfpläne (PIPs): Ein PIP muss bei der Europäischen Arzneimittel-Agentur (EMA) eingereicht werden, bevor ein Medikament für Kinder zugelassen werden kann. Er beschreibt die Studien und Daten, die erforderlich sind, um die Sicherheit, Wirksamkeit und Dosierung des Medikaments bei pädiatrischen Populationen zu bewerten.
- Zulassung für die pädiatrische Anwendung (PUMA): Wenn ein Medikament bei Kindern untersucht wurde und die Anforderungen erfüllt, kann es eine PUMA erhalten. Diese Zulassung erlaubt die Vermarktung des Medikaments für die pädiatrische Anwendung.
- Altersgerechte Formulierungen: Medikamente für die pädiatrische Anwendung sollten in Formulierungen erhältlich sein, die für verschiedene Altersgruppen geeignet sind, wie Flüssigkeiten, Kautabletten oder altersgerechte Dosierhilfen.
- Pädiatrisch-spezifische Zusammenfassung der Merkmale des Arzneimittels (SmPC): Die SmPC ist ein Dokument, das detaillierte Informationen über ein Medikament enthält. Für pädiatrische Produkte sollte sie spezifische Angaben zur Dosierung, Verabreichung und Sicherheitsaspekte für verschiedene Altersgruppen enthalten.
- Pädiatrische Warnhinweise und Vorsichtsmaßnahmen: Die Kennzeichnung sollte spezifische Warnhinweise oder Vorsichtsmaßnahmen bezüglich der Anwendung des Medikaments bei Kindern enthalten, wie potenzielle Nebenwirkungen oder Wechselwirkungen mit anderen Medikamenten, die häufig bei pädiatrischen Patienten angewendet werden.
- Laufende Überwachung und Aktualisierungen: Sobald ein Medikament für die pädiatrische Anwendung zugelassen ist, können nach der Zulassung Studien erforderlich sein, um zusätzliche Daten zu seiner Sicherheit und Wirksamkeit zu sammeln. Diese können bei Bedarf zu Aktualisierungen der Kennzeichnung führen.
US-Pädiatrische Kennzeichnungsanforderungen
In den US hat die Food and Drug Administration (FDA) den Pediatric Research Equity Act (PREA) und den Best Pharmaceuticals for Children Act (BPCA) eingeführt, um die pädiatrische Arzneimittelforschung und -kennzeichnung zu fördern. PREA verpflichtet Pharmaunternehmen, pädiatrische Studien für bestimmte Arzneimittel durchzuführen, die voraussichtlich bei Kindern angewendet werden. Der BPCA gewährt Unternehmen, die diese Studien durchführen, eine zusätzliche Marktexklusivität von sechs (06) Monaten.
Die FDA setzt weitere Richtlinien durch, um die Arzneimittelsicherheit, Wirksamkeit und korrekte Dosierung bei Kindern wie folgt zu gewährleisten:
- Pädiatrische Studienpläne (PSPs): Hersteller müssen Pläne einreichen, die pädiatrische Studien zur Bewertung der Arzneimittelsicherheit und -wirksamkeit darlegen.
- Alterspezifische Informationen: Etiketten sollten alterspezifische Dosierungen, Indikationen und Sicherheitsaspekte enthalten.
- Gewichtsbasierte Dosierung: Gewichtsabhängige Dosierungsempfehlungen gewährleisten eine genaue Verabreichung.
- Nebenwirkungen: Geben Sie pädiatriespezifische Nebenwirkungen und Sicherheitsdaten an.
- Pädiatriespezifische Formulierungen: Medikamente benötigen möglicherweise pädiatriespezifische Darreichungsformen (z. B. Flüssigkeiten und Kautabletten).
- Human Factors Engineering: Etiketten sollten die einfache Verabreichung für Pflegepersonal berücksichtigen.
- Patienteninformationsblätter: Klare Anweisungen zur Verabreichung, Dosierung und zu Nebenwirkungen sind erforderlich.
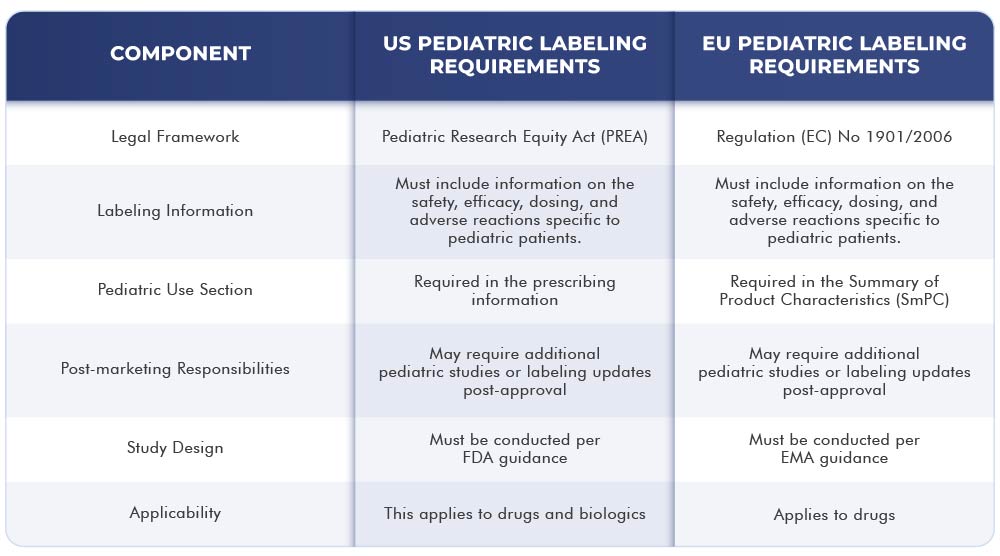
Die folgende Tabelle zeigt die Unterschiede und Gemeinsamkeiten zwischen den Kennzeichnungsanforderungen in den US und der EU:
Fazit
Die Anforderungen an die Arzneimittelkennzeichnung für Kinder in der EU und den US sollen die sichere und angemessene Anwendung von Medikamenten bei Kindern gewährleisten. Obwohl es Ähnlichkeiten zwischen den beiden regulatorischen Rahmenwerken gibt, wie die Notwendigkeit pädiatrischer Studien und die Aufnahme kinderspezifischer Informationen in die Arzneimittelkennzeichnung, bestehen auch deutliche Unterschiede. Das Verständnis dieser Ähnlichkeiten und Unterschiede ist für Pharmaunternehmen, Gesundheitsdienstleister und Regulierungsbehörden von entscheidender Bedeutung, um sicherzustellen, dass Kinder Zugang zu sicheren und wirksamen Medikamenten haben.
Konsultieren Sie einen erfahrenen Kennzeichnungsexperten wie Freyr, um die Einhaltung länderspezifischer Kennzeichnungsvorschriften zu gewährleisten.










