
Eine 510(k)-Meldung oder eine Vorabmeldung vor der Markteinführung ist eine Einreichung bei der US FDA, um zu zeigen, dass das in Verkehr zu bringende Produkt sicher und wirksam ist, d.h. im Wesentlichen einem bereits legal vermarkteten oder einem Referenzprodukt entspricht. Im Folgenden sind die drei (03) Arten von 510(k)-Meldungen aufgeführt, die ein Medizinproduktehersteller einreichen kann:
- Traditionell
- Verkürzt
- Spezielles 510(k)
In diesem Blog werden wir die Fälle untersuchen, unter denen Ihr Antrag gemäß den Anforderungen der US FDA für den zweiten Typ, ein abgekürztes 510(k), qualifiziert wäre.
Ein verkürztes 510(k)-Verfahren wird verwendet, um die wesentliche Äquivalenz zu einem anerkannten Standard, einer speziellen Kontrolle oder einer Leitlinie mittels einer Konformitätserklärung (DoC) nachzuweisen. Bei einer verkürzten Einreichung zeigen Hersteller die wesentliche Äquivalenz zu anerkannten Standards basierend auf der Verwendung von Leitfäden oder DoCs anstelle eines Referenzprodukts, um die Prüfung durch die US FDA zu erleichtern. Unten ist das Flussdiagramm zur Bestimmung der wesentlichen Äquivalenz für einen Antrag auf ein verkürztes 510(k) dargestellt.
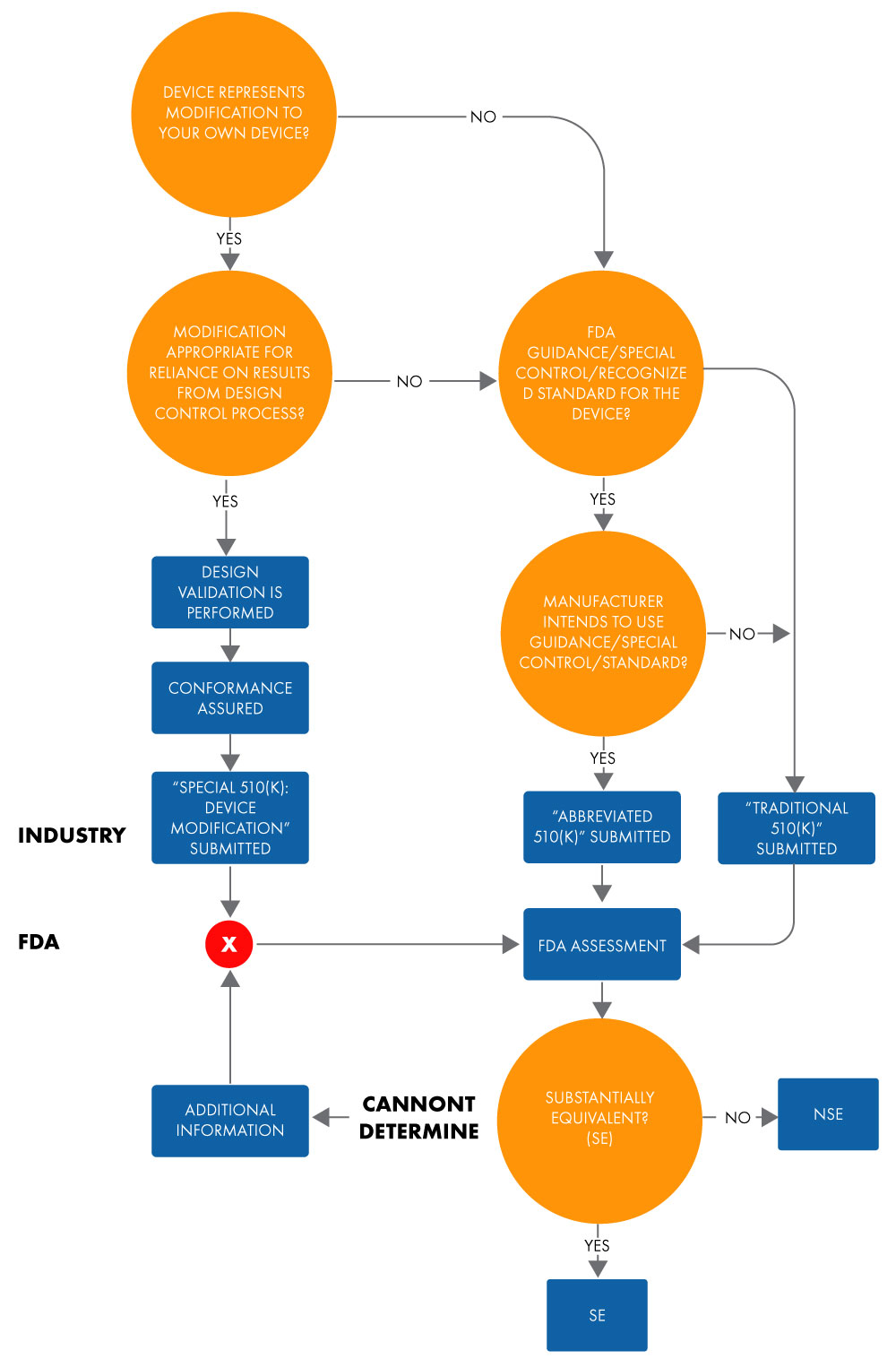
Abbildung 1: Absicht, ein Medizinprodukt über 510(k) zu vermarkten
Der Begriff „verkürzt“ deutet darauf hin, dass dieser Typ des 510(k)-Zulassungsverfahrens kürzer ist. Dies trifft jedoch nicht vollständig zu. Es dauert genauso lange wie eine traditionelle 510(k) -Zulassung. Das Gleiche gilt für Dokumentation und Kosten. Darüber hinaus sind die Formate sowohl für das traditionelle als auch für das verkürzte 510(k) hinsichtlich Kapitelstruktur und Aufbau ähnlich.
Bei der Einreichung eines verkürzten 510(k) sollten Sie sich auf die in 21 CFR 807.87 (traditionelle 510[k]-Einreichungen) genannten Elemente stützen. Sie können ein verkürztes 510(k) einreichen, wenn der Antrag auf Folgendem basiert:
- FDA-Leitfaden(dokumente): Bei der Einreichung eines verkürzten 510(k)-Antrags sollten Sie einen zusammenfassenden Bericht beifügen, der die Einhaltung des relevanten Leitfadendokuments darlegt und beschreibt, wie es bei der Entwicklung und Prüfung des Produkts angewendet wurde.
- Nachweis der Einhaltung besonderer Kontrollen für den Gerätetyp: Sie sollten besondere Kontrollen wie Leistungsstandards, Post-Market Surveillance (PMS), Patientenregister, die Entwicklung und Verbreitung von Leitlinien, Empfehlungen usw. einhalten, die eine angemessene Gewährleistung der Sicherheit und Wirksamkeit des Produkts bieten. Ein verkürzter 510(k)-Antrag, der sich auf eine(n) besondere(n) Kontrolle(n) stützt, sollte Folgendes umfassen: einen zusammenfassenden Bericht, der die Einhaltung der besonderen Kontrollen beschreibt und wie diese bei der Entwicklung und Prüfung des Produkts angewendet wurden.
- Wie die besonderen Kontrollen verwendet wurden, um ein spezifisches Risiko oder Problem anzugehen.
- Informationen, die Abweichungen von den spezifischen Kontrollen und die Bemühungen des Herstellers zur Einhaltung dieser Kontrollen beschreiben.
- Freiwillige Konsensnorm(en): Sie müssen eine Konformitätserklärung (DoC) gemäß der anerkannten Norm für einen verkürzten 510(k)-Antrag einreichen, der sich darauf stützt. Eine Konformitätserklärung (DoC) sollte Folgendes enthalten:
- Name und Anschrift des Antragstellers/Sponsors, der für die DoC verantwortlich ist.
- Details zur Produkt-/Geräteidentifikation, einschließlich Produktcodes, Marketingnamen des Geräts, Modellnummer und aller anderen eindeutigen Produktidentifikationsdaten, die spezifisch für die betreffende Konformitätserklärung sind.
- Eine Konformitätserklärung.
- Eine Liste der Normen, für die die Konformitätserklärung (DoC) gilt, einschließlich der gegebenenfalls für jede Norm gewählten Option(en).
- Die US FDA Anerkennungsnummer für jede Norm.
- Datum und Ort der Ausstellung der Konformitätserklärung (DoC).
- Die Unterschrift, der gedruckte Name und die Funktion des für die Konformitätserklärung (DoC) verantwortlichen Sponsors.
- Jegliche Einschränkung(en) der Gültigkeit der Konformitätserklärung (DoC) (zum Beispiel, wie lange die Erklärung gültig ist, was getestet wurde, Zugeständnisse bezüglich der Testergebnisse usw.).
Zusammenfassend lässt sich sagen, dass ein verkürzter 510(k)-Antrag eine nützliche Möglichkeit für Medizinproduktehersteller ist, die wesentliche Gleichwertigkeit mit anerkannten Normen oder speziellen Kontrollen mithilfe einer Konformitätserklärung (DoC) nachzuweisen. Um sich für einen verkürzten 510(k)-Antrag zu qualifizieren, müssen Medizinproduktehersteller einen zusammenfassenden Bericht vorlegen, der ihre Einhaltung der relevanten Leitfäden erklärt, die Konformität mit speziellen Kontrollen nachweisen und Konformitätserklärungen (DoCs) gemäß anerkannten Normen bereitstellen. Es ist jedoch wichtig zu beachten, dass der Zulassungsprozess, die Dokumentation und die Kosten eines verkürzten 510(k)-Antrags denen eines traditionellen 510(k)-Antrags ähneln.
Qualifiziert sich Ihr Medizinprodukt für einen verkürzten 510(k)-Antrag? Für Unterstützung bei der Einreichung Ihres verkürzten 510(k)-Antrags kontaktieren Sie unsere(n) Regulierungsexperten. Bleiben Sie informiert! Bleiben Sie konform!









