
W branży farmaceutycznej bezpieczeństwo pacjentów zależy od jednego kluczowego czynnika – stałej jakości produktów. Każda tabletka, fiolka czy zastrzyk, które trafiają do pacjenta, muszą działać dokładnie zgodnie z przeznaczeniem. Ta stała jakość jest wynikiem rygorystycznej walidacji procesów (PV), regulowanej przez solidne ramy zapewnienia jakości (QA).
Walidacja procesów to filozofia jakości, która gwarantuje, że procesy produkcyjne są dokładnie poznane, kontrolowane i zdolne do konsekwentnego dostarczania produktów spełniających z góry określone wymagania. Z QA walidacja procesów przestaje być jedynie działaniem mającym na celu spełnienie wymogów regulacyjnych, a staje się proaktywnym zabezpieczeniem zarówno integralności produktu, jak i zdrowia pacjentów.
Czym jest walidacja procesu?
Zgodnie z wytycznymi FDA ICH walidacja procesu to „gromadzenie i ocena danych, począwszy od etapu projektowania procesu aż po produkcję komercyjną, w celu uzyskania naukowych dowodów potwierdzających, że proces ten pozwala na stałe wytwarzanie produktów wysokiej jakości”.
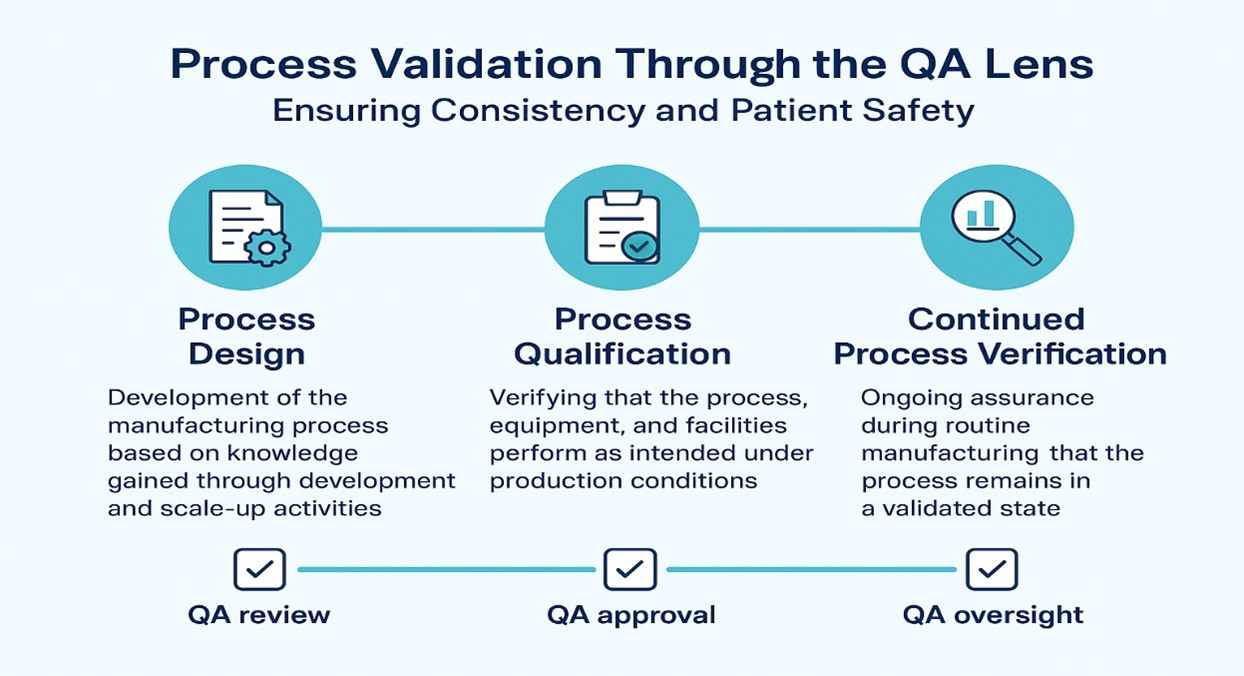
Cykl walidacji zazwyczaj obejmuje trzy (3) kluczowe etapy:
- Etap 1 – Projektowanie procesu:
Opracowanie procesu produkcyjnego w oparciu o wiedzę zdobytą podczas działań związanych z rozwojem i skalowaniem.
QARolaQA: Zapewnienie stosowania oceny ryzyka, kontroli projektowych oraz zasad „jakości poprzez projektowanie” (QbD). - Etap 2 – Kwalifikacja procesu:
Sprawdzenie, czy proces, sprzęt i obiekty działają zgodnie z założeniami w warunkach produkcyjnych.
QARolaQA: zatwierdzanie protokołów kwalifikacyjnych, analiza odstępstw oraz zapewnienie integralności danych podczas realizacji. - Etap 3 – Ciągła weryfikacja procesu (CPV):
Stałe zapewnienie, w trakcie rutynowej produkcji, że proces pozostaje w stanie zatwierdzonym.
QARolaQA: Wdrażanie analiz trendów, wskaźników jakości oraz systemów CAPA w celu utrzymania kontroli.
QA : więcej niż tylko dokumentacja
Podczas gdy walidacja procesu obejmuje oceny techniczne i statystyczne, QA dba o to, by proces ten przebiegał z zachowaniem rygoru naukowego i zgodności z przepisami. Zakres obowiązków QAobejmuje wszystkie etapy – od planowania i zatwierdzania protokołu po zarządzanie zmianami i bieżącą weryfikację.
- Podejście oparte na ryzyku
QA kluczową rolę we wdrażaniu podejścia opartego na ryzyku, zgodnie z wytycznymi ICH . W celu zminimalizowania ryzyka identyfikuje się, ocenia i monitoruje krytyczne parametry procesu (CPP) oraz krytyczne atrybuty jakości (CQA). QA by protokoły walidacyjne były statystycznie uzasadnione, a plany ograniczania ryzyka uwzględnione w projekcie.
- Integralność danych i identyfikowalność
W era cyfrowej integralność danych pozostaje głównym priorytetem QA. Zasady ALCOA+ (przypisane, czytelne, sporządzone w czasie rzeczywistym, oryginalne, dokładne oraz kompletne, spójne, trwałe i dostępne) stanowią wytyczne dla każdego wprowadzania i weryfikacji danych. QA że dane walidacyjne – od kwalifikacji sprzętu po dokumentację partii – są identyfikowalne, zweryfikowane i zgodne z 21 CFR Part 11 .
- Ciągłe doskonalenie dzięki CPV
Po zakończeniu walidacji QA wydajność procesu za pomocą statystycznej kontroli procesów (SPC) oraz narzędzi do analizy trendów. Odchylenia lub wyniki odbiegające od trendu powodują podjęcie działań korygujących i zapobiegawczych (CAPA) w celu ciągłego doskonalenia zdolności procesu. Ten system zamkniętej pętli wzmacnia długoterminową zgodność z wymogami i ogranicza zmienność produktów.
Oczekiwania regulacyjne i światowe standardy
Organy regulacyjne na całym świecie, w tym US FDA, EMA, MHRA i WHO, oczekują od firm farmaceutycznych wykazania walidacji procesów w oparciu o podejście uwzględniające cały cykl życia produktu. QA zgodność z tymi zmieniającymi się wytycznymi, a w szczególności:
- FDA dla przemysłu – Walidacja procesów: ogólne zasady i praktyki
- ICH (Rozwój farmaceutyczny), Q9 (Zarządzanie ryzykiem jakości) oraz Q10 (System jakości w przemyśle farmaceutycznym)
- Załącznik 15 UE – Kwalifikacja i walidacja
Dzięki prowadzeniu ujednoliconej dokumentacji i zapewnieniu identyfikowalności QA gotowość do kontroli oraz zgodność z przepisami na całym świecie, niezależnie od różnic regionalnych.
Wyzwania związane z walidacją procesów i QA
Wyzwanie | Rozwiązanie QA |
|---|---|
Niespójność danych między partiami | Wdrożyć elektroniczne dokumentacje partii (EBR) oraz punkty kontrolne przeglądu QA |
Brak uzasadnienia statystycznego przy doborze próby | QA dostosowania protokołu do statystycznych poziomów ufności (np. 95-procentowych przedziałów ufności) |
Niewystarczająca dokumentacja | QA systemy kontroli dokumentacji oraz identyfikowalność SOP |
Odchylenia podczas walidacji | QA procesem rozpatrywania odstępstw, analizą przyczyn źródłowych oraz wdrażaniem działań korygujących i zapobiegawczych |
Zarządzanie cyklem życia | QA , że programy CPV i warunki wymagające ponownej walidacji są jasno określone |
Transformacja cyfrowa w QA walidacji procesów
Współczesne QA wykorzystują automatyzację i cyfrowe platformy walidacyjne w celu zwiększenia wydajności i dokładności. Narzędzia takie jak systemy zarządzania cyklem walidacji (VLMS) umożliwiają współpracę w czasie rzeczywistym między zespołami QA, produkcji i walidacji.
Dzięki doświadczeniu firmy Freyr w zakresie walidacji systemów komputerowych (CSV) oraz zapewnienia jakości oprogramowania (CSA) klienci mogą wdrażać strategie walidacji cyfrowej zgodne z przepisami, skalowalne i gotowe do kontroli. Zapewnia to nie tylko zgodność z przepisami, ale także doskonałość operacyjną oraz skrócenie czasu wprowadzania produktów na rynek.
Budowanie zaufania poprzez jakość
Walidacja procesów stanowi nieustanne dążenie do zapewnienia jakości, bezpieczeństwa i zaufania pacjentów. Dzięki QA firmy farmaceutyczne mogą zagwarantować, że ich procesy są nie tylko walidowane, ale także stale udoskonalane, tak aby spełniały najwyższe światowe standardy.
Włączając QA każdym etapie walidacji procesów, organizacje wzmacniają swój system zarządzania jakością (QMS), ograniczają ryzyko związane z wymogami regulacyjnymi oraz realizują swój nadrzędny cel – dostarczanie bezpiecznych i skutecznych produktów pacjentom na całym świecie.
W firmie Freyr nasz zespół ekspertów ds. QA walidacji współpracuje z międzynarodowymi firmami farmaceutycznymi w celu stworzenia solidnych, zgodnych z przepisami i gotowych do kontroli systemów walidacji. Od działań naprawczych w ramach systemu zarządzania jakością (QMS) i opracowywania strategii walidacji procesów po cyfrową QA – firma Freyr gwarantuje płynne dostosowanie do wymogów regulacyjnych oraz doskonałość operacyjną.
Dowiedz się, jak firma Freyr może pomóc Ci osiągnąć doskonałość w zakresie walidacji.










