DLACZEGO FREYR?
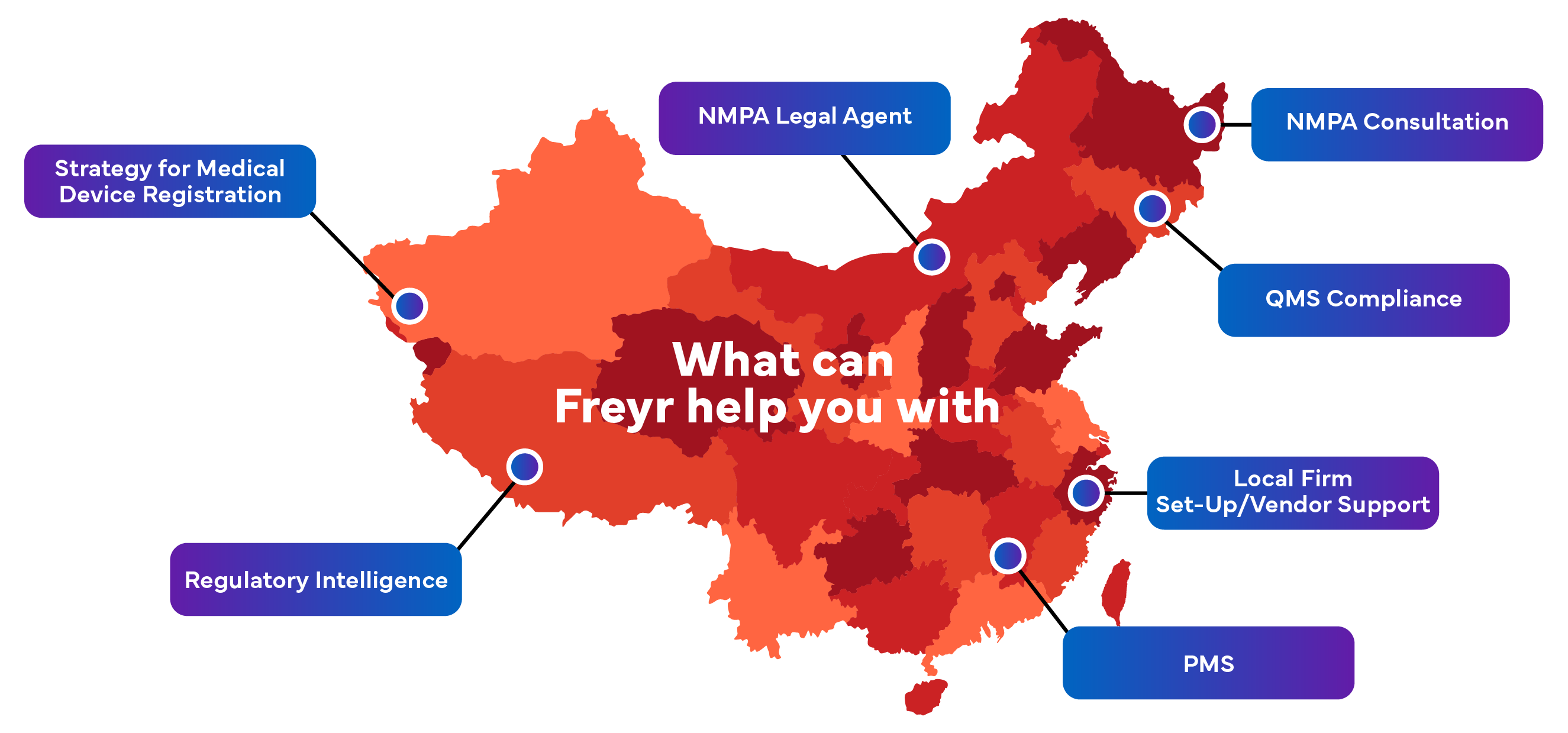
Zapewnij sobie płynny dostęp do rynku z Freyr jako Twoim agentem NMPA w Chinach. Freyr reprezentuje wiele globalnych firm produkujących wyroby medyczne jako agent w Chinach do rejestracji w NMPA.
Poznaj naszych ekspertów regulacyjnych
Umów spotkanie
z naszymi ekspertami regulacyjnymi już dziś, aby szybko osiągnąć zgodność ze wszystkimi chińskimi przepisami dotyczącymi wyrobów medycznych.
Często Zadawane Pytania (FAQ)
- Organ regulacyjny: NMPA (National Medical Products Administration) (dawniej CFDA)
- Rozporządzenie: Zarządzenie Rady Państwa nr 739
- Autoryzowany przedstawiciel: Wymagany agent prawny NMPA
- Wymóg Systemu Zarządzania Jakością: YY/T0287-2017, ISO 13485:2016
- Ocena danych technicznych: Centrum Oceny Wyrobów Medycznych (CMDE)
- Wymogi dotyczące etykietowania: Dekret nr 6 CFDA
- Format zgłoszenia: eRPS
- Język: angielski i chiński
Klasyfikacja wyrobów jest określona w Katalogu Klasyfikacji Wyrobów Medycznych (Ogłoszenie nr 104/2017) Krajowej Administracji Produktów Medycznych (NMPA) * lub/i w zasadach zawartych w Zarządzeniu nr 15 dla wyrobów medycznych. Wyroby są klasyfikowane do trzech (03) klas na podstawie kryteriów ryzyka. Wyroby klasy I to wyroby niskiego ryzyka, a wyroby klasy III to wyroby wysokiego ryzyka.
| Klasa wyrobu | Ryzyko |
| I | Niskie ryzyko |
| II | Średnie ryzyko |
| III | Wysokie ryzyko |
W przypadku rejestracji wyrobów medycznych w Chinach, dla wyrobów medycznych klasy I wymagane jest złożenie dokumentacji w NMPA, a dla wyrobów klasy II i klasy III należy uzyskać certyfikaty rejestracyjne od NMPA. Wyroby klasy I podlegają przeglądowi administracyjnemu, natomiast wyroby klasy II i klasy III przechodzą szczegółowy proces oceny. Wymagania dotyczące danych i badań różnią się w zależności od dostępności produktów referencyjnych. Dlatego producenci wyrobów klasy II i klasy III powinni również zidentyfikować produkty referencyjne, aby określić wymagania dotyczące danych klinicznych dla swoich wyrobów. NMPA wydaje odpowiednio zaświadczenia o złożeniu dokumentacji i certyfikaty rejestracyjne dla wyrobów klasy I oraz klasy II/III.
Podsumowując, w przypadku rejestracji w NMPA-
Klasa I- Dokumentacja rejestracyjna i przegląd administracyjny
Klasa II- Pełna dokumentacja rejestracyjna i pełna ocena wniosku (w tym techniczna)
Klasa III- Pełna dokumentacja rejestracyjna i pełna ocena wniosku (w tym techniczna)
Chińskie przepisy dotyczące wyrobów medycznych określają następujący proces rejestracji w celu uzyskania zgody na wyroby medyczne w Chinach-












