Serviços de Auditoria, Validação e Conformidade Farmacêutica
Beneficie de uma década de proficiência com os nossos serviços através de avaliações de conformidade, auditorias meticulosas e processos de validação robustos.
Explorar Tópicos
- O que é Conformidade, Auditoria e Validação farmacêutica?
- Qual é a importância da Conformidade, Auditoria e Validação na indústria farmacêutica?
- Principais desafios no domínio da Conformidade, Auditoria e Validação.
- O que são Auditorias GxP?
- Compreender as Auditorias Remotas
- O que é a Validação de Sistemas Informáticos (CSV) e porque é crucial na indústria farmacêutica?
- Como a CSV difere da Computer System Assurance (CSA)
- Quais são os componentes de um programa de CSA?
- Como a CSA contribui para a integridade dos dados na indústria farmacêutica?
- Que papel desempenha a conformidade regulamentar na CSA?
- Como ajuda um parceiro estratégico de conformidade regulamentar?
- Porquê escolher a Freyr?
- Os Nossos Serviços
O que é Conformidade, Auditoria e Validação farmacêutica?
Última atualização em: setembro de 2024
No domínio farmacêutico, os processos de conformidade, auditoria e validação são essenciais, salvaguardando a adesão às normas regulamentares, a integridade dos dados e a produção de produtos seguros e eficazes. A conformidade implica alinhar as operações com os regulamentos da indústria e as políticas internas. As auditorias, revisões sistemáticas, verificam a conformidade, identificam áreas de melhoria e mitigam riscos. A validação garante que os sistemas, processos e equipamentos cumprem consistentemente os requisitos predefinidos.
As empresas procuram orientação especializada para avançar sem dificuldades. Os líderes do setor gerem estes processos com competência, garantindo o cumprimento das normas globais sem comprometer a eficácia ou a segurança dos produtos. À medida que o setor farmacêutico evolui, as abordagens estratégicas em matéria de conformidade, auditoria e validação tornam-se fundamentais para o sucesso sustentado. Ao respeitar estes processos, as empresas cumprem os requisitos regulamentares e promovem uma cultura de excelência e inovação num setor dinâmico e desafiante.
Colabore com um parceiro de confiança para orientação estratégica e soluções personalizadas que capacitam as suas operações farmacêuticas a prosperar num cenário Regulatório dinâmico.

Qual é a importância da Conformidade, Auditoria e Validação na indústria farmacêutica?
A conformidade, a auditoria e a validação são componentes críticos na indústria farmacêutica, garantindo que os produtos são seguros, eficazes e produzidos de acordo com as normas regulamentares.
- Garante a Segurança e Eficácia do Produto: A conformidade com os regulamentos garante que os produtos farmacêuticos cumprem rigorosos padrões de segurança e eficácia antes de chegarem ao mercado. Isto envolve processos rigorosos de teste e validação para confirmar que os produtos funcionam conforme o previsto e não representam riscos para os pacientes.
- Mantém a Conformidade Regulamentar: Auditorias e validações regulares ajudam as empresas a cumprir regulamentos complexos e em evolução estabelecidos pelas autoridades de saúde. Isto inclui a conformidade com as Boas Práticas de Fabrico (GMP), as Boas Práticas Clínicas (GCP) e outras normas da indústria, reduzindo o risco de penalidades Regulamentares e recolhas de produtos.
- Melhora a Garantia de Qualidade: Os processos de validação, incluindo as validações de equipamentos e sistemas, garantem que os processos de fabrico e teste produzem consistentemente produtos de alta qualidade. As auditorias verificam se estes processos são seguidos corretamente, levando a uma melhoria da qualidade e fiabilidade do produto.
- Favorece o acesso ao mercado e a reputação: práticas eficazes de conformidade e validação favorecem o acesso ao mercado, demonstrando o cumprimento dos requisitos regulamentares. Isto reforça a reputação e a credibilidade da empresa, criando uma relação de confiança com os profissionais de saúde, os doentes e as entidades reguladoras.
- Facilita a Melhoria Contínua: As auditorias fornecem informações sobre a eficiência dos processos e áreas de melhoria, resultando num melhor controlo de qualidade e em melhores práticas operacionais. Esta avaliação e ajuste contínuos ajudam a manter padrões elevados e a adaptar-se às mudanças nos regulamentos e nas melhores práticas da indústria.
Principais desafios no domínio da Conformidade, Auditoria e Validação.
A área de Conformidade, Auditoria e Validação enfrenta vários desafios importantes que podem afetar a capacidade das empresas farmacêuticas de cumprir os requisitos regulamentares e manter elevados padrões de qualidade e segurança:
| Desafio | Descrição |
|---|---|
| Conformidade Regulatória | As empresas farmacêuticas devem aderir a regulamentos rigorosos de agências como a FDA e a EMA, que exigem documentação rigorosa e medidas de controlo de qualidade. A não conformidade pode levar a penalidades severas, incluindo multas e recolhas de produtos. |
| Controlo de Acesso e Segurança | Garantir que apenas pessoal autorizado possa aceder a áreas e informações sensíveis é crucial. Isso envolve a implementação de sistemas avançados de controlo de acesso e a manutenção da cibersegurança contra ameaças, o que pode ser complexo e dispendioso. |
| Validação de Sistemas Computorizados (CSV) | A validação de sistemas informáticos utilizados em ambientes GxP é essencial, mas muitas vezes onerosa e mal definida. O processo exige tempo e recursos significativos, especialmente quando uma abordagem padrão é aplicada indiscriminadamente. |
| Formação e Sensibilização dos Colaboradores | Programas de formação contínua são necessários para garantir que os colaboradores compreendem os protocolos de conformidade e a sua importância. Uma formação inadequada pode levar à não conformidade e a erros nos processos. |
| Documentação e Manutenção de Registos | Manter uma documentação precisa e abrangente é vital para a conformidade. A documentação inadequada é um problema comum que pode levar a observações regulamentares e falhas durante as auditorias. |
| Integridade dos Dados | Garantir a integridade e a exatidão dos dados é crucial, especialmente na gestão de grandes volumes de informação. Os desafios incluem o manuseamento manual de dados e a necessidade de sistemas robustos de gestão de dados. |
| Gestão de Fornecedores | A dependência de fornecedores terceiros para software e serviços exige validação rigorosa e verificações de conformidade. Gerir estas relações e garantir que cumprem os padrões regulamentares pode ser um desafio. |
| Complexidade Tecnológica | A crescente complexidade das tecnologias, incluindo IA e sistemas Cloud-based, apresenta novos desafios de validação e exige uma adaptação contínua aos cenários de Regulamentação em evolução. |
| Controlo de Qualidade Inadequado | Muitas empresas farmacêuticas têm dificuldade em manter elevados padrões de qualidade em todos os seus processos, o que pode levar a contaminação, contaminação cruzada e outros problemas de qualidade. |
| Melhoria Contínua e Monitorização | Auditorias e inspeções regulares são essenciais para identificar pontos fracos nos sistemas de conformidade. No entanto, muitas organizações não conseguem implementar medidas proativas para a melhoria contínua. |
- Regulamentações em Evolução: Manter-se atualizado com as regulamentações e diretrizes em rápida mudança em diferentes regiões pode ser um desafio. As empresas farmacêuticas devem atualizar continuamente as suas práticas de conformidade para aderir aos padrões Regulatórios novos ou revistos, o que pode exigir recursos e ajustes significativos.
- Complexidade das Normas Globais: Navegar pelos diversos e complexos requisitos regulamentares de diferentes países e regiões aumenta o desafio. Cada jurisdição pode ter o seu próprio conjunto de regras e normas, tornando difícil alcançar uma conformidade consistente em todos os mercados globais.
- Integridade e Segurança dos Dados: Garantir a integridade e a segurança dos dados ao longo dos processos de conformidade, auditoria e validação é fundamental. As empresas devem implementar sistemas e controlos robustos para proteger contra violações de dados, adulteração ou imprecisões, que podem ter consequências graves para a aprovação do produto e a segurança do paciente.
- Restrições de Recursos: Recursos limitados, incluindo tempo, pessoal e orçamento, podem dificultar a eficácia das atividades de conformidade e auditoria. As empresas muitas vezes debatem-se para equilibrar as exigências de manutenção da conformidade com a necessidade de alocar recursos para outras funções empresariais críticas.
- Gestão da Documentação e Arquivo: A documentação e o arquivo adequados são essenciais para demonstrar conformidade e realizar auditorias eficazes. No entanto, gerir grandes volumes de documentação, assegurar a sua exatidão e manter a acessibilidade pode ser um desafio, especialmente num ambiente altamente regulamentado.
- Integração de Novas Tecnologias: A incorporação de tecnologias inovadoras em processos de conformidade e validação existentes pode ser complexa. Embora tecnologias como a automação e a IA (Inteligência Artificial) ofereçam benefícios significativos, a sua integração deve ser cuidadosamente gerida para garantir que cumprem os requisitos de Regulamentação e não introduzem novos riscos.
- Formação e Competência: Garantir que o pessoal está adequadamente formado e competente nos processos de conformidade, auditoria e validação é crucial. São necessários programas de formação contínuos para manter o pessoal atualizado sobre as alterações regulamentares e as melhores práticas, o que pode ser intensivo em recursos.
- Gerir as Descobertas da Auditoria: Gerir e corrigir eficazmente os problemas identificados durante as auditorias pode ser desafiador. As empresas devem implementar ações corretivas e preventivas prontamente, garantindo que estas ações não perturbem as operações em curso nem afetem a qualidade do produto.
- Equilibrar a Conformidade com a Inovação: Encontrar um equilíbrio entre o cumprimento de regulamentações rigorosas e a procura da inovação pode ser difícil. As empresas devem navegar no panorama regulamentar enquanto continuam a desenvolver e a introduzir novos produtos e tecnologias.
- Garantir a Consistência em Todas as Operações: Manter a consistência nas práticas de conformidade e nos processos de validação em diferentes departamentos, instalações e fases do ciclo de vida do produto é essencial, mas desafiador. A variabilidade nas práticas pode levar à não conformidade e a problemas de qualidade.
O que são Auditorias GxP?
O que é uma auditoria de conformidade independente GxP e quem a realiza?
Uma auditoria GxP é um processo concebido para garantir que as empresas cumprem as normas pré-definidas de qualidade, segurança e conformidade regulamentar. Pode abranger vários aspetos dos produtos e processos farmacêuticos, tais como as Boas Práticas de Laboratório (GLP), as Boas Práticas Clínicas (GCP), as Boas Práticas de Fabrico (GMP) e as Boas Práticas de Farmacovigilância (GVP).
A auditoria avalia o nível de conformidade com as leis, regulamentos, diretrizes e Procedimentos Operacionais Padrão (POP) aplicáveis e identifica as lacunas, os riscos e as oportunidades de melhoria. A auditoria apresenta ainda recomendações e medidas corretivas para dar resposta às constatações e reforçar os sistemas de qualidade.
Os benefícios de uma auditoria GxP incluem:
- Fornecer uma avaliação imparcial e objetiva dos sistemas de qualidade e do nível de conformidade.
- Aumentar a confiança dos reguladores, clientes, fornecedores e outras partes interessadas.
- Reduzir a probabilidade e a gravidade de inspeções, observações e sanções regulamentares.
- Melhorar a qualidade, segurança e eficácia dos produtos e processos.
- Aumentar a eficiência e a eficácia das operações e reduzir os custos e os erros.
- Apoiar a melhoria contínua e a inovação dos produtos e processos.
Uma auditoria GxP é realizada por um auditor qualificado e experiente ou por uma equipa de auditores com conhecimentos, competências e credenciais relevantes na indústria farmacêutica e na área GxP específica. O auditor ou a equipa de auditoria deve ser independente da empresa auditada e seguir as normas profissionais e os princípios éticos de auditoria. Devem também utilizar ferramentas e métodos apropriados para conduzir a auditoria, tais como listas de verificação, entrevistas, observações, revisões de documentos, amostragem, testes, etc. A Freyr oferece apoio End-to-End em auditorias GxP. Como líder da indústria, os nossos especialistas tornarão o seu percurso de conformidade contínuo.
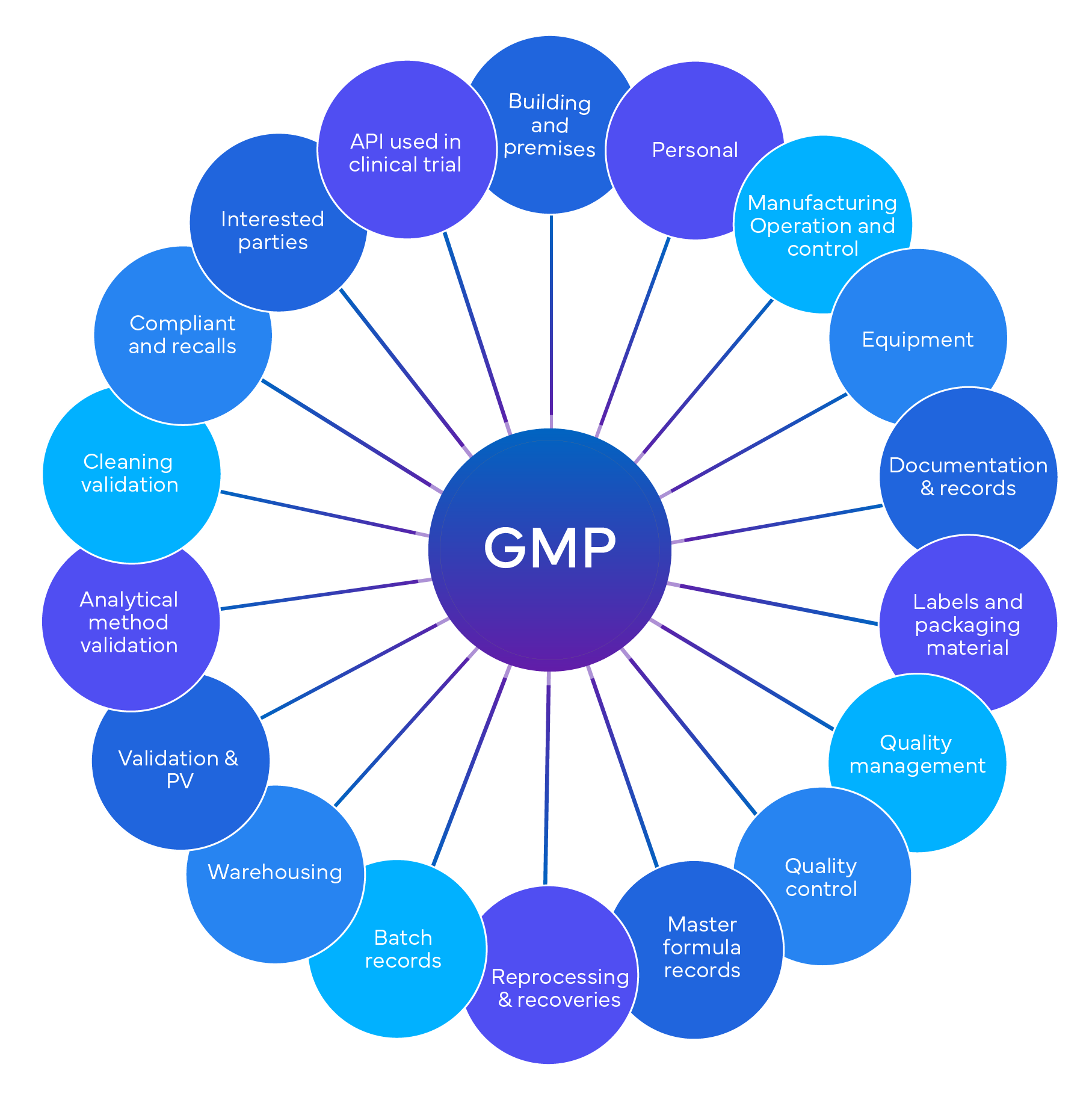
Quadro Regulamentar para Auditorias GxP
A conformidade GxP é um conjunto de regulamentos que regem várias indústrias regulamentadas, incluindo produtos farmacêuticos, dispositivos médicos, alimentos, bebidas e biotecnologia. O objetivo principal da conformidade GxP é manter a qualidade do produto e garantir a segurança pública. Aqui estão alguns pontos-chave:
- Visão Geral da Conformidade GxP:
- O GxP abrange várias normas, incluindo as Boas Práticas de Laboratório (BPL), as Boas Práticas Clínicas (BPC), as Boas Práticas de Fabrico (BPF) e as Boas Práticas de Farmacovigilância (BPFV).
- Estas normas garantem que os produtos são rigorosamente testados, fabricados e manuseados ao longo do seu ciclo de vida.
- Conferência Internacional sobre Harmonização (ICH):
- O ICH fornece diretrizes para a conformidade com as GxP.
- A Orientação sobre Boas Práticas de Fabrico ICH Q7A aborda especificamente as práticas de fabrico para ingredientes farmacêuticos ativos (APIs).
- Inspeções da FDA:
- A Food and Drug Administration dos US (FDA) realiza inspeções para avaliar a conformidade com os regulamentos GxP.
- Estas inspeções avaliam a adesão a regulamentos e diretrizes específicos da FDA.
- Inspeções do Health Canada:
- A Health Canada, a autoridade regulamentar no Canadá, também realiza inspeções para garantir a conformidade com as GxP.
- Estas inspeções focam-se em vários aspetos, incluindo fabrico, controlo de qualidade e distribuição.
- Critérios de Avaliação para Auditorias GxP:
A conformidade em auditorias independentes GxP é tipicamente avaliada com base numa série de critérios, que podem incluir:
- Requisitos Regulamentares: Conformidade com regulamentos, diretrizes e leis específicas aplicáveis à área GxP (por exemplo, regulamentos da FDA, diretrizes ICH ou normas ISO).
- Sistemas de Qualidade: Avaliação de sistemas de gestão da qualidade, práticas de documentação e manutenção de registos.
- Validação de Processos: Verificação de que os processos são validados e cumprem os critérios predefinidos.
- Formação e Competência: Avaliação da formação e qualificações do pessoal.
- Gestão de Risco: Identificação e mitigação de riscos relacionados com a qualidade e segurança do produto.
Saiba como um especialista comprovado em Assuntos Regulamentares pode ajudá-lo a criar a estrutura de auditoria GxP ideal, adequada às suas necessidades, e a manter-se em conformidade com os regulamentos globais.
Benefícios da Realização de Auditorias de Conformidade GxP
As auditorias GxP oferecem inúmeros benefícios para qualquer organização. Em primeiro lugar, fornecem uma avaliação imparcial e independente do risco e da conformidade dentro da organização, permitindo que as empresas identifiquem áreas de não conformidade ou risco potencial que poderiam ser negligenciadas em auditorias internas. Estas auditorias são essenciais para garantir que as empresas cumprem determinados padrões de qualidade, segurança e conformidade regulamentar.
| Aspeto | Descrição |
|---|---|
| Revisão Abrangente | Avaliação exaustiva por um terceiro qualificado para identificar áreas de não conformidade. |
| Normas Regulamentares | Adesão às normas GxP (boas práticas) como GMP, GCP e GLP. |
| Âmbito Personalizado | Âmbito de auditoria personalizado com base em produtos e processos específicos. |
| Auditores Qualificados | Auditores experientes e familiarizados com os regulamentos. |
| Quadro Regulatório | Segue as diretrizes ICH Q7A, da FDA e do Health Canada. |
| Benefícios | Avaliações imparciais, prevenção de riscos, manutenção da qualidade e escalabilidade. |
Aqui estão alguns pontos-chave sobre as auditorias de conformidade GxP:
- Revisão Abrangente: As auditorias GxP envolvem um processo de revisão exaustivo conduzido por uma organização ou consultor terceiro qualificado. O objetivo é identificar quaisquer áreas de não conformidade dentro da organização e fornecer recomendações para melhoria.
- Normas Regulamentares: Os regulamentos revistos durante estas auditorias são definidos pelas normas GxP (boas práticas), tais como as Boas Práticas de Fabrico (BPF), as Boas Práticas Clínicas (BPC) e as Boas Práticas de Laboratório (BPL). Estas normas garantem que os produtos, serviços e processos cumprem consistentemente os requisitos Regulamentares relevantes.
- Âmbito Personalizado: O âmbito de uma auditoria independente é adaptado aos produtos e processos específicos da organização. Pode incluir gestão de pessoal, gestão de instalações, manutenção de registos, garantia e controlo de qualidade, conceção de produtos e processos, e operações técnicas.
- Auditores Qualificados: A auditoria deve ser conduzida por um auditor qualificado e experiente que esteja familiarizado com os regulamentos aplicáveis e possua a experiência necessária para avaliar eficazmente os procedimentos e processos da organização.
- Estrutura Regulamentar: As auditorias GxP seguem estruturas como a Orientação de Boas Práticas de Fabrico ICH Q7A da Conferência Internacional sobre Harmonização (ICH), inspeções da FDA e inspeções da Health Canada. Estas estruturas fornecem orientação sobre os requisitos básicos para a produção, garantia de qualidade, distribuição e outras atividades críticas relacionadas com o fabrico seguro de produtos.
- Benefícios: As auditorias GxP oferecem avaliações imparciais, ajudam a prevenir problemas de não conformidade, mantêm os padrões de qualidade e garantem a responsabilização. A terceirização destas auditorias proporciona acesso a experiência, objetividade, eficiência de custos e escalabilidade, permitindo que as empresas se concentrem nas suas competências essenciais.
Se procura soluções de conformidade GxP, considere a Freyr. Especializamo-nos em conformidade regulamentar, garantia de qualidade e segurança em toda a indústria das ciências da vida. Com a nossa experiência, pode garantir a adesão às normas GxP, otimizar processos e manter produtos e serviços de alta qualidade.
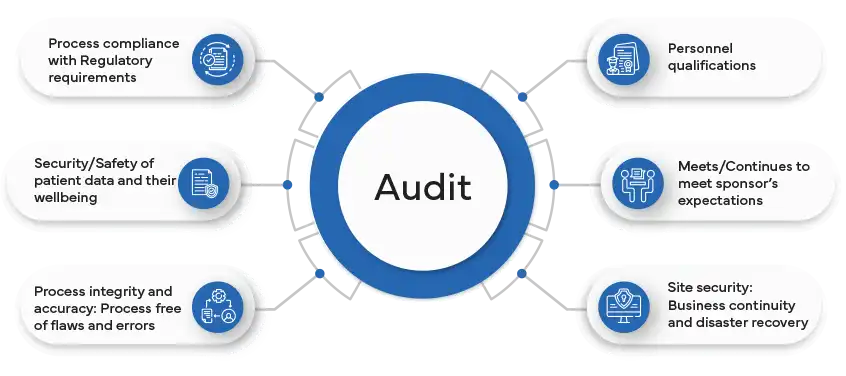
Dicas para Preparar a Sua Organização para uma Auditoria
Preparar a sua organização para uma auditoria é um processo estratégico que envolve um planeamento meticuloso e uma abordagem proativa. Em primeiro lugar, certifique-se de que todos os registos, documentação e ficheiros relevantes estão organizados e facilmente acessíveis. Um sistema de arquivo bem organizado facilita um processo de auditoria mais tranquilo e reflete positivamente o profissionalismo da sua organização.
Em segundo lugar, realize uma pré-auditoria interna para identificar potenciais áreas de preocupação. Esta autoavaliação permite-lhe abordar quaisquer problemas ou discrepâncias antes da auditoria externa. Ao resolver proativamente os problemas, demonstra o seu compromisso com a conformidade e a transparência.
Em terceiro lugar, comunique e colabore eficazmente com a equipa de auditoria. Forneça as informações necessárias, acesso ao pessoal relevante e um ambiente de trabalho propício. Uma comunicação clara ajuda a construir um relacionamento positivo com os auditores, promovendo uma atmosfera colaborativa durante o processo de auditoria.
Por último, certifique-se de que a sua equipa está bem treinada e ciente do processo de auditoria. Eduque os colaboradores sobre os seus papéis, responsabilidades e a importância da conformidade. Ao incutir uma cultura de preparação e cooperação, a sua organização pode gerir auditorias com confiança e profissionalismo.
Compreender as Auditorias Remotas
O que é uma auditoria remota na indústria farmacêutica e como difere das auditorias presenciais tradicionais?
Uma auditoria remota na indústria farmacêutica consiste numa avaliação abrangente dos processos, instalações e sistemas de uma empresa, realizada por autoridades reguladoras ou auditores sem presença física no local. Esta auditoria é facilitada através de ferramentas de comunicação digital, software colaborativo e acesso remoto a documentos e sistemas relevantes. Tem como objetivo garantir a conformidade com as normas regulamentares, avaliar os sistemas de gestão da qualidade e verificar o cumprimento das Boas Práticas de Fabrico (BPF), das Boas Práticas Clínicas (GCP) ou de outros regulamentos aplicáveis.
A diferença entre auditorias remotas e auditorias presenciais tradicionais é a ausência de presença física durante uma auditoria remota. Em vez de visitarem as instalações da empresa, os auditores dependem de interações virtuais, documentação eletrónica e acesso remoto a sistemas. Esta abordagem oferece flexibilidade e eficiência, permitindo que as auditorias ocorram independentemente das distâncias geográficas e das restrições de viagem. No entanto, desafios como a observação direta limitada das instalações e potenciais preocupações com a cibersegurança precisam de ser abordados para garantir a eficácia das auditorias remotas.
Apesar das diferenças, os objetivos das auditorias remotas e tradicionais permanecem os mesmos – verificar a conformidade, identificar áreas para melhoria e garantir a qualidade e segurança dos produtos farmacêuticos. A escolha entre auditorias remotas e presenciais depende de fatores como a natureza da auditoria, os requisitos regulamentares e as capacidades da empresa em facilitar uma avaliação completa por meios remotos.
A Freyr utiliza uma década de experiência para fornecer soluções de Regulamentação inigualáveis, garantindo a conformidade e o sucesso no dinâmico panorama farmacêutico.
Explore a excelência em Regulamentação connosco – o seu parceiro estratégico para o sucesso da conformidade na indústria farmacêutica em constante evolução. Fale connosco para navegar pelas complexidades da Regulamentação sem problemas.
Que desafios podem surgir durante auditorias remotas e como são abordados para garantir avaliações rigorosas?
Durante auditorias remotas, podem surgir vários desafios, mas as organizações podem tomar medidas para os abordar e garantir avaliações completas. Aqui estão alguns desafios chave e as suas potenciais soluções:
- Estabelecer Relações Essenciais com as Partes Interessadas da Auditoria:
- Desafio: O trabalho remoto pode dificultar o desenvolvimento de relações sólidas com as partes interessadas da auditoria.
- Solução: Reuniões virtuais regulares, comunicação aberta e envolvimento ativo podem ajudar a construir e manter relações. Utilizar videochamadas para estabelecer uma ligação pessoal.
- Investimento em Tecnologia para Trabalho Virtual:
- Desafio: As auditorias remotas dependem fortemente da tecnologia, e ferramentas inadequadas podem prejudicar a eficiência.
- Solução: Investir em software robusto de gestão de auditorias, plataformas de comunicação seguras e ferramentas de colaboração. Garantir que os auditores têm o hardware e o software necessários.
- Desenvolver Colaboradores e Promover uma Cultura Positiva Remotamente.:
- Desafio: O trabalho remoto pode levar ao isolamento e dificultar o crescimento profissional.
- Solução: Oferecer formação virtual, mentoria e oportunidades para o desenvolvimento de competências. Promover uma cultura positiva através de atividades de team-building, reconhecimento e verificações regulares.
- Cultivar uma Mentalidade Intencional e Adaptativa:
- Desafio: Os auditores remotos devem adaptar-se às circunstâncias em mudança e manter o foco.
- Solução: Incentivar a flexibilidade, a adaptabilidade e uma mentalidade de crescimento. Formar os auditores para lidar com situações inesperadas e ajustar a sua abordagem conforme necessário.
A Freyr é um parceiro de confiança em soluções de conformidade Regulamentar e segurança para a indústria das ciências da vida. Com profunda experiência no setor, tecnologia inovadora e uma presença global, a Freyr capacita as organizações a navegar pelos complexos cenários de Regulamentação sem problemas. Explore os nossos serviços e contacte-nos hoje para elevar a sua jornada de conformidade.
Como está a Freyr mais bem posicionada para o ajudar com as suas auditorias remotas?
A Freyr, com a sua experiência de uma década, destaca-se na facilitação de auditorias remotas sem problemas para a indústria farmacêutica. Aproveitando tecnologias avançadas e um profundo conhecimento dos requisitos de Regulamentação, a Freyr garante um processo de auditoria completo e eficiente, abordando desafios como a presença física limitada e as preocupações com a cibersegurança.
A nossa equipa dedicada de especialistas em Regulamentação é proficiente na utilização de soluções digitais inovadoras, garantindo uma avaliação virtual abrangente dos seus processos, instalações e documentação. O nosso historial comprovado em auditorias remotas reflete o nosso compromisso em fornecer soluções de Regulamentação fiáveis e eficazes, adaptadas às necessidades em evolução do panorama farmacêutico. Com a Freyr, ganha um parceiro de confiança que compreende as complexidades das auditorias remotas e adota uma abordagem proativa e colaborativa para melhorar o seu percurso de conformidade.
O que é a Validação de Sistemas Informáticos (CSV) e porque é crucial na indústria farmacêutica?
Validação de Sistemas Computorizados (CSV) é um processo crítico na indústria farmacêutica que garante a integridade, fiabilidade e conformidade dos sistemas computadorizados utilizados para vários fins. Vamos aprofundar os detalhes:
- Definição e Objetivo:
- CSV é o processo documentado que garante que um sistema informático produzirá informações ou dados que cumprem requisitos predefinidos.
- O seu principal objetivo é validar e verificar que os sistemas informáticos funcionam consistentemente conforme o previsto, mantendo a exatidão, fiabilidade e segurança dos dados.
- Importância na Indústria Farmacêutica:
- Conformidade com a Regulamentação: A indústria farmacêutica opera sob regulamentações rigorosas (como as Boas Práticas de Fabrico ou GMP) para garantir a qualidade, segurança e eficácia do produto.
- Integridade dos Dados: Dados precisos e fiáveis são cruciais para o desenvolvimento de medicamentos, ensaios clínicos, fabrico e distribuição.
- Mitigação de Risco: A CSV ajuda a identificar e mitigar riscos associados a sistemas informáticos, prevenindo erros, perda de dados e não conformidade.
- Segurança do Paciente: Sistemas devidamente validados contribuem para a segurança dos pacientes, garantindo uma qualidade consistente e a adesão aos padrões.
- Aspetos Essenciais da CSV:
- Definição de Requisitos: Definir claramente os requisitos do sistema, as funcionalidades e as expectativas dos utilizadores.
- Conceção e Configuração: Desenvolver e configurar o sistema de acordo com as especificações.
- Testes e Qualificação: Testes rigorosos (incluindo testes unitários, testes de integração e testes de aceitação do utilizador) para verificar o desempenho do sistema.
- Documentação: Mantenha documentação abrangente ao longo de todo o ciclo de vida do sistema.
- Controlo de Alterações: Gerir as alterações ao sistema, garantindo que não comprometem a sua integridade.
- Desafios Abordados por CSV:
- Integridade dos Dados: Prevenir o acesso não autorizado, a corrupção de dados ou a manipulação.
- Segurança do Sistema: Proteger contra ameaças cibernéticas e modificações não autorizadas.
- Rasto de Auditoria: Manter um rasto de dados eletrónico indelével para auditorias regulamentares.
- Manutenção da Validação: Rever e atualizar regularmente a validação para se adaptar às alterações do sistema.
Como a CSV difere da Computer System Assurance (CSA)?
A Validação de Sistemas Computorizados (CSV) e a Garantia de Sistemas Computorizados (CSA) representam abordagens distintas para assegurar a integridade e a conformidade dos sistemas computorizados na indústria farmacêutica. A CSV, uma prática de longa data, foca-se principalmente na fase de validação do ciclo de vida de um sistema, garantindo que os sistemas de software cumprem os requisitos regulamentares através de protocolos predefinidos. Por outro lado, a CSA adota uma abordagem mais abrangente e dinâmica, cobrindo todo o ciclo de vida de um sistema computorizado, desde o desenvolvimento e implementação até à utilização operacional e eventual desativação.
A CSV aborda a necessidade de processos de validação rigorosos, enfatizando abordagens baseadas no risco para identificar e mitigar potenciais problemas. No entanto, o panorama farmacêutico está a evoluir, impulsionando o surgimento da CSA como uma estratégia mais abrangente. A CSA estende o seu foco para além da validação, adaptando metodologias ágeis e incorporando monitorização contínua ao longo do ciclo de vida de um sistema. Esta perspetiva holística permite que as organizações geram proativamente os riscos, especialmente em cibersegurança e integridade de dados, alinhando-se com a crescente ênfase da indústria na tecnologia e segurança de dados.
A adaptabilidade da CSA é valiosa num ambiente regulatório em rápida evolução. Enquanto a CSV segue as práticas tradicionais de validação, a CSA alinha-se com as expectativas em constante evolução das autoridades reguladoras. Vai além dos esforços de revalidação periódica, incorporando monitorização contínua, análise de dados em tempo real e estratégias proativas de gestão de riscos para garantir a conformidade contínua e o desempenho ideal. À medida que a indústria farmacêutica adota a transformação digital, compreender as nuances entre o CSV e o CSA torna-se imperativo para as empresas que pretendem manter-se na vanguarda em matéria de conformidade regulamentar e integridade do sistema.
Neste contexto, a Freyr, com a sua vasta experiência e conhecimento, está bem equipada para guiar as empresas farmacêuticas através das complexidades tanto da CSV como da CSA, oferecendo soluções personalizadas para satisfazer as exigências em evolução da conformidade com a Regulamentação e dos avanços tecnológicos.
Quais são os componentes de um programa de CSA?
Garantia de Software Informático (CSA) é uma abordagem moderna que melhora a fiabilidade, a segurança e a conformidade em sistemas informatizados. Vamos explorar os seus componentes e benefícios a longo prazo:
- Abordagem baseada no risco:
- Componente: A CSA foca-se na avaliação e gestão de riscos.
- Importância: Identificar áreas críticas ajuda a alocar os esforços de validação de forma eficaz.
- Testes Não Estruturados:
- Componente: O CSA inclui testes não-roteirizados para além dos casos de teste roteirizados tradicionais.
- Importância: Testes não planeados simulam cenários do mundo real, revelando problemas ocultos.
- Monitorização Contínua do Desempenho:
- Componente: A CSA envolve a monitorização contínua do desempenho do sistema.
- Importância: Detetar anomalias precocemente previne falhas no sistema e problemas de integridade dos dados.
- Supervisão de Dados:
- Componente: O CSA enfatiza a qualidade e integridade dos dados.
- Importância: Garante dados precisos para a tomada de decisões e conformidade.
- Atividades de Validação Externa.:
- Componente: A CSA colabora com fornecedores de software para validação externa.
- Importância: A validação independente aumenta a confiança e reduz o viés.
- Transição da CSV para a CSA:
- Etapas Iniciais:
- Compreender os princípios da CSA.
- Avaliar os sistemas existentes quanto ao risco.
- Priorizar funcionalidades críticas.
- Benefícios:
- Carga de trabalho de validação reduzida.
- Resposta ágil às mudanças.
- Fiabilidade do sistema melhorada.
- Etapas Iniciais:
- Fiabilidade do Sistema a Longo Prazo:
- A CSA assegura:
- Adaptabilidade: Os sistemas evoluem sem comprometer a fiabilidade.
- Segurança: Proteção contra ameaças cibernéticas.
- Conformidade: Alinhamento contínuo com as regulamentações.
- Qualidade: Dados e qualidade do produto consistentes.
- A CSA assegura:
Como a CSA contribui para a integridade dos dados na indústria farmacêutica?
A CSA mantém a integridade dos dados na indústria farmacêutica, garantindo a precisão, consistência e fiabilidade dos dados ao longo do ciclo de vida de um sistema. Ao contrário das abordagens tradicionais, a CSA adota uma estratégia holística que se estende para além da validação, abordando ativamente potenciais desafios e discrepâncias que possam surgir ao longo do tempo.
Uma contribuição da CSA para a integridade dos dados reside nas suas capacidades de monitorização contínua. Em vez de depender apenas de esforços de validação periódicos, a CSA envolve análises de dados em tempo real e medidas proativas de gestão de risco. Esta abordagem permite às organizações detetar e resolver potenciais discrepâncias de dados, evitando que as imprecisões se acumulem ao longo do tempo. A ênfase da CSA num modelo de ciclo de vida dinâmico e adaptativo garante que a integridade dos dados permanece um foco constante, alinhando-se com as expectativas regulamentares.
Para evitar discrepâncias de dados ao longo do tempo, a CSA incorpora várias medidas estratégicas. Primeiramente, emprega processos robustos de controlo de alterações, documentando meticulosamente quaisquer modificações em sistemas ou processos informatizados que possam afetar a integridade dos dados. São realizadas auditorias e avaliações regulares dos sistemas para identificar e retificar potenciais problemas antes que estes se agravem. Além disso, a CSA enfatiza a importância de programas de formação e sensibilização dos utilizadores para garantir que o pessoal compreenda a importância de manter a integridade dos dados e adira às melhores práticas.
Em conclusão, a abordagem proativa e abrangente da CSA à integridade dos dados distingue-a como uma solução estratégica na indústria farmacêutica. Ao incorporar monitorização contínua, gestão de riscos e medidas rigorosas de controlo de alterações, a CSA mantém a integridade dos dados e garante que as empresas farmacêuticas estão bem preparadas para navegar no cenário em evolução das expectativas regulatórias. À medida que as organizações se esforçam para manter os mais altos padrões de integridade dos dados, a CSA surge como um aliado fundamental na sua jornada, alinhando-se com as tendências da indústria e os avanços regulatórios.
Para as organizações que procuram orientação sobre a implementação de estratégias CSA eficazes, a Freyr é um parceiro fiável que oferece soluções personalizadas para abordar os desafios únicos do panorama farmacêutico.
Que papel desempenha a conformidade regulamentar na CSA?
A conformidade regulatória é um pilar da CSA, garantindo que as empresas farmacêuticas aderem a padrões e diretrizes em evolução ao longo do ciclo de vida de um sistema. Ao contrário do foco tradicional da Validação de Sistemas Computorizados (CSV), a CSA enfatiza a conformidade contínua e a adaptabilidade aos cenários regulatórios em mudança. À medida que as empresas fazem a transição de CSV para CSA, manter-se atualizado sobre os regulamentos em evolução torna-se primordial.
No contexto da CSA, a conformidade regulamentar implica alinhar os sistemas informatizados com os requisitos regulamentares globais e locais, desde o desenvolvimento até à utilização operacional e eventual desativação. A CSA enfatiza a conformidade contínua em vez da validação periódica, promovendo uma abordagem proativa para abordar prontamente potenciais alterações regulamentares. Este alinhamento estratégico garante que as empresas farmacêuticas estão bem preparadas para cumprir as expectativas regulamentares, salvaguardando a integridade dos dados, a segurança do paciente e a fiabilidade geral do sistema.

O envolvimento regular com as autoridades regulamentares, a participação em fóruns da indústria e a subscrição de publicações regulamentares fornecem informações valiosas sobre padrões em evolução. Aproveitar a experiência de consultores regulamentares e investir em formação contínua para o pessoal envolvido nos processos CSA melhora ainda mais a sensibilização regulamentar. Colaborar com parceiros regulamentares, como a Freyr Solutions, oferece uma abordagem proativa, garantindo acesso a informações regulamentares atualizadas e soluções personalizadas para navegar na transição sem problemas.
A conformidade regulatória na CSA é um compromisso dinâmico e contínuo que se alinha com a mudança da indústria para a adaptabilidade e melhoria contínua. Manter-se informado, ser proativo e colaborar com especialistas regulatórios são cruciais para empresas em transição de CSV para CSA, facilitando uma evolução suave e em conformidade no cenário farmacêutico em constante mudança.
Como um parceiro de Regulamentação de confiança, a Freyr fornece o apoio e a experiência necessários para guiar as empresas através desta transição, garantindo a excelência e conformidade com a Regulamentação na era da CSA.
Como ajuda um parceiro estratégico de conformidade regulamentar?
Um parceiro estratégico de conformidade regulamentar desempenha um papel fundamental para garantir que as empresas farmacêuticas cumprem os requisitos regulamentares e mantêm elevados padrões de qualidade. Eis como podem ajudar:
- Orientação Especializada: Um parceiro estratégico fornece aconselhamento especializado sobre como navegar por regulamentações complexas e em evolução em diferentes regiões. Oferecem informações sobre as mais recentes alterações Regulatórias, ajudando as empresas a ajustar as suas práticas e a manter a conformidade.
- Processos Simplificados: Ajudam a simplificar os processos de conformidade através da implementação de melhores práticas e fluxos de trabalho eficientes. Isto inclui o desenvolvimento de sistemas robustos para documentação, auditoria e validação, reduzindo os encargos administrativos e melhorando a eficiência geral.
- Mitigação de Risco: Ao identificar potenciais riscos e vulnerabilidades de conformidade, um parceiro estratégico ajuda a mitigar os riscos antes que se tornem problemas. Realizam auditorias e avaliações rigorosas para garantir que todos os processos estão em conformidade e abordam proativamente quaisquer lacunas.
- Formação e Suporte: Oferecem formação e suporte para garantir que o pessoal está bem informado sobre os requisitos regulamentares e as melhores práticas. Isto ajuda a construir competência interna e garante que todos os envolvidos nas atividades de conformidade estão atualizados com os padrões atuais.
- Integração de Tecnologia: Um parceiro estratégico auxilia na integração de tecnologias inovadoras, como automação e IA, nos processos de conformidade. Garante que estas tecnologias são implementadas de forma eficaz e de acordo com os requisitos regulamentares, melhorando a integridade dos dados e a eficiência dos processos.
- Documentação e Manutenção de Registos: Gerem a criação, organização e manutenção de documentação de conformidade crucial. Isto garante que todos os registos são precisos, completos e facilmente acessíveis para auditorias e inspeções.
- Submissões e Aprovações Regulatórias: Tratam da preparação e submissão de documentos e submissões de Regulamentação. Isto inclui garantir que as submissões cumprem todos os requisitos necessários e gerir as comunicações com as autoridades de Regulamentação para facilitar aprovações atempadas.
- Ações Corretivas e Preventivas: Um parceiro estratégico apoia o desenvolvimento e a implementação de ações corretivas e preventivas em resposta a resultados de auditorias ou problemas de conformidade. Eles ajudam a garantir que estas ações são eficazes e não perturbam as operações em curso.
- Estratégia de Conformidade Global: Desenvolvem e implementam estratégias para alcançar a conformidade global, abordando os diversos requisitos regulamentares de diferentes mercados. Isto garante que os produtos cumprem todas as normas necessárias para distribuição e utilização internacionais.
- Monitorização Contínua: Oferecem monitorização e suporte contínuos para manter as empresas informadas sobre quaisquer atualizações ou alterações Regulamentares. Esta abordagem proativa ajuda as empresas a manterem-se em conformidade e a adaptarem-se a novas regulamentações à medida que surgem.
Porquê escolher a Freyr?
Mais de dez anos de excelência em conformidade regulamentar.
Espectro completo de conformidade, auditoria e validação.
Conhecimentos em diversas indústrias e geografias.
Utiliza ferramentas inovadoras para resultados precisos.
Profissionais qualificados com conhecimento aprofundado da indústria.
Gestão bem-sucedida de desafios complexos de conformidade.
Perguntas Frequentes
A conformidade farmacêutica implica a adesão a leis, regulamentos e diretrizes que regem a indústria farmacêutica. Garante que as empresas alinham as suas operações com os padrões da indústria, salvaguardando assim a segurança e a eficácia dos produtos, ao mesmo tempo que mantêm a integridade dos dados.
O objetivo de uma auditoria é avaliar sistematicamente a adesão de uma empresa às normas regulamentares e políticas internas. As auditorias ajudam a identificar áreas para melhoria, mitigar riscos e garantir que os processos são eficazes na produção de produtos farmacêuticos seguros e conformes.
A validação na indústria farmacêutica é o processo de confirmar que os sistemas, processos e equipamentos cumprem consistentemente os requisitos predefinidos. É essencial para garantir a conformidade com as normas regulamentares e para manter a qualidade e segurança dos produtos farmacêuticos ao longo do seu ciclo de vida.
Estes processos são críticos para garantir a segurança e eficácia do produto, manter a conformidade Regulamentar, melhorar a garantia de qualidade, apoiar o acesso ao mercado e facilitar a melhoria contínua. Ajudam as empresas a cumprir padrões rigorosos e a construir confiança com as partes interessadas.
Os desafios incluem lidar com regulamentações em constante evolução, garantir a integridade dos dados, gerir as restrições de recursos e manter a documentação adequada. Além disso, a integração de tecnologias inovadoras e a garantia da competência do pessoal podem complicar os esforços de conformidade.
As auditorias GxP são avaliações realizadas para garantir a adesão às normas de Boas Práticas (GxP), que incluem as Boas Práticas de Fabrico (BPF), as Boas Práticas Clínicas (BPC) e as Boas Práticas de Laboratório (BPL). Estas auditorias ajudam a identificar lacunas de conformidade e a melhorar os sistemas de qualidade.
Uma auditoria de conformidade GxP independente é uma avaliação objetiva da adesão de uma empresa aos padrões de qualidade e regulamentares. Realizada por auditores qualificados, identifica riscos e áreas para melhoria, melhorando a conformidade e a segurança do produto.
As auditorias GxP fornecem avaliações imparciais, melhoram a conformidade regulamentar e identificam áreas para melhoria operacional. Ajudam a manter padrões de alta qualidade e a construir confiança com reguladores e clientes.
A CSV assegura que os sistemas informatizados utilizados na indústria farmacêutica produzem consistentemente dados fiáveis e cumprem os requisitos regulamentares. É vital para manter a integridade dos dados, mitigar riscos e garantir a segurança do paciente ao longo do ciclo de vida do produto.
A CSV foca-se em validar que um sistema cumpre os requisitos regulamentares e funciona conforme o previsto, enquanto a CSA abrange uma abordagem mais ampla que inclui a garantia contínua do desempenho e conformidade do sistema ao longo do seu ciclo de vida.














