Serviços Globais de Rotulagem Regulamentar Farmacêutica
Aproveite uma década de experiência com os nossos serviços de Rotulagem Regulamentar, abrangendo autorizações de novos produtos, submissões a Autoridades de Saúde, pós-aprovações, CMC e gestão do ciclo de vida. O nosso foco na excelência global e local garante a criação e atualização estratégicas para documentos de rotulagem essenciais como IBs, CDS e CCDS, garantindo conformidade e sucesso na indústria farmacêutica.
Explorar Tópicos
- O que é a Rotulagem Regulamentar?
- Por que a Rotulagem Regulatória é Importante na Indústria Farmacêutica?
- Qual é o Processo de Aprovação de Rotulagem?
- Quais são os Desafios Comuns na Rotulagem Regulamentar?
- Quais são os principais regulamentos que regem a rotulagem farmacêutica?
- Como pode um parceiro regulamentar ajudar a alcançar a conformidade com os requisitos de rotulagem?
- Como Podem as Empresas Começar com os Serviços de Rotulagem Regulamentar?
- Podem os Serviços de Rotulagem Regulamentar Auxiliar na Monitorização Pós-comercialização?
- Porquê escolher a Freyr?
- Os Nossos Serviços
O que é a Rotulagem Regulamentar?
Última atualização em: agosto de 2024
A rotulagem regulamentar farmacêutica envolve a criação, revisão e gestão de documentos cruciais que comunicam informações essenciais do produto às partes interessadas, garantindo a conformidade com as normas regulamentares globais. Os componentes principais incluem a Core Data Sheet (CDS) e a Company Core Data Sheet (CCDS), derivados de fontes como Investigational Brochures e dados pós-comercialização. Este processo é fundamental para transmitir informações de segurança e eficácia em rótulos específicos de cada país e para alinhar com os requisitos da Autoridade de Saúde (HA).
Com foco na harmonização global, a rotulagem regulatória farmacêutica aborda as exigências regulatórias em evolução, abrangendo novas autorizações de produtos, submissões às HA, pós-aprovações e gestão do ciclo de vida. A precisão e a adesão às diretrizes em evolução são cruciais para uma rotulagem regulatória farmacêutica bem-sucedida, influenciando a autorização de mercado de um produto, o perfil de segurança e a viabilidade regulatória geral.

A Freyr, líder em serviços End-to-End de rotulagem regulamentar de medicamentos, orgulha-se de ter uma equipa dedicada de mais de 180 especialistas globais em rotulagem, destacando-se na elaboração de documentos cruciais como Brochuras do Investigador (IB), Folhas de Dados Essenciais de Desenvolvimento e Informações Essenciais de Segurança de Desenvolvimento. A utilização de inteligência artificial aumenta a precisão e acelera a implementação e revisão das folhas de dados. Com um modelo CCDS simplificado e processos orientados pela precisão, os serviços abrangentes da Freyr satisfazem eficazmente as necessidades dinâmicas da indústria farmacêutica, proporcionando um apoio inigualável para a conformidade da rotulagem e o sucesso regulamentar.
Por que a Rotulagem Regulatória é Importante na Indústria Farmacêutica?
- Garantir a Segurança do Paciente e a Comunicação de Informações: A rotulagem regulamentar é crucial para a segurança do paciente. Os rótulos fornecem informações essenciais sobre o uso do medicamento, dosagens, efeitos secundários e contraindicações. Pacientes, médicos prescritores, profissionais de saúde e cuidadores dependem destes rótulos para tomar decisões informadas. Uma rotulagem clara e precisa reduz o risco de erros de medicação, eventos adversos e uso indevido.
Garante que os pacientes recebem o tratamento correto e compreendem o seu uso adequado. Além disso, as autoridades regulamentares exigem que cada produto farmacêutico no mercado tenha rotulagem para comunicar eficazmente as informações de tratamento. - Conformidade e Mitigação de Riscos: A conformidade com os regulamentos de rotulagem não é apenas uma formalidade; é um requisito legal. Organismos reguladores como a US Food and Drug Administration (FDA), a Agência Europeia de Medicamentos (EMA) e outros exigem uma rotulagem precisa e abrangente. A não conformidade pode resultar em multas regulamentares, danos à reputação da marca e até mesmo paralisações temporárias da linha de produção. As empresas farmacêuticas devem demonstrar que os seus processos de rotulagem, métodos, testes e equipamentos são capazes de produzir consistentemente produtos seguros e eficazes. A rotulagem devidamente validada mitiga riscos e garante a adesão às boas práticas de fabrico (GMP).
- Acesso ao Mercado e Harmonização Global: Rótulos bem estruturados facilitam o acesso ao mercado global. A rotulagem consistente entre regiões simplifica os processos, reduz redundâncias e alinha-se com as normas harmonizadas. À medida que os reguladores internacionais adotam os requisitos de validação das BPF, incluindo a serialização, as cadeias de abastecimento farmacêuticas enfrentam uma complexidade crescente. As empresas que priorizam a conformidade da rotulagem estabelecem confiança, aumentam a aceitação no mercado e posicionam-se para o sucesso num cenário competitivo.
Qual é o Processo de Aprovação de Rotulagem?
O processo de aprovação da rotulagem na indústria farmacêutica envolve várias etapas para garantir que todas as informações relacionadas com o medicamento sejam precisas, conformes e claras tanto para os prestadores de cuidados de saúde como para os doentes. Começa com a elaboração do conteúdo do rótulo, que inclui detalhes sobre dosagem, administração, segurança e advertências. As equipas regulamentares e médicas reveem internamente este rascunho para garantir que está em conformidade com as normas regulamentares locais e internacionais. Uma vez finalizado, o rótulo é submetido às autoridades de saúde para aprovação, onde é submetido a um escrutínio rigoroso para verificar a sua conformidade com os requisitos de segurança e eficácia. Só após receber a aprovação oficial é que o rótulo pode ser utilizado na comercialização do medicamento.
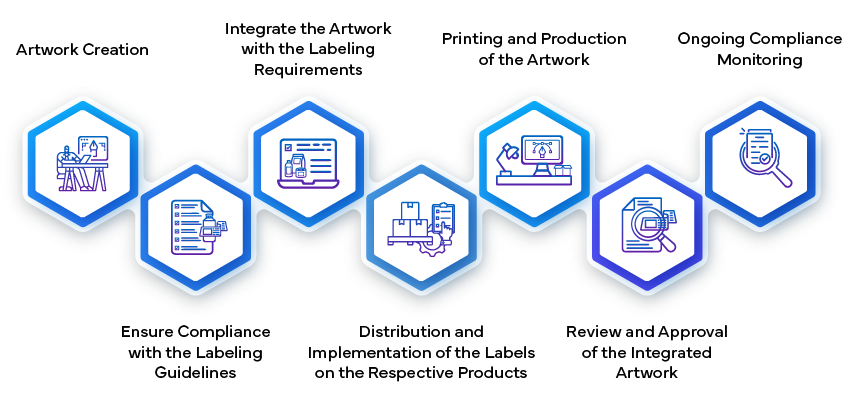
- Criação e Submissão do Rótulo:
- Recolha Inicial de Dados: As empresas farmacêuticas compilam todos os dados relevantes para o rótulo do medicamento. Isso inclui informações sobre eficácia, segurança, dosagens, indicações, contraindicações e riscos potenciais. O rótulo serve como uma ferramenta de comunicação crítica para profissionais de saúde e pacientes.
- Submissão às Autoridades Regulamentares: A empresa submete os dados do rótulo aos organismos regulamentares, como a US Food and Drug Administration (FDA) ou a European Medicines Agency (EMA). Estas agências avaliam os dados para garantir que o medicamento oferece benefícios que superam os seus riscos conhecidos e potenciais para a população-alvo.
- Análise Contextual: Os revisores analisam a condição ou doença alvo para a qual o medicamento se destina. Consideram o panorama de tratamento existente, ponderando os riscos do medicamento em relação aos seus benefícios. Por exemplo, um medicamento que trata uma doença com risco de vida sem terapia alternativa pode ser aprovado mesmo que os riscos fossem inaceitáveis para uma condição não fatal.
- Avaliação de Dados Clínicos: Os avaliadores da FDA analisam as informações sobre o benefício clínico e o risco submetidas pelo fabricante do medicamento. Eles consideram quaisquer incertezas decorrentes de dados imperfeitos ou incompletos. Tipicamente, a agência espera resultados de ensaios clínicos bem concebidos para validar a eficácia e segurança do medicamento.
- Definir o Artwork:
- Uma vez aprovado o conteúdo do rótulo, o próximo passo é criar o Artwork do rótulo. Isso envolve o design dos elementos visuais, layout, tipos de letra e gráficos. O Artwork deve estar em conformidade com as diretrizes regulamentares e representar com precisão as informações no rótulo.
- O Artwork do rótulo é submetido a revisões internas na empresa farmacêutica para garantir a consistência e a conformidade. Inclui detalhes como instruções de dosagem, avisos, condições de armazenamento e informações de contacto.
- O Artwork final é submetido às autoridades regulamentares para aprovação. Este passo garante que a apresentação visual do rótulo cumpre os padrões de qualidade e comunica eficazmente informações críticas aos utilizadores.
- Fabrico e Implementação:
- Uma vez aprovado, o Artwork do rótulo torna-se parte integrante da embalagem do medicamento. Os fabricantes garantem que os rótulos são corretamente afixados a cada unidade do produto (por exemplo, frascos, embalagens blister, ampolas).
- Os procedimentos de controlo de qualidade verificam se os rótulos cumprem as especificações, incluindo conteúdo preciso, legibilidade e adesão às diretrizes de design.
- O rótulo serve como uma ponte entre a empresa farmacêutica, as agências reguladoras, os prestadores de cuidados de saúde e os doentes. Desempenha um papel vital para garantir a utilização segura e eficaz da medicação ao longo do ciclo de vida do produto.
Quais são os Desafios Comuns na Rotulagem Regulamentar?
Os desafios comuns na rotulagem regulamentar incluem acompanhar os requisitos regulamentares em evolução, gerir a rotulagem multilingue e garantir a consistência em diversos portefólios de produtos. A natureza dinâmica das normas regulamentares para a rotulagem farmacêutica exige vigilância contínua para se manter atualizado com os requisitos mais recentes. Adaptar-se às regulamentações em mudança e implementar prontamente as atualizações necessárias ao conteúdo e formato da rotulagem é essencial para manter a conformidade e garantir a segurança do paciente.
| Desafio | Descrição |
|---|---|
| Requisitos Regulamentares em Evolução | Lidar com regulamentações e diretrizes em constante mudança, necessitando de atualizações constantes na documentação de rotulagem. |
| Harmonização Global | Garantir a consistência da informação do produto em diversas regiões, alinhando-se com os requisitos variados das diferentes autoridades de saúde. |
| Integração de Dados Pós-Comercialização | Gestão da incorporação de dados de segurança e eficácia pós-comercialização na rotulagem, mantendo a precisão e a relevância. |
| Conformidade com as Normas de Rotulagem Locais | Aderir a padrões de rotulagem específicos de cada país, abordando variações linguísticas, culturais e de formatação. |
| Gestão Eficiente de Alterações de Rotulagem | Simplificação dos processos para o acompanhamento, implementação e documentação de alterações na rotulagem de forma rápida e precisa. |
A rotulagem multilingue representa um desafio significativo para as empresas farmacêuticas que operam em mercados globais. Traduzir com precisão o conteúdo da rotulagem para várias línguas, ao mesmo tempo que se adere às nuances linguísticas e regulamentares regionais, exige atenção aos detalhes e processos robustos de gestão de tradução. Garantir a consistência e a clareza entre as diferentes versões linguísticas é crucial para comunicar eficazmente informações vitais a diversas populações de doentes.
Manter a consistência entre os portefólios de produtos apresenta outro desafio comum na rotulagem Regulamentar. As empresas farmacêuticas gerem frequentemente vários produtos com requisitos de rotulagem, formulações e indicações variáveis. Alcançar coerência e conformidade em diversas linhas de produtos, ao mesmo tempo que se cumprem as exigências Regulamentares específicas para cada produto, exige processos e sistemas eficientes para garantir a uniformidade no conteúdo, formato e mensagem da rotulagem.
Quais são os principais regulamentos que regem a rotulagem farmacêutica?
A rotulagem farmacêutica é regida por um conjunto complexo de regulamentos concebidos para garantir a segurança, a eficácia e a utilização correta dos medicamentos. Alguns deles estão listados abaixo:
US FDA (Administração de Alimentos e Medicamentos dos Estados Unidos)
A US FDA rege a rotulagem farmacêutica através de um conjunto rigoroso de regulamentos delineados no Código de Regulamentos Federais (CFR) Título 21. Estes regulamentos exigem que os rótulos forneçam informações abrangentes, incluindo indicações do medicamento, instruções de uso, contraindicações e potenciais efeitos secundários. A FDA enfatiza a importância de uma linguagem clara, precisa e inequívoca para garantir a segurança do paciente e a tomada de decisões informadas pelos profissionais de saúde. Além disso, os requisitos de rotulagem da FDA estendem-se a vários aspetos, como embalagens, folhetos e rotulagem eletrónica, garantindo que todas as informações são acessíveis e padronizadas em diferentes formatos. A conformidade com estes regulamentos é obrigatória para a aprovação de medicamentos e a presença contínua no mercado nos Estados Unidos.
EMA (Agência Europeia de Medicamentos)
A EMA supervisiona a rotulagem farmacêutica na EU (European Union) através de diretivas e orientações concebidas para harmonizar a rotulagem em todos os Member States. A Diretiva 2001/83/CE da Comissão Europeia é fundamental para estes esforços, especificando os requisitos para o Resumo das Características do Medicamento (SmPC), folhetos informativos para o paciente e rótulos das embalagens. A EMA garante que a rotulagem inclui informações essenciais tanto para profissionais de saúde como para pacientes, promovendo o uso seguro e eficaz de medicamentos em toda a EU (European Union). Além disso, a rotulagem deve estar disponível nas línguas oficiais dos Member States onde o medicamento é comercializado, refletindo o compromisso da EMA com a acessibilidade e os cuidados centrados no paciente.
TGA (Therapeutic Goods Administration)
Na Austrália, a TGA é responsável pela regulamentação da rotulagem farmacêutica ao abrigo da Lei de Produtos Terapêuticos de 1989. As diretrizes da TGA exigem que os rótulos dos medicamentos forneçam informações claras, precisas e abrangentes sobre o produto, incluindo os seus ingredientes, indicações, dosagem e riscos potenciais. Os requisitos de rotulagem são concebidos para proteger a saúde pública, garantindo que os consumidores e os profissionais de saúde tenham as informações necessárias para utilizar os medicamentos de forma segura e eficaz. A TGA também dá grande ênfase à legibilidade dos rótulos, exigindo que sejam escritos em inglês simples e que as informações críticas sejam exibidas de forma proeminente para evitar o uso indevido e erros de medicação.
Health Canada
A Health Canada regulamenta a rotulagem farmacêutica através de um quadro que prioriza a segurança e o bem-estar dos pacientes e profissionais de saúde. A Lei dos Alimentos e Medicamentos e os seus regulamentos associados descrevem os requisitos para os rótulos dos medicamentos, que devem incluir informações detalhadas sobre a composição do produto, indicações, contraindicações e potenciais efeitos secundários. A Health Canada também exige que os rótulos sejam bilingues, apresentados em inglês e francês, para acomodar a diversidade linguística do país. Além disso, a Health Canada atualiza regularmente os seus requisitos de rotulagem para refletir novas evidências científicas e as necessidades de saúde pública em evolução, garantindo que a rotulagem permanece relevante e eficaz na promoção do uso seguro de medicamentos.
PMDA (Pharmaceuticals and Medical Devices Agency)
A PMDA, autoridade regulamentar do Japão, supervisiona a rotulagem farmacêutica de acordo com a Lei dos Assuntos Farmacêuticos e as diretrizes relacionadas. A PMDA exige que os rótulos dos medicamentos forneçam informações abrangentes, incluindo indicações, instruções de dosagem e potenciais efeitos adversos, num formato facilmente compreendido tanto por profissionais de saúde como por pacientes. A PMDA também exige que os rótulos incluam avisos e precauções específicos para a população japonesa, considerando fatores como diferenças genéticas e práticas culturais. Esta abordagem garante que os medicamentos são utilizados de forma segura e eficaz no Japão, com uma rotulagem adaptada às necessidades únicas do mercado local.
NMPA (National Medical Products Administration)
Na China, a NMPA rege a rotulagem farmacêutica através de um quadro regulamentar que enfatiza a precisão, clareza e segurança. A Lei de Administração de Medicamentos da República Popular da China descreve os requisitos para os rótulos dos medicamentos, que devem incluir informações sobre as indicações, dosagem, contraindicações e potenciais efeitos secundários do medicamento. A NMPA também exige que a rotulagem seja apresentada em chinês simplificado para garantir a acessibilidade à população local. Além disso, a NMPA exige que os rótulos sejam submetidos a uma revisão rigorosa durante o processo de aprovação do medicamento para garantir a conformidade com as normas nacionais e proteger a saúde pública, prevenindo erros de medicação e uso indevido.
Como pode um parceiro regulamentar ajudar a alcançar a conformidade com os requisitos de rotulagem?
Um parceiro regulamentar é fundamental para alcançar a conformidade com os requisitos de rotulagem, oferecendo experiência especializada e suporte abrangente. Orientam as empresas através do complexo cenário regulamentar, garantindo que os materiais de rotulagem — incluindo embalagens, folhetos e rótulos eletrónicos — aderem aos requisitos específicos de diferentes autoridades de saúde, como a FDA dos US, EMA, TGA, Health Canada, PMDA e NMPA. Isto envolve compreender e aplicar os regulamentos mais recentes, que podem variar significativamente entre regiões, para garantir que todas as informações do produto são precisas, completas e conformes.
Além disso, um parceiro regulamentar ajuda a otimizar o processo de rotulagem ao fornecer serviços críticos como a criação, revisão e validação de conteúdo. Eles auxiliam na elaboração e revisão do conteúdo da rotulagem para se alinhar com os padrões regulamentares e garantir que todas as informações necessárias sejam incluídas, desde listas de ingredientes e instruções de uso até avisos de segurança e condições de armazenamento. Isto reduz o risco de erros e omissões que poderiam levar a atrasos regulamentares ou retiradas do mercado, acelerando o tempo de colocação no mercado de novos produtos.

Além disso, um parceiro regulamentar apoia as empresas na manutenção da conformidade contínua, monitorizando as atualizações regulamentares e implementando as alterações necessárias. Oferecem aconselhamento estratégico sobre a adaptação de rótulos a novas diretrizes ou requisitos de mercados emergentes, ajudando as empresas a evitar problemas de não conformidade e garantindo que os seus produtos permanecem em conformidade com os regulamentos atuais. Ao alavancar a sua experiência e mantendo-se a par das alterações regulamentares, um parceiro regulamentar ajuda as empresas a navegar no cenário dinâmico da rotulagem de forma eficiente e eficaz.
Como Podem as Empresas Começar com os Serviços de Rotulagem Regulamentar?
Para iniciar os serviços de rotulagem regulamentar, as empresas devem primeiro avaliar as suas necessidades específicas de rotulagem com base nos mercados-alvo e nos requisitos regulamentares. Em seguida, devem fazer parceria com um fornecedor de serviços regulamentares fiável com experiência em normas de rotulagem globais. Este fornecedor pode ajudar na elaboração, revisão e atualização dos rótulos para garantir a conformidade. Além disso, a implementação de um sistema centralizado de gestão de rotulagem ajuda a simplificar o processo, garantindo a consistência em todos os rótulos dos produtos. Auditorias e atualizações regulares são essenciais para manter os rótulos alinhados com as regulamentações em evolução.
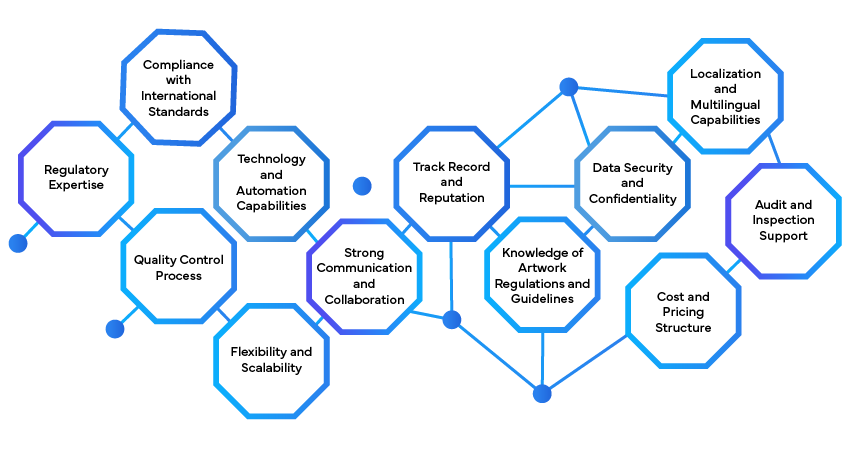
Avaliar as Necessidades Regulamentares:
- Identifique os requisitos regulamentares específicos aplicáveis ao seu produto e mercados-alvo.
- Compreender documentos críticos, como Fichas de Dados Essenciais (CDS), Brochuras do Investigador (IB) e requisitos de rotulagem locais.
Selecione um Parceiro de Rotulagem Regulatória:
- Pesquise e escolha um prestador de serviços de rotulagem regulamentar de confiança com experiência na sua indústria.
- Considerar fatores como a experiência, o conhecimento regulamentar global e a capacidade de lidar com diversos desafios de rotulagem.
Definir o Âmbito do Projeto:
- Delinear claramente o âmbito do seu projeto de rotulagem regulamentar, incluindo o tipo de serviços necessários (por exemplo, elaboração de IB, criação de CCDS, revisão de conformidade da rotulagem).
- Estabelecer prazos, marcos e entregáveis para cada fase do projeto.
Colaborar na Recolha de Dados:
- Colabore de perto com o seu parceiro de rotulagem regulamentar escolhido para recolher dados essenciais, incluindo informações de ensaios clínicos, dados de segurança e eficácia, e quaisquer dados de vigilância pós-comercialização.
Iniciar a Criação e Revisão de Documentos:
- Inicie a criação ou revisão de documentos cruciais como IBs, DCDS, CCDS e conteúdo de rotulagem local.
- Facilitar revisões regulares e sessões de feedback para garantir a precisão e o alinhamento com os requisitos regulamentares.
Implementar Processos de Controlo de Alterações:
- Desenvolver processos robustos de controlo de alterações para atualizações de rotulagem e acompanhar prontamente quaisquer modificações aos documentos essenciais.
- Garantir que as alterações são implementadas de forma consistente em rótulos globais e regionais.
Monitorizar a Conformidade:
- Estabelecer mecanismos para a monitorização contínua da conformidade com os padrões regulamentares em evolução.
- Mantenha-se informado sobre as alterações nos regulamentos e atualize os documentos de rotulagem em conformidade.
Utilizar Tecnologia e Automação:
- Utilizar software e tecnologia de rotulagem regulamentar para melhorar a precisão, a eficiência e a gestão de documentos.
- Explore ferramentas que suportam a inteligência artificial para otimizar a implementação de fichas de dados e os processos de revisão.
Envolver Especialistas de Regulamentação:
- Envolva especialistas ou consultores de regulamentação na sua organização ou através do seu fornecedor de serviços escolhido para fornecer informações e orientação durante todo o processo de rotulagem.
Melhoria Contínua:
- Estabelecer uma cultura de melhoria contínua, revendo e aprimorando regularmente os processos de rotulagem com base no feedback, nas mudanças da indústria e nos cenários regulamentares em evolução.
Podem os Serviços de Rotulagem Regulamentar Auxiliar na Monitorização Pós-comercialização?
Sim, os serviços de rotulagem regulamentar podem, de facto, auxiliar na monitorização pós-comercialização de produtos farmacêuticos. Estes serviços desempenham um papel crucial no apoio à vigilância pós-comercialização, ao facilitar a gestão de atualizações de rotulagem, o tratamento de alterações de rotulagem relacionadas com a segurança e a garantia de conformidade com os requisitos regulamentares pós-aprovação. Ao manter informações de rotulagem precisas e atualizadas, os serviços de rotulagem regulamentar ajudam as empresas farmacêuticas a responder a preocupações de segurança e a implementar atempadamente as alterações necessárias para apoiar a conformidade regulamentar contínua e a segurança do paciente.
Além disso, os serviços de rotulagem regulamentar podem auxiliar na disseminação eficiente de informações de segurança atualizadas para profissionais de saúde e pacientes. No caso de novas descobertas de segurança ou alterações nos perfis de risco de produtos farmacêuticos, os especialistas em rotulagem regulamentar podem ajudar a atualizar rapidamente o conteúdo da rotulagem para refletir os dados de segurança mais recentes e os requisitos regulamentares. Esta abordagem proativa à monitorização pós-comercialização e às atualizações de rotulagem apoia a comunicação atempada de informações de segurança importantes a prestadores de cuidados de saúde e pacientes, contribuindo para uma farmacovigilância e cuidados ao paciente aprimorados.
No geral, os serviços de rotulagem regulamentar fornecem um apoio valioso na monitorização pós-comercialização, ao garantir que os produtos farmacêuticos mantêm uma rotulagem precisa e em conformidade ao longo do seu ciclo de vida. Ao aproveitar a experiência de profissionais regulamentares e processos eficientes de gestão de rotulagem, as empresas podem abordar eficazmente as considerações de segurança pós-comercialização e as obrigações regulamentares, contribuindo assim para a segurança e eficácia contínuas dos seus produtos no mercado.
Porquê escolher a Freyr?
Uma década de excelência em rotulagem Regulamentar
Mais de 180 especialistas globais em serviços de rotulagem
Especializa-se na criação e gestão de documentos essenciais
Conhecimentos em Folhetos do Investigador, Fichas de Dados Essenciais e Fichas de Dados Essenciais da Empresa
Compromisso com a conformidade e precisão globais
Utiliza IA (Inteligência Artificial) para uma navegação regulamentar eficiente.
Estabeleça parceria connosco agora
Factos Rápidos
+
+
+
Perguntas Frequentes
As Core Data Sheets (CDS) fornecem um resumo consolidado de informações cruciais sobre medicamentos, incluindo indicações, dosagens e perfis de segurança. Garantem uma comunicação consistente de detalhes essenciais em todos os mercados globais, facilitando a conformidade regulamentar e a tomada de decisões informadas. As CDS também servem como referência para a criação de rótulos de produtos locais.
Os Investigational Brochures (IB) detalham os dados de ensaios clínicos e informações de desenvolvimento de medicamentos para uso em investigação, enquanto as Company Core Data Sheets (CCDS) resumem os principais dados de segurança e eficácia para fins regulamentares globais, orientando o conteúdo e as atualizações da rotulagem. As CCDS são utilizadas para criar rótulos específicos do produto para aprovação para comercialização.
A inteligência artificial melhora a rotulagem regulamentar ao automatizar a análise de dados, melhorar a precisão na criação de conteúdo e acelerar as revisões de documentos. As ferramentas de IA simplificam os processos de rotulagem e garantem a consistência em diversos requisitos regulamentares. Também ajudam a prever e a resolver potenciais problemas de conformidade.
A rotulagem multilingue garante que os produtos farmacêuticos são acessíveis a diversas populações de doentes, cumprindo os requisitos regulamentares regionais e melhorando a segurança ao fornecer instruções e avisos claros e compreensíveis em várias línguas. Isto reduz o risco de falhas de comunicação e erros na administração de medicamentos.
Um sistema centralizado de gestão de rotulagem coordena a criação, revisão e atualização de documentos de rotulagem, garantindo consistência e conformidade em todos os mercados globais. Otimiza os processos e mantém informações de produto precisas e atualizadas. Este sistema também apoia o tratamento eficiente de alterações de rotulagem e atualizações regulamentares.
Structured Product Labeling (SPL) é um formato baseado em XML utilizado para a rotulagem de medicamentos que padroniza e organiza as informações do produto. Garante consistência e facilita a troca de dados entre agências regulamentares e fabricantes. O SPL apoia a gestão eficiente das informações de rotulagem ao longo do ciclo de vida de um produto.
O Global Location Number (GLN) é um identificador único utilizado para identificar locais e entidades na cadeia de abastecimento. Ajuda a rastrear e gerir produtos farmacêuticos com precisão em mercados globais. Os GLNs garantem uma distribuição de produtos e uma gestão de inventário precisas e eficientes.
O National Drug Code (NDC) é um identificador único para medicamentos, atribuído pela FDA. Ajuda na identificação precisa de produtos farmacêuticos e facilita a gestão e o rastreamento de inventário. O NDC é crucial para a dispensa precisa de medicamentos e para a comunicação regulamentar.
Um Investigator's Brochure (IB) fornece informações detalhadas sobre dados clínicos e pré-clínicos de um medicamento em investigação. É utilizado para informar os investigadores de ensaios clínicos sobre a segurança, eficácia e dosagem do medicamento para fins de estudo. O IB também apoia a tomada de decisões éticas e informadas na investigação clínica.















