BIMO significa Bioresearch Monitoring, um programa de inspeção no local e auditorias de dados para monitorizar todos os aspetos da conduta e comunicação da investigação regulamentada pela US Food and Drug Administration (FDA). O programa foi estabelecido em 1977, após ter sido identificada a necessidade de auditar locais de investigação clínica. O principal objetivo deste programa é garantir a qualidade e integridade dos dados submetidos para aprovações de novos produtos e submissões de comercialização. Além disso, este programa também protege os direitos e o bem-estar de sujeitos humanos e animais envolvidos na investigação regulamentada pela FDA.
Os principais objetivos do Programa BIMO
Anualmente, são realizadas mais de 1000 inspeções. Os principais objetivos abrangidos pelo programa BIMO são:
- Auditar dados clínicos
- Inspeção de investigação clínica em curso
- Inspeção de laboratórios não clínicos
- Inspeção de Comités de Ética em Investigação (IRB)
Que produtos estão abrangidos pela Auditoria BIMO?
O BIMO é aplicável a Medicamentos, Produtos Biológicos, Dispositivos Médicos, Produtos Alimentares, Produtos de Tabaco e Produtos Veterinários. O programa de conformidade é supervisionado pelos seis (06) centros de produtos da FDA – Centro de Avaliação e Investigação de Produtos Biológicos (CBER), Centro de Dispositivos e Saúde Radiológica (CDRH), Centro de Avaliação e Investigação de Medicamentos (CDER), Centro de Segurança Alimentar e Nutrição Aplicada (CFSAN), Centro de Produtos de Tabaco (CTP) e Centro de Medicina Veterinária (CVM).
Que empresas estão sujeitas à Auditoria BIMO?
Tanto as empresas nacionais como as internacionais que realizam ou se enquadram em qualquer das atividades abaixo estão sujeitas aos requisitos de Monitorização de Biorinvestigação -
- Laboratórios de testes não clínicos para conformidade com as Boas Práticas de Laboratório (GLP)
- Investigadores clínicos para conformidade com as Boas Práticas Clínicas (GCP)
- Patrocinadores.
- Organizações de Investigação por Contrato (CROs)
- Monitores de ensaios clínicos
- Instalações de bioequivalência in vivo
- Comités de Ética em Investigação (IRBs)
Que programas de conformidade se enquadram no Programa BIMO?
A FDA dos US pode realizar uma auditoria BIMO a qualquer momento através dos sete (07) programas de conformidade multicêntricos. Estes sete programas de conformidade multicêntricos são implementados através de –
- Inspeção a Investigadores Clínicos (IC) e Investigadores Patrocinadores (IP)
- Inspeção do Comité de Ética em Investigação (IRB)
- Inspeção da Organização de Investigação por Contrato/Patrocinador/Monitor (CRO/S/M)
- Inspeção de Boas Práticas de Laboratório (GLP)
- Inspeção de Bioequivalência-Biodisponibilidade (BEQ)
- Inspeção de Notificação de Experiência Adversa a Medicamentos Pós-Comercialização (PADE)
- Inspeção de Relatórios da Estratégia de Avaliação e Mitigação de Risco (REMS)
Cada um destes programas descreve um âmbito detalhado de revisão ou inspeção a ser realizada para assegurar a conformidade com a FDA.
Que regulamentos são aplicáveis para a Auditoria BIMO?
Os regulamentos - 21 CFR 50 - Proteção de Sujeitos Humanos, 21 CFR 54 - Divulgação Financeira, 21 CFR 56 - IRBs, 21 CFR 58 - Boas Práticas de Laboratório para laboratórios não clínicos, 21 CFR 809 - Produtos de Diagnóstico In Vitro e 21 CFR 812 - Isenção para Dispositivos de Investigação são aplicáveis ao BIMO Audit.
Quantas auditorias são realizadas anualmente no âmbito do Programa BIMO?
O número de auditorias BIMO realizadas pela US FDA varia a cada ano. Nos últimos anos, o número de inspeções no local diminuiu devido ao início da pandemia de COVID-19, e a FDA teve de suspender toda a vigilância no local dos estudos clínicos. Apenas estudos clínicos específicos, críticos e cruciais estavam a ser monitorizados.
As “Avaliações Regulamentares Remotas” (RRAs) foram introduzidas durante a pandemia de COVID-19 para monitorizar remotamente a investigação regulamentada. As RRAs são realizadas através de videoconferências e são uma iniciativa voluntária para avaliar remotamente os dados e os processos. No entanto, o facto a ser notado aqui é que as RRAs não são equivalentes ou uma alternativa à inspeção no local, mas são meramente um procedimento que evoluiu devido à pandemia de COVID-19.
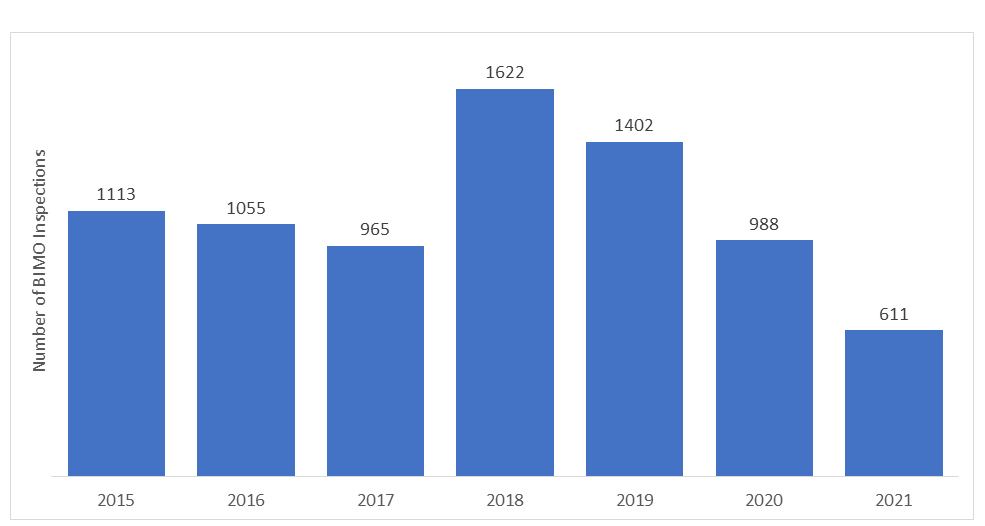
*Os dados representados para os anos de 2020 e 2021 não incluem inspeções RRA
Quantas Avaliações Regulamentares Remotas (RRAs) foram realizadas durante a Pandemia de COVID-19 no âmbito do Programa BIMO?
Em 2021, a adoção da inspeção RRA aumentou significativamente em todos os programas. Em abril de 2021, a FDA publicou um documento de orientação sobre “Avaliações Interativas Remotas de Instalações de Fabrico de Medicamentos e Monitorização de Biorinvestigação Durante a Emergência de Saúde Pública da COVID-19 – Orientação para a Indústria,” que fornece informações exaustivas sobre o processo da FDA para a realização de RRAs.
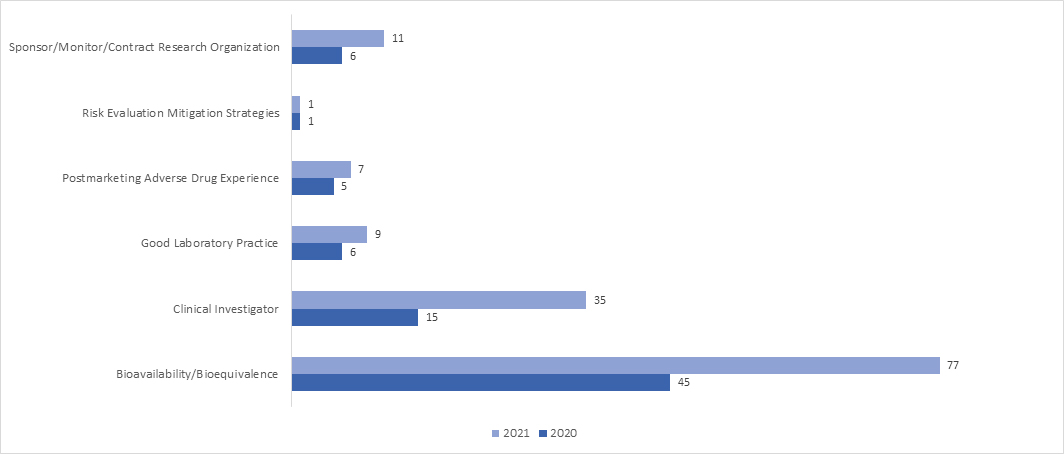
Quais são os possíveis resultados de uma Auditoria BIMO?
Durante a auditoria BIMO, a US FDA pode decidir tomar qualquer uma das ações listadas abaixo, com base na conformidade –
1. Nenhuma Ação Indicada (NAI)
O NAI é aplicável quando o inspetor de campo da FDA não identificou qualquer prática censurável ou apenas questões menores para as quais não se justifica uma ação adicional.
2. Ação Voluntária Indicada (VAI)
VAI é aplicável quando foram identificadas práticas censuráveis, mas não são significativas.
3. Ação Oficial Indicada (OAI)
O OAI é aplicável quando são identificadas práticas censuráveis que comprometem a integridade dos dados e/ou os direitos dos sujeitos humanos.
Quais são as não conformidades mais comuns emitidas no âmbito de uma Auditoria BIMO?
Algumas das não conformidades mais comuns observadas durante a Auditoria BIMO são –
- Não manter um controlo adequado dos registos
- Falha em relação ao plano de investigação
- Incumprimento dos regulamentos
- Falha na monitorização dos protocolos
- Proteção inadequada do sujeito
- Falta de responsabilização adequada pelo produto que está a ser investigado
A auditoria BIMO é crucial para qualquer desenvolvedor ou fabricante de novos dispositivos e tecnologias médicas que planeia lançar o seu dispositivo no mercado dos US. É muito importante cumprir os regulamentos e diretrizes para evitar qualquer uma das armadilhas descritas.
Precisa de alguma assistência relativamente às inspeções de auditoria BIMO? Contacte a Freyr. Mantenha-se informado. Mantenha-se em conformidade.