
Die Vielfalt der Arzneimitteltherapien ist groß: Medikamente können entweder in Kombination mit einem bereits zugelassenen Präparat eingesetzt oder als zwei neue Medikamente gleichzeitig entwickelt werden, um ihre Wirksamkeit synergistisch zu steigern. Krebstherapien mit nur einem Medikament haben deutlich gezeigt, dass Medikamentenresistenz eine große Bedrohung für Patienten darstellt, die mit Krebsmedikamenten behandelt werden. Angesichts der Vielfalt der bei Krebstherapien eingesetzten Kombinationstherapien ersetzen Zweifach-Medikamentenschemata schrittweise die Monotherapie als Standardbehandlung bei Patienten. Im Laufe des Jahrzehnts hat die Kombinationstherapie bessere Behandlungsmöglichkeiten eröffnet.
Wenn Sie ein Unternehmen sind, das sich des Paradigmenwechsels in der Entwicklung von Krebsmedikamenten von der Einzelwirkstoffentwicklung zu neuartigen Kombinationen bewusst ist, müssen Sie wissen, dass dieser Fortschritt zu vermehrten Anträgen auf Genehmigung von Cross-Labeling-Anfragen durch den Antragsteller geführt hat. Durch die Berücksichtigung von Diskussionen, den neuesten Branchentrends und dem aktuellen Verständnis der Anforderungen eines Sponsors hat die US Food and Drug Administration (USFDA) eine Reihe von Leitlinien erlassen, um Unterstützung bei Etikettierungsänderungen für Arzneimittelregime mit zuvor zugelassenen Arzneimitteln zu bieten.
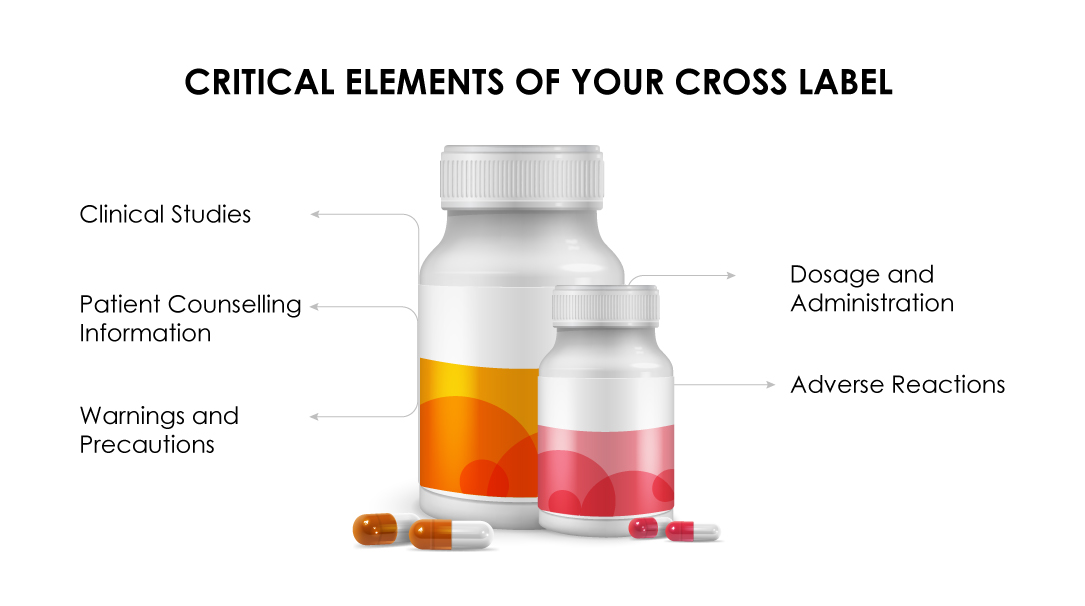
Herzlichen Glückwunsch! Ihr Antrag auf Leitlinien zur Kreuzkennzeichnung wurde genehmigt, wenn:
(a) Die Indikation für das beantragte Kombinationsschema unter einer ähnlichen Arzneimittelindikation zugelassen ist.
(b) Der Abschnitt Dosierung und Art der Anwendung muss die empfohlene Dosierung für das Arzneimittel des Sponsors in einem Kombinationsschema hervorheben.
(c) Die Daten der klinischen Studie müssen den Nutzen der Kombination für alle Medikamente im Schema begründen.
(d) Im Abschnitt „Warnhinweise und Vorsichtsmaßnahmen“ muss die Einzigartigkeit der Kombinationsbehandlung auf der Grundlage klinisch relevanter Daten dargelegt werden.
(e) Die Nebenwirkungen müssen so hervorgehoben werden, wie sie in den klinischen Studien beobachtet wurden.
(f) Die Patienteninformationsbroschüre muss sich auf die für die jeweilige Darreichungsform spezifischen Nebenwirkungen beschränken.
Informationen, die sich ausschließlich auf das Arzneimittel des Sponsors beziehen, müssen die übrigen Abschnitte der Kennzeichnung ausfüllen, es sei denn, es müssen spezifische pharmakokinetische Faktoren erwähnt werden.
Die genehmigte Leitlinie zur Kreuzkennzeichnung richtet sich speziell an Produkte für die Krebstherapie, um ein grundlegendes Verständnis der Kreuzkennzeichnung zu vermitteln. Um Sponsoren bei operativen und regulatorischen Hindernissen bezüglich der Kennzeichnungsänderung zu unterstützen, besagt die Leitlinie:
- Fristen
Die Antragsteller sollen den Entwurf des Inhalts für die Cross-Labeling mit einer evidenzbasierten Begründung der Rolle jedes im Therapieschema genannten Produkts in ihrem Vorschlag für die Cross-Labeling eines neuen Krebsmedikaments in einem Prä-NDA- oder BLA-Antrag vorlegen.
Es wird erwartet, dass die Kreuzkennzeichnung für jedes Arzneimittel im Schema gleichzeitig festgelegt wird. Die Genehmigung kann jedoch aufgrund unterschiedlicher Zeitpläne der Arzneimittel nacheinander erteilt werden.
- Regulatorische Einreichung
Jeder Antragsteller, der eine Kreuzkennzeichnung beantragt, muss diese über einen Originalantrag oder eine Wirksamkeits-Ergänzung für die Kreuzkennzeichnung einreichen.
Ein Antragsteller kann sich dafür entscheiden, Daten aus anderen Anträgen heranzuziehen, um die synergetischen Vorteile des Kombinationsschemas zu begründen.
Bei der Bezugnahme auf Daten hat der Antragsteller:
- muss sicherstellen, dass die referenzierten Daten bereits bei der FDA eingereicht wurden.
- jeden Abschnitt der Daten des Antragstellers, auf den verwiesen wird, mit Anmerkungen versehen.
- sollte (im folgenden Abschnitt) nur Informationen enthalten, die für das Arzneimittel des Antragstellers relevant sind:
- KASTENWARNUNG (Falls zutreffend)
- DARREICHUNGSFORMEN UND STÄRKEN
- KONTRAINDIKATIONEN
- Wechselwirkungen mit anderen Arzneimitteln
- ANWENDUNG BEI BESTIMMTEN PATIENTENGRUPPEN
- ÜBERDOSIERUNG
- BESCHREIBUNG
- KLINISCHE PHARMAKOLOGIE
- NICHTKLINISCHE TOXIKOLOGIE
- QUELLENANGABEN
- DARREICHUNGSFORM, PACKUNGSGRÖSSEN, LAGERUNG UND HANDHABUNG
Cross-Labeling für Krebsmedikamente kann dazu beitragen, Patienten über Dosierung, Wirksamkeit und Vorteile der Behandlungsergebnisse aufzuklären. Angesichts des exponentiellen Anstiegs der Kombinationstherapie als Standardmethode können Cross-Labels bei der Verbesserung oder Einführung bestehender therapeutischer Methoden von Vorteil sein. Unsere erfahrenen Experten bei Freyr sind bestens mit dynamischen Kennzeichnungsherausforderungen vertraut und können Lösungen für Ihre Kennzeichnungsfragen anbieten. Erleben Sie professionelle Kennzeichnungsunterstützung von höchster Qualität. Kontaktieren Sie Freyr!










