
Die Medizinprodukte-Verordnung (MDR) der Europäischen Union (EU) sorgt schon seit einiger Zeit für Schlagzeilen. Die MDR hat die Medizinprodukterichtlinie (MDD) und die Richtlinie über aktive implantierbare medizinische Geräte (AIMDD) ersetzt. Ursprünglich sollte der gesamte Übergang bis Mai 2020 vollständig in Kraft treten; doch aufgrund des Ausbruchs der COVID-19-Pandemie wurde die Umsetzung auf den 26. Mai 2021 verschoben. Innerhalb dieses Zeitrahmens werden bis zum 26. Mai 2024 alle MDD-Zertifikate ungültig, und die Produkthersteller müssen der EU MDR entsprechen. Des Weiteren dürfen MDD-Produkte, die vor dem 26. Mai 2020 gemäß den Richtlinien 90/385/EWG und 93/42/EWG rechtmäßig in Verkehr gebracht wurden, und Produkte, die ab dem 26. Mai 2020 aufgrund eines Zertifikats in Verkehr gebracht wurden, weiterhin bis zum 27. Mai 2025 auf dem Markt bereitgestellt werden. Die Zeitpläne sind unten dargestellt –
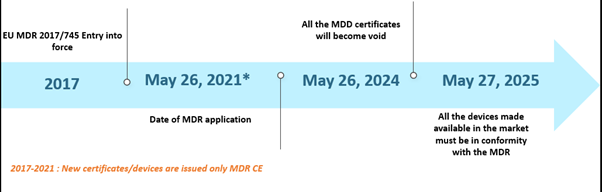
Vergangene Szenarien der EU MDR-Fristen
Allerdings stellten die begrenzte Kapazität der Benannten Stellen (BS) und die mangelnde Vorbereitung der Hersteller einige Herausforderungen bei der Umsetzung der MDR gemäß dem vorgegebenen Zeitplan dar. Stand Oktober 2022 gibt es insgesamt achtunddreißig (38) Benannte Stellen (BS), und diese BS erhielten etwa 8120 Anträge für die EU MDR-Zertifizierung, wovon 1990 Zertifikate ausgestellt wurden. Nach ihren Schätzungen mit dem ursprünglichen Zeitplan konnten nur 7000 Zertifikate bearbeitet werden, was zu einer weiteren Fristverlängerung führte. Darüber hinaus war ein weiterer wahrscheinlicher Grund für die Verlängerung die Sicherstellung der weiteren Verfügbarkeit sicherer Medizinprodukte, deren Zertifikate bereits abgelaufen sind oder vor dem 26. Mai 2024 ablaufen werden. Das aktuelle Szenario für die verlängerte Frist ist unten dargestellt-
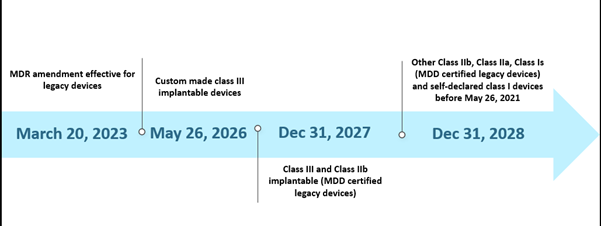
Vergangene Szenarien der EU MDR-Fristen
Die neue Verlängerung gilt für Bestandsgeräte, die Artikel 120 (3e) erfüllen und zum 20. März 2023 eine gültige MDD-CE-Kennzeichnung oder Ausnahmeregelung besaßen. Diese Geräte werden zusammen mit den MDR-CE-gekennzeichneten Geräten auf dem Markt bleiben. Bis zum 26. Mai 2024 sollten Hersteller von Bestandsgeräten ein implementiertes Qualitätsmanagementsystem (QMS) eingerichtet und einen Antrag bei einer MDR-benannten Stelle (NB) für die Konformitätsbewertung eingereicht haben. Bis zum 26. September 2024 sollten Hersteller von Bestandsgeräten eine Vereinbarung mit einer MDR-benannten Stelle (NB) getroffen haben.
Betrachten wir nun die Auswirkungen, die diese Verlängerung für die Hersteller haben könnte.
Chancen, die Hersteller durch diese Verlängerung haben:
- Verlängerter Marktzugang für MDD-/AIMDD-zertifizierte Produkthersteller, die bereits Initiativen zur MDR-Konformität ergriffen haben.
- Die MDR-zertifizierten Hersteller, deren MDD-/AIMDD-CE-Zertifikate nicht widerrufen wurden, dürfen Bestandsgeräte zusätzlich zu ihren MDR-konformen Geräten bis zum Ende der Übergangsfrist auf dem Markt bereitstellen.
- Hersteller, die zum 20. März 2023 eine nationale Ausnahmeregelung besitzen, können von der Übergangsfrist profitieren.
- Die Verlängerungsfrist verschafft mehr Zeit für ein besseres Verständnis der Regeln und Vorschriften, was dazu beiträgt, den Prozess zu optimieren und die MDR-Konformität zu erreichen.
Herausforderungen, die sich für Hersteller durch diese Verlängerung ergeben könnten:
- Es gibt keinen Marktvorteil für Hersteller von Altprodukten, die der MDR nicht entsprechen wollten.
- Die MDR-Verlängerung kann dazu führen, dass sich Zertifizierungsprozesse in die Länge ziehen und Produktneueinführungen verzögert werden, was eine direkte Folge des Rückstands bei den Überprüfungen durch die benannten Stellen (NBs) ist.
Welche Maßnahmen sollten Hersteller ergreifen?
- Es ist unerlässlich, dass die Hersteller die MDR-Risikoklasse ihres Medizinprodukts bestimmen, um den geeigneten Übergangszeitplan gemäß den geänderten MDR-Vorschriften zeitnah zu ermitteln.
- Um die Einhaltung der MDR-Vorschriften zu gewährleisten, ist es entscheidend, die MDR-benannten Stellen (NBs) zu identifizieren und Kontakt mit ihnen aufzunehmen, die über die spezifische Kompetenz für die Klassifizierung Ihres Medizinprodukts verfügen.
- Es ist entscheidend, eine umfassende Lückenanalyse für Ihr unter der MDD/AIMDD zertifiziertes Medizinprodukt durchzuführen, jegliche Nichtkonformitäten mit den MDR-Vorschriften zu identifizieren und zu beheben sowie die rechtzeitige Einhaltung sicherzustellen.
Für Hersteller ist es unerlässlich, sofort Maßnahmen zu ergreifen, um die Einhaltung der MDR zu gewährleisten. Die verlängerte Frist bietet Herstellern einige Möglichkeiten, die MDR-Konformität zu erreichen, birgt aber auch Herausforderungen, wie verzögerte Zertifizierungsprozesse und die Kosten der Konformität. Um diese Herausforderungen zu meistern und die Chancen zu nutzen, lassen Sie sich von unserem Expertenteam durch den MDR-Konformitätsprozess begleiten und Ihren Erfolg in diesem anspruchsvollen regulatorischen Umfeld sichern. Vereinbaren Sie noch heute einen Termin mit uns, um mehr darüber zu erfahren, wie wir Ihnen helfen können, die MDR-Konformität zu erreichen und der Konkurrenz einen Schritt voraus zu sein. Bleiben Sie informiert. Bleiben Sie konform.









