
Welche Rolle spielt Cybersicherheit bei Medizinprodukten?
Der 510(k)-Zulassungsprozess ist ein regulatorischer Weg, der von der US FDA (United States Food and Drug Administration) genutzt wird, um die kommerzielle Verbreitung von Medizinprodukten zu bewerten und freizugeben. Der Prozess zielt darauf ab, sicherzustellen, dass Medizinprodukte für den Gebrauch durch Patienten sicher und wirksam sind. Die US FDA definiert Cybersicherheit als „den Prozess der Verhinderung von unbefugtem Zugriff, Änderung, Missbrauch oder Nutzungsverweigerung oder der unbefugten Nutzung von Informationen, die von einem Medizinprodukt gespeichert, abgerufen oder an einen externen Empfänger übertragen werden.“
Medizinprodukte werden zunehmend mit Netzwerken verbunden und sind daher anfällig für Cybersicherheitsbedrohungen wie Hacking, Datenlecks und Malware-Angriffe. Die Berücksichtigung von Cybersicherheit bereits in der Design- und Entwicklungsphase ist entscheidend, um sicherzustellen, dass Medizinprodukte über angemessene Sicherheitskontrollen verfügen. Bedrohungen und Schwachstellen können nicht vollständig beseitigt werden, und die Reduzierung von Cybersicherheitsrisiken ist besonders anspruchsvoll. Wird die Cybersicherheit nicht ordnungsgemäß aufrechterhalten, kann dies zu einer beeinträchtigten Funktionalität der Geräte, zum Verlust persönlicher oder medizinischer Daten und zur Ausbreitung von Sicherheitsbedrohungen auf andere vernetzte Netzwerke oder Geräte führen.
Vorfälle durch beeinträchtigte Cybersicherheit
Cybersicherheitsvorfälle haben dazu geführt, dass Medizinprodukte und Krankenhausnetzwerke funktionsunfähig wurden, was die Patientenversorgung in Gesundheitseinrichtungen in den US gestört hat. Solche Cyberangriffe und Exploits können auch zu Patientenschäden aufgrund klinischer Gefahren führen, beispielsweise einer Verzögerung bei der Diagnose und/oder Behandlung von Patienten.
Nachfolgend sind die wichtigsten Vorfälle im gesamten Gesundheitswesen aufgeführt, die die Bedeutung der Cybersicherheit für die Patientensicherheit unterstreichen.
- Im Jahr 2017 betraf der WannaCry-Ransomware-Angriff Krankenhaussysteme und Medizinprodukte weltweit.
- Im Jahr 2020 verdeutlichte ein Ransomware-Angriff auf ein deutsches Krankenhaus die potenziellen dreiundachtzig (83) Auswirkungen einer verzögerten Patientenversorgung, da der Angriff Patienten dazu zwang, in ein anderes Krankenhaus verlegt zu werden.
Die wichtigsten Cybersicherheitsaspekte für die 510(k)-Zulassung
Nach der US FDA-Leitlinie zur Cybersicherheit, die speziell für Prämarkt-Einreichungen gilt, sind dies die allgemeinen Prinzipien der Cybersicherheit für Hersteller von Medizinprodukten.
- Qualitätssystem-Verordnung (QSR).: Hersteller sollten Cybersicherheitsprobleme bereits in der Design- und Entwicklungsphase des Medizinprodukts berücksichtigen, da dies zu einer robusteren und effizienteren Minderung von Patientenrisiken führen kann. Hersteller sollten Cybersicherheits-bezogene Design-Inputs für ihr Produkt festlegen sowie einen Ansatz zur Verwaltung von Cybersicherheitslücken und -risiken als Teil der Softwarevalidierung und Risikoanalyse, die gemäß 21 CFR 820.30(g) erforderlich ist.
- Designsicherheit: Hersteller von Medizinprodukten müssen sicherstellen, dass ihre Produkte unter Berücksichtigung der Gerätesicherheit entwickelt werden. Die US FDA bewertet die Angemessenheit der Sicherheit, basierend auf der Fähigkeit des Produkts, Sicherheitsziele wie Authentizität, Autorisierung, Verfügbarkeit, Vertraulichkeit und Sicherheit sowie zeitnahe Aktualisierbarkeit innerhalb der gesamten Systemarchitektur bereitzustellen und umzusetzen.
- Transparenz: Ein Mangel an Cybersicherheitsinformationen über das Gerät, wie z. B. Informationen, die für die Integration des Geräts in die Nutzungsumgebung erforderlich sind, sowie Informationen, die Benutzer benötigen, um die Cybersicherheit über den gesamten Lebenszyklus des Geräts aufrechtzuerhalten, kann dessen Sicherheit und Wirksamkeit beeinträchtigen. Um diesen Bedenken zu begegnen, ist es wichtig, dass Gerätebenutzer Zugang zu Informationen über Cybersicherheitskontrollen, potenzielle Risiken und andere relevante Informationen haben.
- Einreichungsdokumentation: Das Cybersicherheitsdesign und die Dokumentation eines Geräts sollten dem Cybersicherheitsrisiko des Geräts entsprechen. Hersteller sollten das größere System berücksichtigen, in dem ein Gerät verwendet werden kann.
Abbildung 1: Häufige Cybersicherheitsherausforderungen und -lösungen 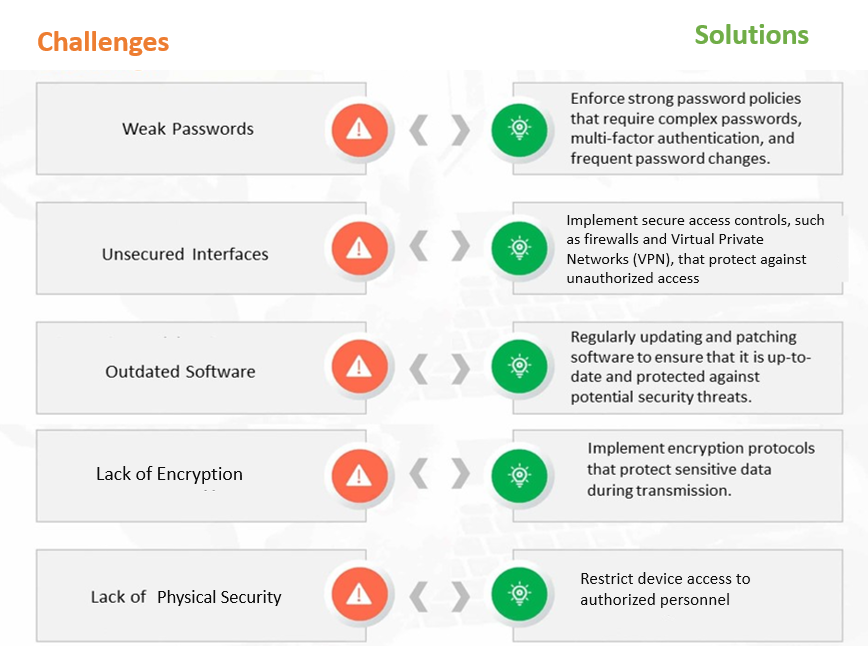
Fazit
Zusammenfassend lässt sich sagen, dass Cybersicherheit bei Medizinprodukten entscheidend ist, um die Patientensicherheit zu gewährleisten und Vorfälle zu verhindern, die die Gesundheitsversorgung stören könnten. Die Cybersicherheitsvorschriften der US FDA betonen die Notwendigkeit für Hersteller, Cybersicherheitsprobleme während des Designs und der Entwicklung von Medizinprodukten anzugehen und transparente Informationen über Cybersicherheitskontrollen bereitzustellen. Die QSR, Design-Sicherheit, Transparenz und Einreichungsdokumentation sind wichtige Überlegungen für die 510(k)-Zulassung. Es ist auch wichtig, gängige Cybersicherheitsherausforderungen wie Schwachstellen in Drittanbieterkomponenten und Ransomware-Angriffe anzugehen und Lösungen wie eine robuste Risikoanalyse und regelmäßige Software-Updates zu implementieren.
Um einen reibungslosen und konformen 510(k)-Zulassungsprozess zu erleben, kontaktieren Sie unsere Regulierungsexperten. Bleiben Sie informiert! Bleiben Sie konform!









