
Ein Qualitätsmanagementsystem (QMS) ist ein wesentlicher Bestandteil der Medizinprodukteindustrie, das die Sicherheit, Wirksamkeit und regulatorische Konformität von Medizinprodukten über ihren gesamten Lebenszyklus hinweg gewährleistet. Das QMS wird in allen Phasen des Lebenszyklus von Medizinprodukten implementiert, einschließlich der Design- und Entwicklungsphase, um sicherzustellen, dass das Produkt die regulatorischen Anforderungen und Benutzeranforderungen erfüllt und dass potenzielle Risiken identifiziert und behoben werden.
Abbildung 1 – Phasen des Lebenszyklus von Medizinprodukten
In diesem Blogbeitrag werden wir die Bedeutung von QMS in der Design- und Entwicklungsphase des Lebenszyklus von Medizinprodukten erörtern.
Design- und Entwicklungsphase im Lebenszyklus von Medizinprodukten
Die Design- und Entwicklungsphase ist eine der kritischsten Phasen im Lebenszyklus eines Medizinprodukts. In dieser Phase wird das Design des Produkts entwickelt und Prototypen erstellt, gefolgt von Verifizierungs- und Validierungstests als Teil des Lebenszyklus von Medizinprodukten.
Um sicherzustellen, dass das Medizinprodukt die regulatorischen Anforderungen, die Sicherheit, die Wirksamkeit und die Erwartungen der Anwender erfüllt, ist die Implementierung eines Qualitätsmanagementsystems (QMS) in der Design- und Entwicklungsphase des Lebenszyklus eines Medizinprodukts unerlässlich.
Die Dokumentation ist während der Entwurfs- und Entwicklungsphase von Medizinprodukten entscheidend. Das QMS stellt sicher, dass alle Dokumentationen bezüglich Entwurf und Entwicklung kontrolliert, verwaltet und dokumentiert werden.
Die Design History File (DHF) ist eine wichtige Akte/Aufzeichnung, die alle Dokumentationen zum Design und zur Entwicklung des Produkts enthält. Die DHF liefert den Nachweis, dass das Produktdesign die regulatorischen Anforderungen erfüllt.
Die DHF sollte Dokumente zu Design-Inputs, Design-Outputs, Design-Reviews, Design-Verifizierung, Validierung, Änderungen am Design und Risikomanagement enthalten. Erfahren Sie hier mehr über die DHF.
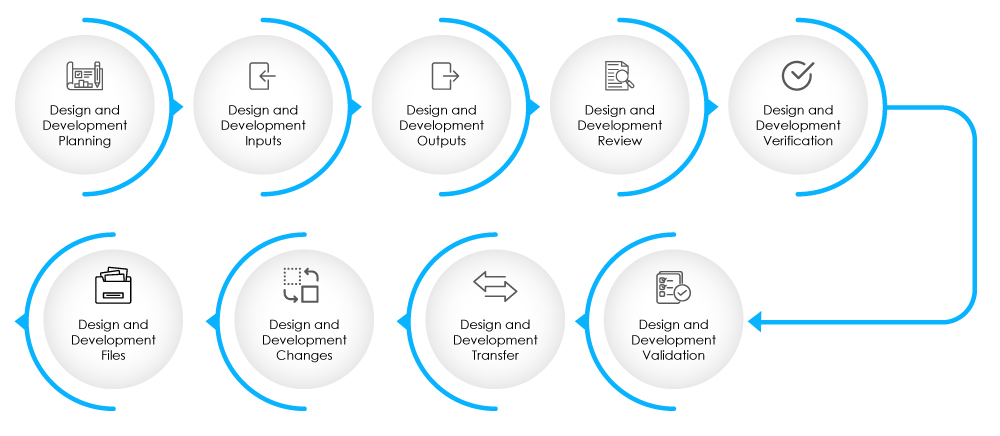
Abb. 2 – Phasen der Entwurfs- und Entwicklungsphase
Bewährte Verfahren für die Entwurfs- und Entwicklungsphase
- Einen strukturierten Ansatz etablieren: Entwickeln Sie einen strukturierten Ansatz für die Entwicklung und Verwaltung der DHF, der auf die spezifischen Bedürfnisse Ihres Unternehmens zugeschnitten ist. Dieser Ansatz sollte klare Richtlinien, Verfahren und Arbeitsabläufe für die Entwicklung und Verwaltung der DHF umfassen.
- Design-Inputs definieren und dokumentieren: Definieren und dokumentieren Sie die Design-Inputs klar, einschließlich der Anforderungen und Spezifikationen für das Gerät. Dies kann dazu beitragen, dass die DHF umfassend und vollständig ist.
- Designänderungen verwalten: Implementieren Sie einen robusten Änderungsmanagementprozess, der Verfahren zur Dokumentation, Bewertung und Genehmigung von Designänderungen umfasst. Dies kann dazu beitragen, dass Änderungen ordnungsgemäß dokumentiert und hinsichtlich ihrer Auswirkungen auf die Sicherheit und Wirksamkeit des Geräts bewertet werden.
- Rückverfolgbarkeit sicherstellen: Entwickeln Sie eine Rückverfolgbarkeitsmatrix, die die Design-Inputs mit den Design-Outputs verknüpft, und stellen Sie sicher, dass alle Design- und Entwicklungsaktivitäten ordnungsgemäß dokumentiert und erfasst werden. Dies kann dazu beitragen, dass die DHF rückverfolgbar ist und der Entscheidungsprozess gut dokumentiert ist.
- Innovation und Compliance in Einklang bringen: Entwickeln Sie eine Innovationskultur und stellen Sie gleichzeitig sicher, dass die Compliance-Anforderungen in Bezug auf die DHF, wie Designkontrollen und Risikomanagement, erfüllt werden. Dies kann durch die Entwicklung von Verfahren und Arbeitsabläufen erreicht werden, die Innovationen fördern und gleichzeitig die Einhaltung regulatorischer Anforderungen gewährleisten.
- Dokumentenkontrolle implementieren: Implementieren Sie Dokumentenkontrollverfahren, die sicherstellen, dass die DHF-Dokumente ordnungsgemäß kontrolliert, versionskontrolliert und für autorisiertes Personal zugänglich sind. Dies kann dazu beitragen, dass DHF-Dokumente sicher sind und Änderungen ordnungsgemäß dokumentiert und genehmigt werden.
- Team schulen: Stellen Sie sicher, dass das für die Entwicklung und Verwaltung der DHF zuständige Team angemessen zu den DHF-Anforderungen geschult ist und über die technische Expertise zur Produktentwicklung verfügt. Dies kann durch regelmäßige Schulungen, Mentoring und die Einstellung erfahrener Fachkräfte mit den erforderlichen Fähigkeiten und Kenntnissen erreicht werden.
Durch die Befolgung dieser bewährten Verfahren kann die Medizinprodukteindustrie die Einhaltung der regulatorischen Anforderungen sicherstellen, die Sicherheit und Wirksamkeit ihrer Produkte fördern und ihren Wettbewerbsvorteil auf dem Markt erhalten.
Zusammenfassend lässt sich sagen, dass die Implementierung eines QMS ab der Design- und Entwicklungsphase entscheidend für den Erfolg in der stark regulierten Medizinprodukteindustrie ist. Durch die Führung systematischer Aufzeichnungen und die Einhaltung der regulatorischen Anforderungen kann die Medizinprodukteindustrie sicherstellen, dass sie qualitativ hochwertige Produkte liefert und die Kundenzufriedenheit aufrechterhält.
Freyr bietet QMS-Dienstleistungen an, um der Medizinprodukteindustrie dabei zu helfen, die regulatorischen Anforderungen in allen Phasen des Lebenszyklus von Medizinprodukten zu erfüllen. Kontaktieren Sie unsere QMS- und Regulierungsexperten, um mehr zu erfahren.









