
Etykietowanie produktów farmaceutycznych jest jednym z najdokładniej kontrolowanych aspektów zgodności z przepisami. Nawet najmniejszy błąd może mieć poważne konsekwencje zarówno dla bezpieczeństwa pacjentów, jak i dla reputacji firmy. Proszę zwrócić uwagę na poniższe ustalenia:
- 20% firm farmaceutycznych i producentów urządzeń medycznych co miesiąc zgłasza problemy związane z kontrolą jakości w zakresie etykietowania.
- Badania wykazały, że na niektórych rynkach 40% etykiet leków nie spełnia wymogów prawnych, a często brakuje na nich kluczowych informacji dotyczących bezpieczeństwa.
- Według podsumowańFDA US FDA na całym świecie 35–40% wycofań produktów wynika z błędów w opakowaniach i na etykietach.
- W audytach regulacyjnych ponad 50% ustaleń dotyczy dokumentacji związanej z etykietowaniem, od informacji dotyczących stosowania po artwork tłumaczenia.
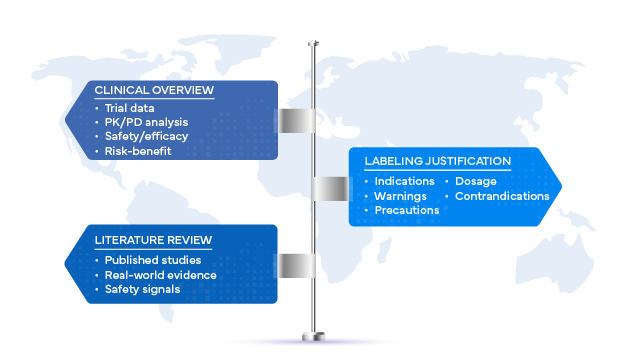
Statystyki te podkreślają jedną istotną kwestię: decyzje dotyczące klasyfikacji muszą być precyzyjne, oparte na dowodach naukowych i w pełni uzasadnione. Podstawą takiego uzasadnienia są przeglądy kliniczne oraz systematyczne przeglądy literatury.
Rola przeglądu klinicznego
Przegląd kliniczny, zgodnie z definicją zawartą w ICH (R2), to coś więcej niż tylko formalność regulacyjna. Jest to uporządkowana, krytyczna analiza wszystkich dostępnych danych klinicznych stanowiących podstawę opracowania produktu. W kontekście informacji o produkcie odgrywa on decydującą rolę w zapewnieniu, że bezpieczeństwo, skuteczność oraz profil korzyści i ryzyka są jasno przedstawione w informacjach dotyczących przepisywania leku.
Najważniejsze elementy przeglądu klinicznego, które mają wpływ na treść ulotki, to:
- Bezpośrednie powiązanie wyników badań klinicznych z oświadczeniami dotyczącymi produktu
- Uzasadnienie umieszczenia ostrzeżeń, środków ostrożności i przeciwwskazań
- Zapewnienie spójności między ustaleniami dotyczącymi bezpieczeństwa a decyzjami w sprawie oznakowania
- Przedstawienie organom regulacyjnym przejrzystej, opartej na dowodach analizy stosunku korzyści do ryzyka
Na przykład, jeśli dane z badań klinicznych wskazują na wystąpienie zdarzenia niepożądanego o znaczeniu statystycznym w danej podgrupie, przegląd wyników klinicznych stanowi uzasadnienie dla umieszczenia w ulotce ostrzeżeń dotyczących konkretnej podgrupy.
Dlaczego przeglądy literatury są niezbędne
Chociaż dane z badań klinicznych stanowią podstawę uzasadnienia treści ulotki, systematyczne przeglądy literatury poszerzają bazę dowodową poprzez uwzględnienie wyników badań wykraczających poza badania prowadzone przez sponsora. Przeglądy te stanowią syntezę recenzowanych publikacji, dowodów pochodzących z praktyki klinicznej oraz danych dotyczących bezpieczeństwa po wprowadzeniu produktu do obrotu, zapewniając organom regulacyjnym szerszą i obiektywną perspektywę.
Dokładny przegląd literatury pomaga firmom w:
- Zweryfikować informacje dotyczące bezpieczeństwa, korzystając z niezależnych źródeł
- Wykrywanie wczesnych sygnałów ostrzegawczych lub działań niepożądanych, które nie ujawniły się podczas badań klinicznych
- Wyniki testów porównawczych w stosunku do produktów konkurencji lub tendencje ogólne w danej kategorii
- Dostosowanie arkuszy danych podstawowych (CCDS) do regionalnych dokumentów dotyczących produktów (LPD)
Na przykład opublikowane badania lub metaanalizy mogą ujawnić rzadkie, ale poważne zdarzenia niepożądane, co stanowi dodatkowe uzasadnienie dla umieszczenia lub aktualizacji ostrzeżenia w ulotce.
Wymogi regulacyjne dotyczące uzasadnienia oznakowania
Światowe organy ds. zdrowia, w tym US FDA, EMA, MHRA i PMDA, oczekują, że uzasadnienia umieszczane na etykietach będą odzwierciedlać rygor naukowy, przejrzystość i spójność. Eksperci ds. oceny regulacyjnej często analizują:
- Hierarchia dowodów: priorytetowe traktowanie danych z randomizowanych badań kontrolowanych przy jednoczesnym uwzględnieniu istotnych badań obserwacyjnych lub badań w warunkach rzeczywistych
- Spójność między dokumentami: zapewnienie zgodności między opisem klinicznym, podsumowaniem bezpieczeństwa klinicznego (SCS) a proponowaną ulotką
- Jasne uzasadnienie: wyjaśnienie, dlaczego każde wskazanie, zalecenie dotyczące dawkowania lub ostrzeżenie zostało uwzględnione (lub pominięte)
Brak jasnych dowodów uzasadniających oznakowanie może skutkować zapytaniami ze strony organów regulacyjnych, wydłużeniem terminów rozpatrywania wniosków, a nawet odrzuceniem wniosku.
Najlepsze praktyki dotyczące uzasadniania decyzji dotyczących etykietowania
Firmy farmaceutyczne mogą wzmocnić swoje wnioski dotyczące etykietowania, stosując się do poniższych najlepszych praktyk:
- Współpraca międzyfunkcyjna: Należy zaangażować zespoły ds. klinicznych, bezpieczeństwa i regulacji w celu uzyskania całościowej oceny
- Wykorzystaj możliwości technologii: korzystaj z narzędzi opartych na sztucznej inteligencji do przeglądu literatury, aby przyspieszyć i wyodrębniania informacji
- Prowadzenie dokumentacji: Należy rejestrować uzasadnienia dotyczące włączenia lub wyłączenia pacjentów z badań, aby spełnić wymogi kontroli organów regulacyjnych
- Porównanie z rynkiem światowym: dostosowanie się do produktów konkurencji i zmieniających się wytycznych w celu wyeliminowania luk w zakresie zgodności
- Stale aktualizuj: uwzględniaj najnowszą literaturę i monitorowanie bezpieczeństwa stosowania produktów leczniczych nigdy nie tłumacz jako system fotowoltaiczny w bieżących strategiach dotyczących etykietowania
Podsumowanie
W obliczu bezprecedensowej kontroli organów regulacyjnych i rosnących kosztów związanych z nieprzestrzeganiem przepisów firmy nie mogą sobie pozwolić na opieranie się na domysłach podczas opracowywania etykiet produktów. Solidny przegląd wyników badań klinicznych w połączeniu z kompleksowym przeglądem literatury gwarantuje, że każde twierdzenie jest poparte przejrzystymi dowodami naukowymi.
W Freyr Solutions pomagamy międzynarodowym firmom farmaceutycznym radzić sobie z tymi złożonymi wyzwaniami. Dzięki naszemu end-to-end w zakresie etykietowania regulacyjnego, dokumentacji klinicznej oraz strategii zapewnienia zgodności z przepisami mamy pewność, że Państwa decyzje dotyczące etykietowania są naukowo uzasadnione, zgodne z wymogami organów regulacyjnych oraz spójne na całym świecie.
Nawiąż współpracę z firmą Freyr już dziś, aby wzmocnić swoją strategię w zakresie etykietowania dzięki popartym dowodami argumentom, którym ufają organy regulacyjne i na których polegają pacjenci.










