
La farmacovigilancia (FV) implica actividades para detectar, evaluar, comprender y prevenir los efectos adversos de los medicamentos/eventos adversos (EA) de los productos farmacéuticos para garantizar la seguridad de los pacientes. En la fase de poscomercialización de cualquier empresa fabricante de productos farmacéuticos o biológicos, los presupuestos se asignan principalmente a procesos como la notificación de reacciones adversas a medicamentos (RAM) y el procesamiento de casos, la notificación agregada y la detección de señales. Una encuesta de una firma consultora líder con sede en Inglaterra muestra que un departamento de FV gasta alrededor del 40-85% del presupuesto asignado en operaciones de procesamiento de casos. Por otro lado, el volumen de casos ha crecido a una tasa del 10-15% cada año, según el Sistema de Notificación de Eventos Adversos (FAERS) de la Administración de Alimentos y Medicamentos de US (FDA).
La era de la digitalización transformó los sistemas de farmacovigilancia y reunió la experiencia en farmacovigilancia, tecnología, calidad y reglamentaria de toda la industria para identificar oportunidades de automatización. Algunos impulsores clave de este cambio de paradigma son:
- Naturaleza intensiva en recursos - Las estrategias centradas en el paciente y los regímenes de tratamiento han allanado el camino para un aumento de los procesos de farmacovigilancia (PV). Los procesos de PV actualmente son intensivos en recursos, lo que los hace más propensos al riesgo de errores e ineficiencias operativas.
- Aumento del volumen de casos de Eventos Adversos (EA)/Reacciones Adversas a Medicamentos (RAM) con una mayor carga de enfermedad - Con las nuevas enfermedades que alteran la industria de la salud, junto con los repuntes posteriores a la COVID-19, ha habido un aumento exponencial en el volumen de casos de EA y RAM.
- Exigencia reglamentaria estricta: Las normas de los organismos reguladores de salud a nivel mundial se han vuelto más estrictas, lo que lleva a las organizaciones a adoptar un 'cambio digital' para gestionar las operaciones de PV.
¿La FDA de US ya estaba 'digitalmente preparada' o se está actualizando para mejorar?
El lanzamiento del Sistema de Notificación de Eventos Adversos de la Administración de Alimentos y Medicamentos (FAERS) y del Sistema de Notificación de Eventos Adversos de Vacunas (VAERS) ayudó a las partes interesadas a revisar el rendimiento de sus productos medicinales en el mercado basándose en los casos de EA y RAM. Bajo el proyecto ‘Mejora de la Eficiencia y el Rigor de la Farmacovigilancia en la FDA’, que comenzó en 2014, los investigadores utilizan los enfoques del Procesamiento del Lenguaje Natural (NLP) y el Aprendizaje Automático (ML) para analizar los informes de FAERS y VAERS. El proyecto tiene como objetivo mejorar el rendimiento y la precisión de las bases de datos utilizadas por la FDA de US.
Digitalización en Operaciones de PV
Dado que muchas de las operaciones de PV giran en torno al procesamiento de casos, la notificación agregada y la detección de señales, muchas operaciones de PV digital proponen un 'enfoque de superposición'. Este enfoque funciona principalmente con el modelo de aprendizaje automático (ML) e impulsa los datos sobre la información que se recopila, analiza y procesa en cualquiera de las tres operaciones. El segundo enfoque es el aprendizaje por fases y la experimentación con diversas herramientas hasta ponerlas en funcionamiento para las operaciones.
Enfoque de ML para futuras operaciones de PV
Una de las revisiones sistemáticas publicadas a principios de 2022 indicaron el uso potencial de la PNL para superar las prácticas convencionales de FV. Los científicos de datos revelaron que la PNL podría mapear e identificar diferentes tipos de EA y términos relevantes para la literatura seleccionada. Con tales resultados complementarios y fiables, las operaciones digitales de FV serían el futuro en varias organizaciones basadas en FV.
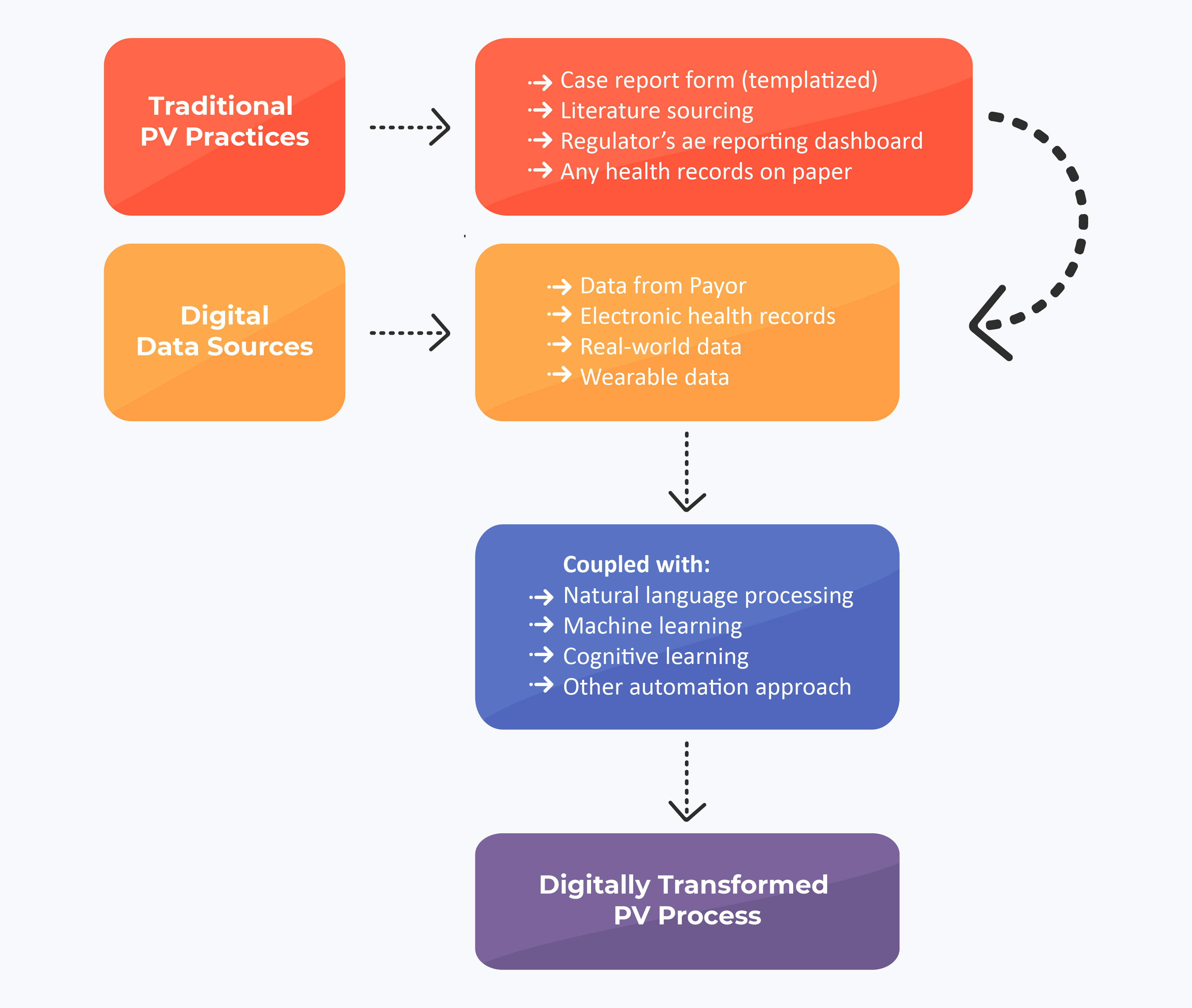
El poder de la tecnología debe aprovecharse para transformar la industria de la farmacovigilancia, permitiéndole centrarse más en el análisis y la predicción para facilitar una toma de decisiones ágil, la maximización del beneficio/riesgo para pacientes y proveedores de atención médica, y una mayor eficiencia de la atención médica. Los imperativos comerciales de la farmacovigilancia ahora pueden ser más sencillos cuando se asocian con un socio experimentado y con conocimientos como Freyr. Además, un socio como Freyr puede atender consultas comerciales personalizadas y resolverlas con un tiempo de respuesta rápido. ¡Consulte a Freyr!










