Cuando la pandemia de COVID-19 fue reconocida por primera vez como una crisis de salud global en 2020, las Autoridades Sanitarias (AS) globales tomaron medidas innovadoras para abordarla de la mejor manera posible. Del mismo modo, las empresas farmacéuticas desarrollaron varias vacunas/productos medicinales en beneficio del público. Sin embargo, registrar los productos resultó ser bastante desafiante. Para simplificar el registro manteniendo su seguridad, calidad y eficacia, las AS concedieron Autorizaciones de Uso de Emergencia (EUA) a algunas vacunas y productos relevantes.
Puede surgir la pregunta de cómo las Autoridades Sanitarias (AS) pudieron asegurar que los beneficios de dichos productos superaban los riesgos. La respuesta es la adopción de las mejores prácticas de farmacovigilancia (FV).
¿Qué es la Farmacovigilancia?
PV se define como un conjunto de actividades científicas relacionadas con la detección, evaluación, comprensión y prevención de efectos adversos y cualquier otro problema relacionado con los medicamentos. A continuación, se presenta una explicación figurada de cómo funciona PV y el proceso que implica.
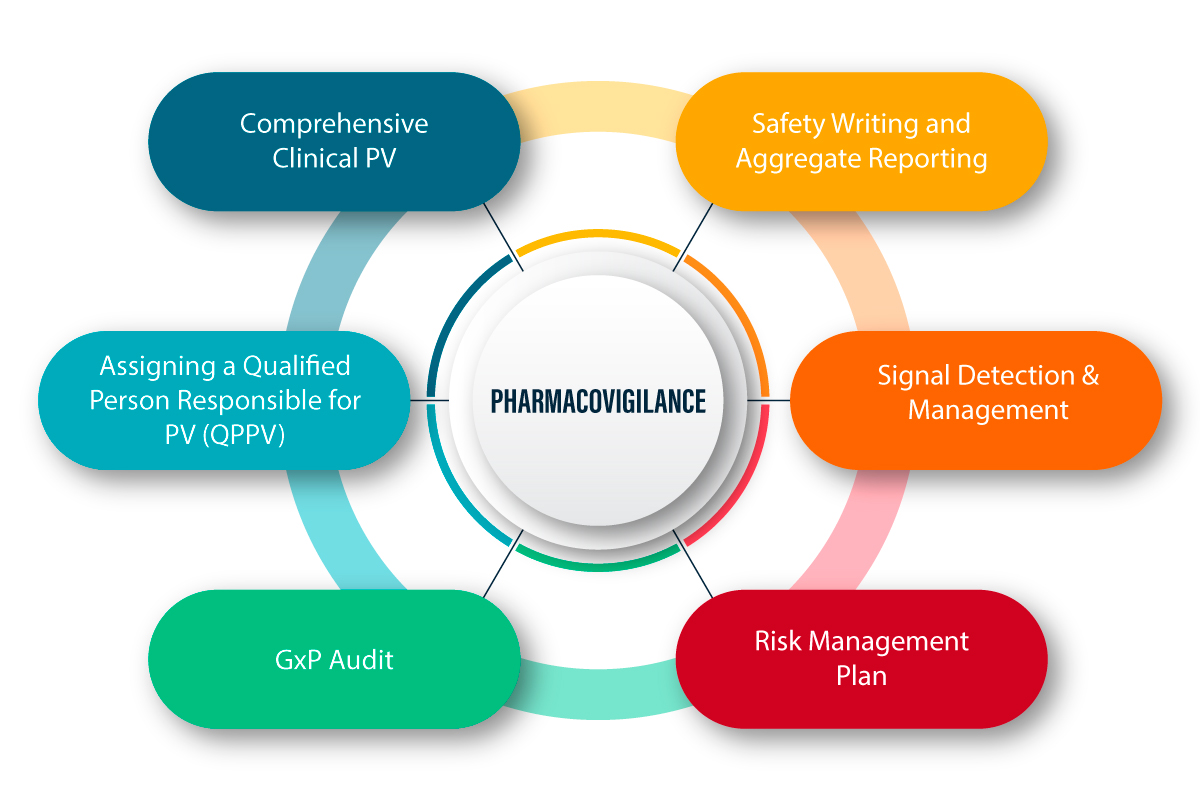
La PV en la pandemia de COVID-19
Cuando la pandemia de COVID-19 comenzó a extenderse por todo el mundo, las vacunas y los productos medicinales relevantes tuvieron que introducirse en el mercado en un período limitado, manteniendo los estándares de calidad requeridos. En tales escenarios, hubo menos sujetos disponibles para ensayos clínicos durante la etapa de desarrollo de medicamentos/vacunas, y el proceso tuvo que completarse más rápido de lo normal. Esto podría provocar la aparición de ciertos efectos adversos en la fase posterior a la aprobación.
Por lo tanto, el equilibrio beneficio-riesgo de las vacunas/productos medicinales se consideró primordial. Con una comunicación oportuna de las reacciones adversas y los efectos secundarios perjudiciales, la eficacia de los productos se mantuvo en tiempo real.
Algunas de las actividades clave de farmacovigilancia que ayudaron a mantener la seguridad, la calidad y la eficacia de dichos productos durante la pandemia son las siguientes:
- Adoptar un buen plan de gestión de riesgos
- Evaluación de riesgos con la ayuda de los Informes Periódicos Actualizados de Seguridad (PSURs)
- Recopilación de los datos de exposición
- Estudios de Seguridad Posteriores a la Autorización (PASS)
- Notificación espontánea de reacciones adversas sospechosas.
- Gestión eficaz de señales
Farmacovigilancia (PV) en Asuntos Regulatorios (RA)
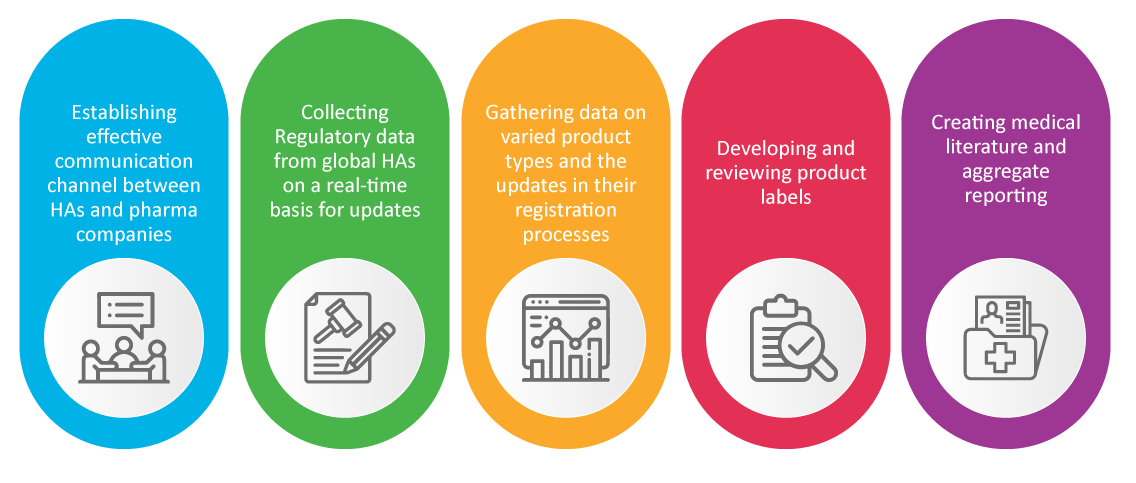
Es bien sabido que el equipo de Asuntos Regulatorios de una empresa farmacéutica es responsable de la seguridad y aprobación de los nuevos productos. Los especialistas en RA se encargan de las actividades de farmacovigilancia que resultaron cruciales durante la pandemia, tales como:
Conclusión
Para concluir, la farmacovigilancia (FV) ayuda a supervisar e informar sobre la seguridad de un medicamento. Con informes individualizados de casos de estudio (ICSR), a los fabricantes/patrocinadores les resulta más fácil cumplir con las normativas respectivas de las autoridades sanitarias globales. ¿Busca apoyo reglamentario para la preparación de ICSR? Consulte a un experto reglamentario de confianza para el cumplimiento. Contacte con Freyr.










