Resumen y definición
Dispositivos Médicos y adquisiciones (M&A) en el Dispositivos Médicos plantean complejos retos normativos en múltiples jurisdicciones. La integración de dos empresas requiere armonizar los sistemas de gestión de la calidad (SGC), gestionar las solicitudes reglamentarias y armonizar los procesos clínicos y poscomercialización.
Los servicios especializados de Freyr en materia de Dispositivos Médicos y adquisiciones y normativa sobre Dispositivos Médicos ofrecen end-to-end para ayudar a su organización a superar estos retos sin contratiempos, garantizando el cumplimiento continuo de la ISO 13485, el Reglamento sobre Dispositivos Médicos (MDR), FDA y otras normas internacionales.
Proceso de cumplimiento normativo en Dispositivos Médicos
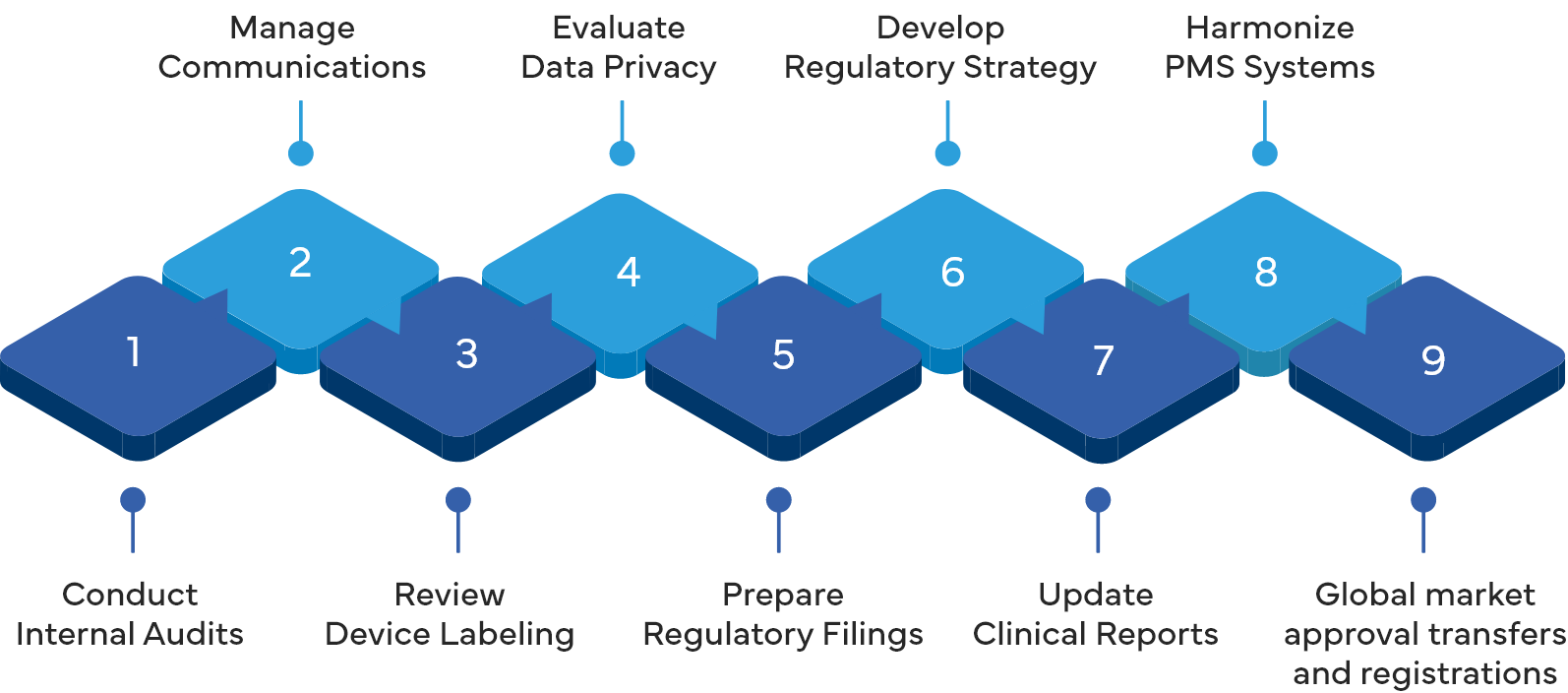
Servicios de Freyr
INTEGRACIÓN DE PMS
- Integrar los sistemas de gestión de pedidos de las dos empresas.
- Armonizar los procesos de notificación de eventos adversos y de análisis de tendencias.
DILIGENCIA DEBIDA REGULATORIA
- Evaluación exhaustiva del cumplimiento normativo de la empresa objetivo, incluyendo el sistema de gestión de la calidad, los registros de productos, los datos clínicos y el etiquetado.
- Identificación de posibles riesgos y responsabilidades normativas.
- Análisis de deficiencias y planificación de medidas correctoras.
ESTRATEGIA Y PLANIFICACIÓN REGULATORIA
- Elaboración de una estrategia regulatoria integral para integrar las carteras de productos de ambas empresas.
- Planificación de la transferencia y actualización de los registros y licencias reglamentarios en todos los mercados pertinentes.
- Elaboración de un calendario para las actividades normativas.
INTEGRACIÓN DEL SISTEMA DE GESTIÓN DE LA CALIDAD Y DE LAS ACCIONES CORRECTIVAS Y PREVENTIVAS
- Armonizar los sistemas de gestión de la calidad de ambas empresas para garantizar el cumplimiento de ISO 13485 otras normas pertinentes.
- Desarrollo e implantación de un sistema unificado de documentación del sistema de gestión de la calidad.
- Realización de auditorías internas y análisis de deficiencias.
- Solicitudes reglamentarias y registros:
- Preparar y presentar toda la documentación reglamentaria necesaria para la transferencia y actualización de los registros de productos.
- Gestión de las comunicaciones con las autoridades reguladoras.
INTEGRACIÓN DE LA PROTECCIÓN DE DATOS Y LA CIBERSEGURIDAD
- Realizar una evaluación exhaustiva de los riesgos relacionados con la privacidad de los datos y la ciberseguridad.
- Elaborar y poner en práctica un plan para integrar los sistemas de protección de datos y ciberseguridad.
- Garantizar el cumplimiento del RGPD y otras normativas pertinentes.
- Mapeo de todos los datos que se transfieren.
ACTUALIZACIONES DE LA FICHA TÉCNICA
- Gestión de datos clínicos y evaluaciones:
- Evaluación de la validez y la transferibilidad de los datos clínicos.
- Actualizar los informes de evaluación clínica (CER) según sea necesario.
- Gestión de las actividades de seguimiento clínico poscomercialización (PMCF).
CUMPLIMIENTO DE LAS NORMAS DE ETIQUETADO
- Revisar y actualizar los materiales de etiquetado para reflejar el cambio de propiedad y garantizar el cumplimiento de la normativa local.
- Creación de una estrategia de etiquetado unificada.
Desafío
Los servicios de Freyr y cómo te ayudamos
Variabilidad en el grado de madurez y el estado de cumplimiento de los sistemas de gestión de la calidad
Servicios de armonización de sistemas de gestión de la calidad: Nuestro equipo de consultores especializados en fusiones y adquisiciones lleva a cabo análisis de deficiencias y auditorías internas para unificar y armonizar los sistemas de gestión de la calidad (SGC) con ISO 13485 las normas reglamentarias, con el fin de lograr una integración fluida.
Trámites normativos complejos y transferencias de registros
Asuntos Regulatorios (escisiones, Dispositivos Médicos y adquisiciones, desinversiones) Servicios: Gestión de solicitudes reglamentarias, transferencias de licencias y comunicaciones con las autoridades internacionales para garantizar la obtención oportuna de las autorizaciones y el cumplimiento normativo continuo.
Garantizar el cumplimiento de las normas de etiquetado para reflejar el cambio de propiedad
Servicios de actualización y cumplimiento normativo en materia de etiquetado: Desarrollamos e implementamos estrategias de etiquetado unificadas y conformes con la normativa para reflejar el cambio de propiedad y cumplir con todos los requisitos reglamentarios regionales.
Gestión de los datos de evaluación clínica y PMCF
Gestión de datos clínicos y evaluaciones: evaluar la transferibilidad de los datos clínicos, actualizar los informes de evaluación clínica (CER) y gestionar las actividades de seguimiento clínico poscomercialización (PMCF).
Cumplimiento normativo en materia de protección de datos y ciberseguridad
Evaluaciones de privacidad de datos y ciberseguridad: Evaluar e integrar los sistemas de privacidad de datos y ciberseguridad para garantizar el cumplimiento del RGPD y otras normativas internacionales.
Combinación de los sistemas de vigilancia poscomercialización y la notificación
Servicios de farmacovigilancia y asuntos médicos (SoMAD): Armonizar los sistemas de vigilancia poscomercialización, la notificación de reacciones adversas y el análisis de tendencias para garantizar un seguimiento de la seguridad coherente y conforme a la normativa.
NO ofrecemos
Asesoramiento jurídico en Dispositivos Médicos y adquisiciones en el sector de Dispositivos Médicos
Asesoramiento financiero o en materia de transacciones
Servicios de integración operativa o de fabricación
Nota: Aunque actuamos como su asesor en materia de fusiones y adquisiciones desde el punto de vista normativo, nos centramos exclusivamente en el cumplimiento normativo y no prestamos servicios jurídicos, financieros ni operativos relacionados con fusiones y adquisiciones.
¿Por qué asociarse con Freyr?

Historia de éxito demostrada
Entrada optimizada al mercado global para una organización de diagnóstico dental impulsada por IA.
Una empresa de diagnóstico dental en fase inicial impulsada por IA se asoció con Freyr para navegar por el complejo panorama normativo global.