¿Qué es la QMSR?
FDA es un enfoque simplificado que se ajusta a los requisitos de ISO 13485:2016, la cual constituye una actualización de la anterior estructura del QSR. Esta armonización es fundamental, ya que simplifica el cumplimiento normativo a nivel mundial para los fabricantes, especialmente para aquellos que operan a escala global. Esta armonización permitirá a las empresas cumplir los requisitos normativos tanto en US en otros mercados de una manera mucho más unificada.
La QMSR exige mejoras en la gestión de riesgos, el diseño de los productos sanitarios y la vigilancia poscomercialización. Esta actualización puede añadir cierta complejidad, pero también permite a los fabricantes estandarizar sus procedimientos de calidad, lo que a su vez aumenta la seguridad de los productos sanitarios y mejora la documentación, algo que puede resultar fundamental durante USFDA .
¿Por qué es fundamental la transición de QSR a QMSR?

Ajustarse a las normas internacionales
Esto ayudará a los fabricantes a armonizar sus sistemas de gestión de la calidad con Dispositivos Médicos internacionales aplicables a Dispositivos Médicos mediante la adopción de la norma QMSR, lo que reducirá las redundancias normativas para los Dispositivos Médicos que operan a nivel mundial.
Mejora de la calidad, la seguridad y la eficacia
Esta integración garantiza que los dispositivos se fabriquen de acuerdo con los requisitos del sistema de gestión de la calidad a nivel mundial. Esto ayuda al fabricante a mejorar la calidad y la seguridad de los dispositivos.
Cumplimiento Reglamentario
Esto ayuda a los fabricantes a adaptarse a los nuevos requisitos y reduce el riesgo de incumplimiento cuando el reglamento entre en vigor el 2 de febrero de 2026.
Cambios clave en la transición de QSR a QMSR:
Armonización con la terminología de ISO 13485:2016
Esto garantiza que los fabricantes adopten normas aceptadas a nivel mundial.
Gestión de riesgos:
Hace hincapié en la gestión de riesgos a lo largo de todo el ciclo de vida de los Dispositivos Médicos.
Diseño y controles del dispositivo
En virtud de FDA , se ampliaron los controles de diseño para garantizar que los fabricantes tengan plenamente en cuenta las necesidades de los usuarios, la seguridad del producto y los criterios de rendimiento, lo cual constituye un aspecto fundamental durante USFDA .
Post Market Surveillance
Las empresas deben reforzar el sistema de vigilancia poscomercialización. Esto implicará que los fabricantes recopilen información sobre la seguridad y la eficacia de los productos, lo que contribuirá a detectar y resolver rápidamente los problemas.
Documentación y mantenimiento de registros
La normativa definitiva hace hincapié en la importancia de llevar un registro exhaustivo de la documentación, lo cual resulta fundamental durante la inspección.
Fechas importantes
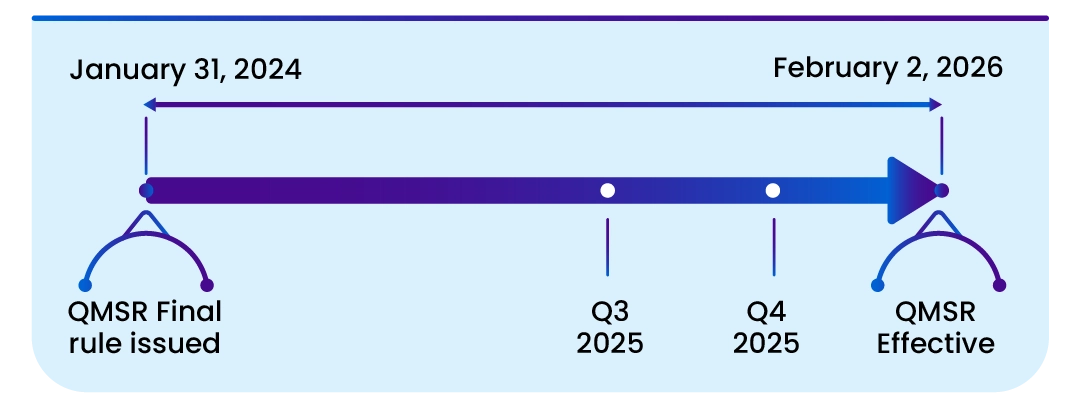
Esta norma entrará en vigor el 2 de febrero de 2026. La incorporación por referencia de determinados documentos enumerados en esta norma fue aprobada por el Director del Registro Federal el 2 de febrero de 2024.
Obtén asesoramiento experto sobre el cumplimiento de la normativa QMSR
QMSR
- Clasificación de los productos sanitarios segúnFDA
- Elaboración de documentos de conformidad con el 21 CFR 820.
- Análisis de deficiencias de los documentos del Sistema de Gestión de la Calidad (SGC) existente, de conformidad con 21 CFR 820.
- Plan de remediación para el cumplimiento de 21 CFR 820.
- Auditorías simuladas.
- Un equipo dedicado de Garantía de Calidad (QA) de expertos en Dispositivos Médicos.
- Experiencia demostrada en la gestión del cumplimiento de 21 CFR 820.
- Modelos flexibles de entrega de proyectos.




 La norma QMSR entrará en vigor el 2 de febrero de 2026, por lo que los fabricantes estarán obligados a actualizar su sistema de gestión de la calidad.
La norma QMSR entrará en vigor el 2 de febrero de 2026, por lo que los fabricantes estarán obligados a actualizar su sistema de gestión de la calidad. Una implementación puntual y un mantenimiento eficaz pueden reducir la probabilidad de que se produzcan retiradas de productos y reclamaciones.
Una implementación puntual y un mantenimiento eficaz pueden reducir la probabilidad de que se produzcan retiradas de productos y reclamaciones. El cumplimiento de la normativa QMSR puede reducir las observaciones deFDA US ,FDA no afectará a la situación del producto en el mercado regulado.
El cumplimiento de la normativa QMSR puede reducir las observaciones deFDA US ,FDA no afectará a la situación del producto en el mercado regulado.