
La Farmacovigilanza (FV) comprende attività volte a rilevare, valutare, comprendere e prevenire gli effetti avversi dei farmaci/eventi avversi (EA) dei prodotti farmaceutici per garantire la sicurezza dei pazienti. Nella fase post-marketing di qualsiasi azienda produttrice di farmaci o prodotti biologici, i budget sono principalmente allocati a processi quali la segnalazione delle Reazioni Avverse ai Farmaci (ADR) e l'elaborazione dei casi, la segnalazione aggregata e il rilevamento dei segnali. Un'indagine condotta da una delle principali società di consulenza con sede in Inghilterra mostra che un dipartimento di FV spende circa il 40-85% del budget allocato per le operazioni di elaborazione dei casi. D'altra parte, i volumi dei casi sono cresciuti a un tasso del 10-15% ogni anno, secondo il sistema di segnalazione degli eventi avversi (FAERS) della US Food and Drug Administration (FDA).
L'era della digitalizzazione ha trasformato i sistemi di farmacovigilanza (FV) e ha riunito l'esperienza in FV, tecnologia, qualità e normativa in tutto il settore per identificare opportunità di automazione. Alcuni dei principali motori di questo cambiamento di paradigma sono:
- Natura ad alta intensità di risorse - Le strategie incentrate sul paziente e i regimi di trattamento hanno aperto la strada a un aumento dei processi di farmacovigilanza (PV). I processi di PV sono attualmente ad alta intensità di risorse, il che li rende più soggetti al rischio di errori e inefficienze operative.
- Aumento dei volumi di casi di eventi avversi (AE)/reazioni avverse ai farmaci (ADR) con un maggiore carico di malattie - Con nuove malattie che sconvolgono il settore sanitario, in concomitanza con i picchi post-COVID19, si è verificato un aumento esponenziale dei volumi di casi di AE e ADR.
- Esigenze normative rigorose - Le norme delle autorità di regolamentazione sanitarie globali sono diventate più rigorose, spingendo così le organizzazioni ad adottare una 'svolta digitale' per la gestione delle operazioni PV.
La FDA era già "pronta digitalmente" o si sta aggiornando per il meglio?
Il lancio del Food and Drug Administration Adverse Event Reporting System (FAERS) e del Vaccine Adverse Event Reporting System (VAERS) ha aiutato gli stakeholder a rivedere le prestazioni dei loro prodotti medicinali sul mercato in base ai casi di AE e ADR. Nell'ambito del progetto 'Improving the Efficiency and Rigor of Pharmacovigilance at FDA', avviato nel 2014, i ricercatori utilizzano gli approcci di Natural Language Processing (NLP) e Machine Learning (ML) per analizzare i rapporti FAERS e VAERS. Il progetto mira a migliorare le prestazioni e l'accuratezza dei database utilizzati dalla US FDA.
Digitalizzazione nelle Operazioni di Farmacovigilanza
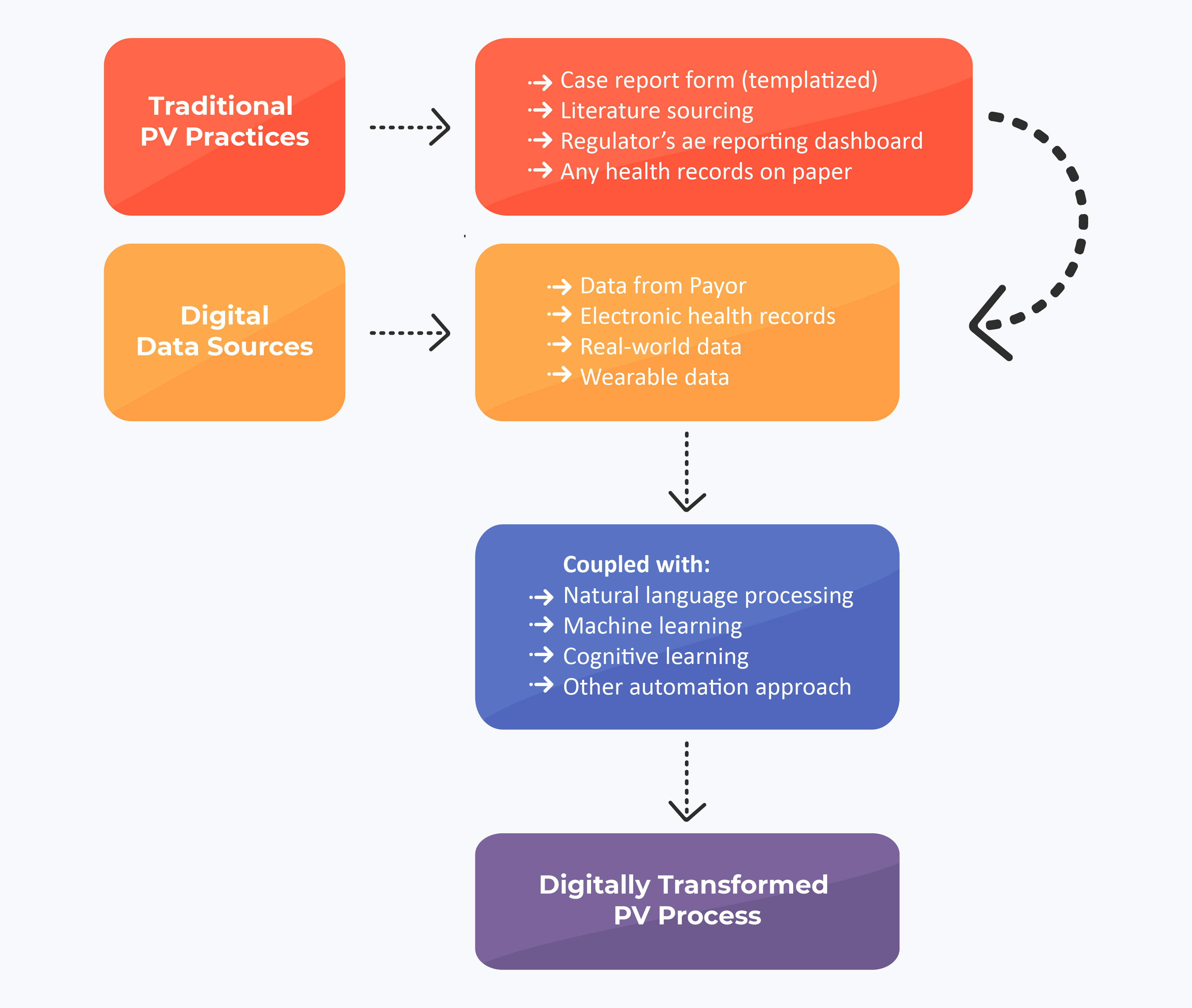
Mentre molte delle operazioni di farmacovigilanza (PV) ruotano attorno all'elaborazione dei casi, alla segnalazione aggregata e al rilevamento dei segnali, molte operazioni di PV digitale propongono un 'approccio di sovrapposizione'. Questo approccio si basa principalmente sul modello di Machine Learning (ML) e gestisce i dati sulle informazioni che vengono raccolte, analizzate ed elaborate in una delle tre operazioni. Il secondo approccio è l'apprendimento per fasi e la sperimentazione con vari strumenti fino a renderli operativi.
Approccio ML per le future operazioni PV
Una delle revisioni sistematiche pubblicate all'inizio del 2022 ha indicato il potenziale utilizzo dell'NLP nel superare le pratiche convenzionali di farmacovigilanza (PV). Gli scienziati dei dati hanno rivelato che l'NLP potrebbe mappare e identificare diversi tipi di eventi avversi (AE) e termini rilevanti per la letteratura selezionata. Con risultati così complementari e affidabili, le operazioni di farmacovigilanza digitale sarebbero il futuro in diverse organizzazioni basate sulla farmacovigilanza.
Il potere della tecnologia deve essere sfruttato per trasformare l'industria della farmacovigilanza, permettendole di concentrarsi maggiormente sull'analisi e la previsione per consentire un processo decisionale agile, la massimizzazione del rapporto beneficio/rischio per pazienti e operatori sanitari e una maggiore efficienza dell'assistenza sanitaria. Gli imperativi aziendali della farmacovigilanza possono ora essere gestiti con facilità collaborando con un partner esperto e competente come Freyr. Inoltre, un partner come Freyr può soddisfare richieste aziendali personalizzate e risolverle con tempi di risposta rapidi. Consulta Freyr!










