Quando la pandemia di COVID-19 è stata riconosciuta per la prima volta come crisi sanitaria globale nel 2020, le Autorità Sanitarie (AS) globali hanno adottato misure innovative per affrontarla nel miglior modo possibile. Allo stesso modo, le aziende farmaceutiche hanno sviluppato diversi vaccini/prodotti medicinali a beneficio del pubblico. Tuttavia, la registrazione dei prodotti si è rivelata piuttosto impegnativa. Per semplificare la registrazione mantenendo la loro sicurezza, qualità ed efficacia, le AS hanno concesso Autorizzazioni all'Uso di Emergenza (EUA) a pochi vaccini e prodotti pertinenti.
Potrebbe sorgere la domanda su come le Autorità Competenti siano state in grado di garantire che i benefici di tali prodotti superassero i rischi. La risposta è l'adozione delle migliori pratiche di farmacovigilanza (FV).
Che cos'è la Farmacovigilanza?
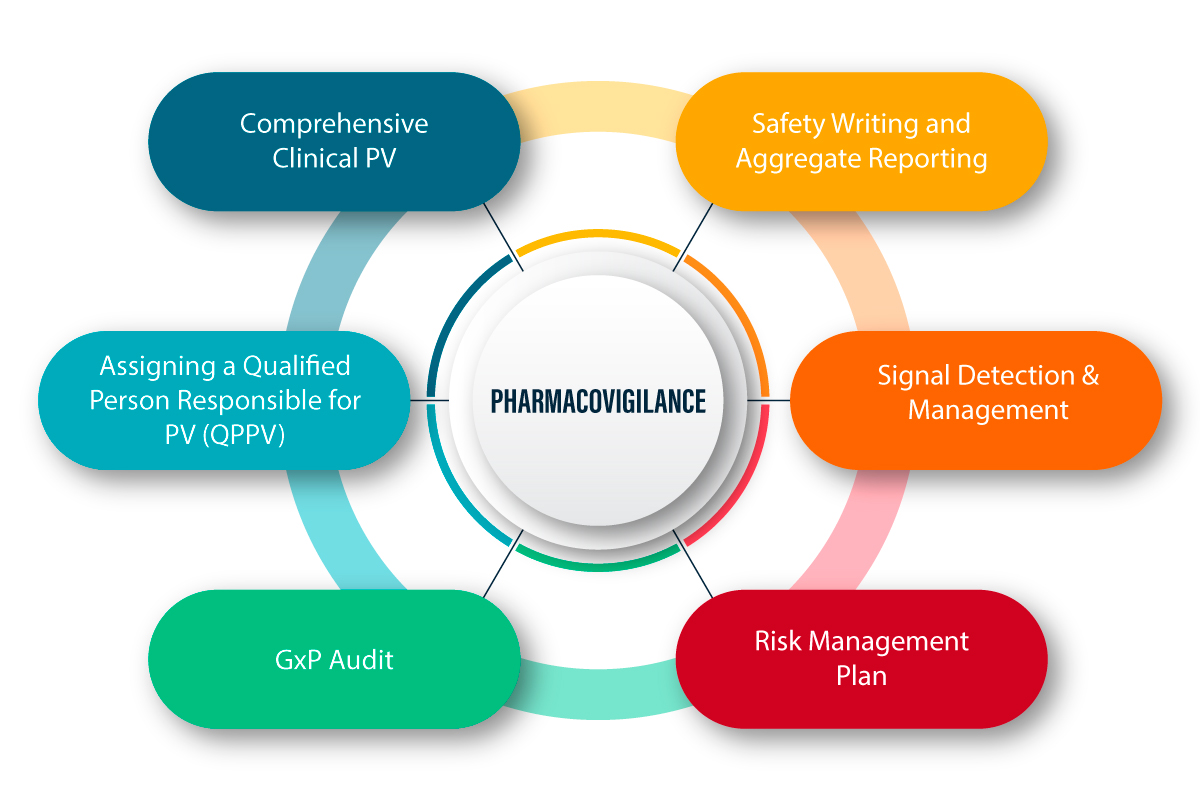
La PV è definita come un insieme di attività scientifiche legate all'individuazione, alla valutazione, alla comprensione e alla prevenzione degli effetti avversi e di qualsiasi altro problema correlato ai farmaci. Segue una spiegazione illustrativa di come funziona la PV e del relativo processo.
La Farmacovigilanza nella Pandemia di COVID-19
Quando la pandemia di COVID-19 ha iniziato a diffondersi in tutto il mondo, vaccini e prodotti medicinali pertinenti dovevano essere introdotti sul mercato in un periodo limitato, mantenendo gli standard di qualità richiesti. In tali scenari, c'erano meno soggetti disponibili per gli studi clinici durante la fase di sviluppo di farmaci/vaccini, e il processo doveva essere completato più velocemente del normale. Ciò potrebbe portare alla comparsa di alcuni effetti avversi nella fase post-approvazione.
Pertanto, il rapporto rischio-beneficio dei vaccini/prodotti medicinali è stato considerato di primaria importanza. Con una comunicazione tempestiva delle reazioni avverse e degli effetti collaterali dannosi, l'efficacia dei prodotti è stata mantenuta in tempo reale.
Alcune delle principali attività di farmacovigilanza (PV) che hanno contribuito a mantenere la sicurezza, la qualità e l'efficacia dei suddetti prodotti durante la pandemia sono le seguenti:
- Adozione di un buon piano di gestione del rischio
- Valutazione del rischio con l'aiuto dei Rapporti periodici di aggiornamento sulla sicurezza (PSUR)
- Raccolta dei dati sull'esposizione
- Studi di Sicurezza Post-Autorizzazione (PASS)
- Segnalazione spontanea di reazioni avverse sospette
- Gestione efficace dei segnali
PV negli Affari Regolatori (RA)
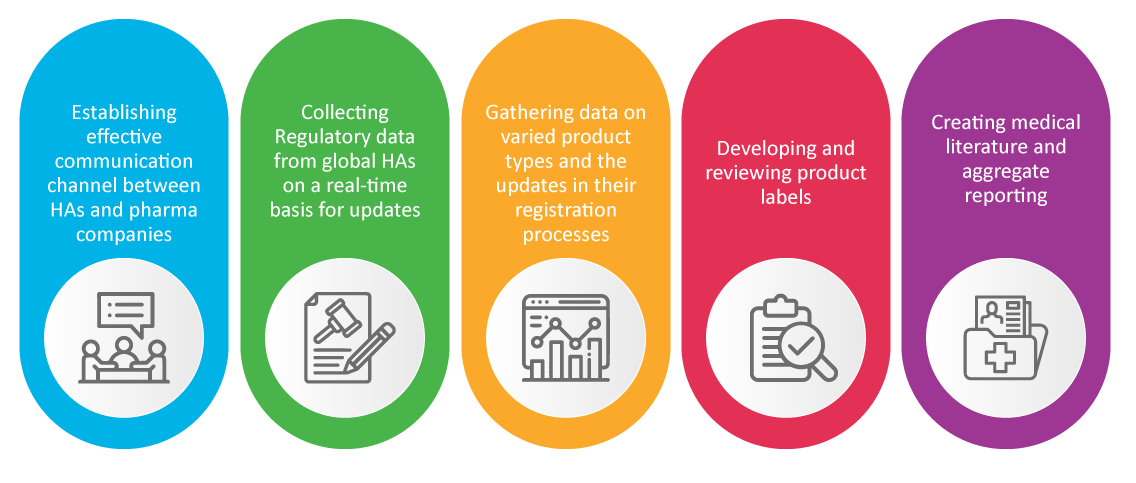
È risaputo che il team di Affari Regolatori di un'azienda farmaceutica è responsabile della sicurezza e dell'approvazione dei nuovi prodotti. Gli specialisti RA si occupano delle attività di farmacovigilanza che si sono rivelate cruciali durante la pandemia, come:
Conclusione
In conclusione, la FV aiuta a monitorare e segnalare la sicurezza di un prodotto farmaceutico. Con rapporti di studio di caso individuali (ICSR) personalizzati, diventa più facile per i produttori/sponsor conformarsi alle rispettive normative delle HA globali. Cercate supporto normativo per la preparazione degli ICSR? Consultate un esperto normativo comprovato per la conformità. Contattate Freyr.










