
La pubblicità di farmaci diretta al consumatore (DTC) è diventata un argomento di discussione molto popolare negli ultimi anni. Queste pubblicità, rivolte ai consumatori anziché ai professionisti sanitari, sono state considerate responsabili dell'aumento della consapevolezza dei pazienti e della domanda di determinati farmaci. Tuttavia, sono state anche criticate per il potenziale rischio di portare a diagnosi e trattamenti eccessivi.
Nel contesto delle attuali tendenze nelle aziende farmaceutiche, la spesa totale per il marketing è notoriamente superiore al budget destinato alla ricerca. A livello globale, sono stati spesi 1,42 trilioni di dollari in marketing. Negli STATI UNITI D'AMERICA, 486,62 miliardi di dollari sono stati spesi nel 2021 per commercializzare farmaci ai medici; in Canada, 29.305,1 milioni di dollari sono stati spesi nel 2022. Analizzando questi numeri, il 56% era costituito da campioni gratuiti, il 25% da attività di "dettaglio" (promozione diretta di farmaci) da parte di rappresentanti farmaceutici ai medici, il 12,5% da pubblicità diretta agli utenti, il 4% da attività di dettaglio negli ospedali e il 2% da annunci su riviste2. A volte, pratiche di marketing negative possono influire sia sui pazienti che sulla professione sanitaria.
Tipi di attività promozionali per i farmaci
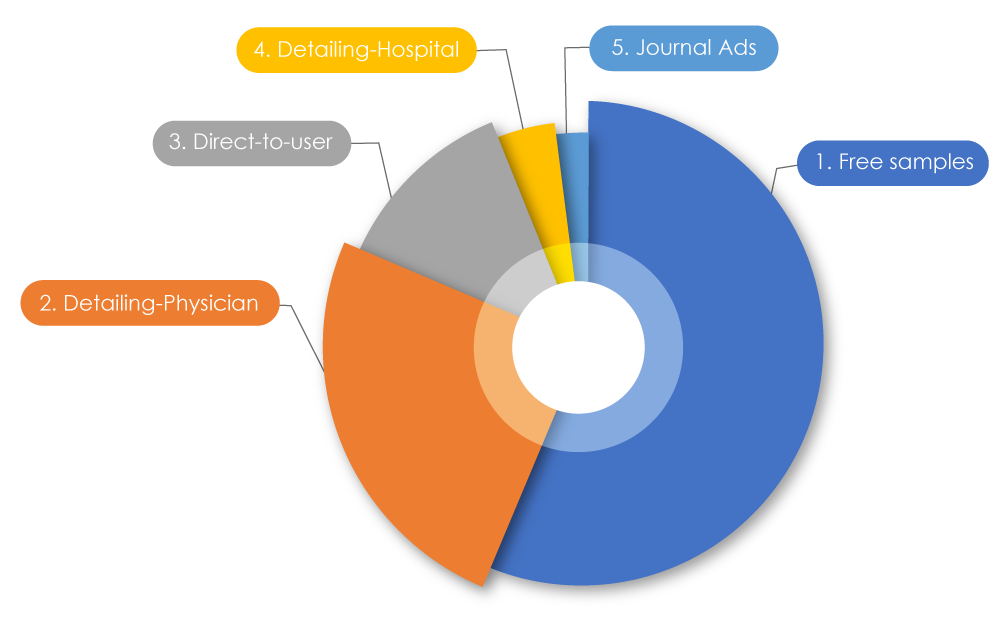
Fonte: Pharmaceutical marketing - Wikiwand
Pubblicità farmaceutica al pubblico
Sono imposte restrizioni alla pubblicità dei farmaci da prescrizione al pubblico in generale, comunemente nota anche come pubblicità diretta al consumatore (DTC). Per promuovere i farmaci da prescrizione al pubblico, la comunicazione deve soddisfare determinati requisiti fondamentali:
- La coerenza "on-label" della pubblicità e della promozione dei farmaci da prescrizione si basa sull'uso previsto per il quale il prodotto è approvato dalla FDA (l'etichettatura del farmaco approvata dalla FDA). L'etichettatura fornisce informazioni su come utilizzare il prodotto in modo sicuro ed efficace per l'indicazione approvata. La pubblicità e la promozione che non sono coerenti con l'etichettatura approvata dalla FDA sono considerate promozioni "off-label" illegali.
- La promozione e la pubblicità dei farmaci da prescrizione richiedono un giusto equilibrio tra i benefici e i rischi del prodotto, assicurando che tali informazioni appaiano comparabili in profondità, dettaglio e contesto.
- Le dichiarazioni dovrebbero essere supportate da prove sufficientemente sostanziali o esperienza clinica.
- Veritiero e non fuorviante - Se la pubblicità e la promozione di farmaci soggetti a prescrizione medica sono false o fuorvianti in qualsiasi aspetto, saranno considerate non conformi ai sensi del Federal Food, Drug, and Cosmetic Act (FDCA) e soggette a provvedimenti esecutivi
- Utilizzo di un linguaggio adatto ai consumatori, evitando l'uso di linguaggio tecnico, termini scientifici e gergo medico nella pubblicità e promozione rivolte ai consumatori. Deve essere conforme all'etichettatura o alla monografia approvata del prodotto.
Informazioni Contenute nella Pubblicità Farmaceutica Destinata al Pubblico Generale
La pubblicità e la promozione di farmaci da prescrizione rivolte ai consumatori devono contenere i seguenti elementi fondamentali, come richiesto dal FDCA e dai regolamenti della Food and Drug Administration (FDA).
- I nomi proprietari e stabiliti dovrebbero essere come specificato nei regolamenti FDA
- Dovrebbe includere la quantità quantitativa degli ingredienti del farmaco pubblicizzato.
- Dovrebbe includere un “breve riassunto” che illustri ogni effetto collaterale, avvertenza, precauzione e controindicazione. Principalmente focalizzato sulle informazioni importanti sui rischi piuttosto che su un elenco esaustivo dei rischi correlati al prodotto. La maggior parte dei rischi è presentata in un modo che è più probabile che sia compreso dai consumatori.
- I principali rischi del prodotto dovrebbero essere presentati in modo chiaro, evidente e neutro come una “Dichiarazione importante”
- Le dichiarazioni di divulgazione per gli eventi avversi per le pubblicità DTC devono includere la seguente dichiarazione MedWatch stampata in testo ben visibile: “Si incoraggia a segnalare gli effetti collaterali negativi dei farmaci da prescrizione alla FDA. Visitare www.fda.gov/medwatch o chiamare il numero +1–800-FDA-1088”
- L'etichettatura e la pubblicità di promemoria sono esenti dai requisiti generali. È importante sottolineare che l'etichettatura e la pubblicità di promemoria non sono consentite per un farmaco da prescrizione con un'avvertenza incorniciata nella sua etichettatura approvata dalla FDA.
Per la pubblicità di farmaci DTC, Contattaci
Per la pubblicità di farmaci DTC
Restrizioni sulle interazioni tra pazienti o organizzazioni di pazienti e l'industria
Le interazioni tra aziende farmaceutiche e pazienti/organizzazioni di pazienti sono consentite solo in pochi paesi, come gli Stati Uniti, ma con limitazioni, ad esempio:
- Deve essere come da etichetta/CFL
- Equilibrato
- Adeguatamente comprovato e
- Non altrimenti falso o fuorviante
Inoltre, le interazioni con i clienti non devono implicare lo Statuto Anti-Corruzione, inducendo organizzazioni di pazienti o pazienti a raccomandare o utilizzare il prodotto pubblicizzato.
Nel REGNO UNITO, la pubblicità di DTC al pubblico è consentita per i prodotti farmaceutici ma esclude i bambini. La pubblicità di medicinali soggetti a prescrizione medica al pubblico è proibita. Gli annunci pubblicitari devono includere il nome del prodotto e il nome del principio attivo. Campioni di prodotti o buoni che consentono ai consumatori di ottenere il prodotto gratuitamente o a un prezzo irragionevolmente basso non sono consentiti.
In Germania, la pubblicità al pubblico è consentita per i prodotti farmaceutici esclusivamente per i bambini di età inferiore ai 14 anni. La pubblicità al pubblico dei medicinali soggetti a prescrizione medica è vietata. Ma ci sono anche regole speciali per la pubblicità dei medicinali al di fuori degli ambienti professionali. Queste regole speciali sono principalmente stabilite nella Legge sulla Pubblicità dei Medicinali (Heilmittelwerbegesetz, "HWG") e sono state modificate dalla Legge tedesca sui Prodotti Farmaceutici (Arzneimittelgesetz – "AMG") per essere in linea con la Direttiva 2001/83/CE4.
Dibattito sulla possibilità di pubblicità dei farmaci nell'era digitale
Chi sostiene la pubblicità dei farmaci direttamente ai consumatori (DTC) afferma che questa dà più potere ai pazienti, fornendo loro informazioni sulle diverse opzioni di cura. Sottolineano anche che può aumentare la richiesta di farmaci, il che può essere un vantaggio per le aziende farmaceutiche.
Dall'altro lato, i critici della pubblicità diretta al consumatore (DTC) dei farmaci sostengono che possa portare a sovradiagnosi e sovratrattamento. Affermano che queste pubblicità spesso esagerano i benefici dei farmaci minimizzandone i rischi, portando i pazienti a chiedere ai loro medici farmaci di cui potrebbero non aver bisogno. Inoltre, affermano che ciò può portare a un aumento dei costi sanitari, poiché ai pazienti potrebbero essere prescritti farmaci di marca più costosi anziché alternative generiche più economiche.
Nonostante il dibattito in corso, la pubblicità farmaceutica DTC (Direct-to-Consumer) è destinata a rimanere. La FDA ha emesso linee guida per questo sottotipo di pubblicità, che includono requisiti per la divulgazione dei rischi e un giusto equilibrio tra benefici e rischi. In conclusione, la pubblicità farmaceutica DTC ha il potenziale per educare i pazienti e aumentare la domanda di determinati farmaci. Tuttavia, è anche importante considerare i potenziali svantaggi ed essere consapevoli dei limiti delle informazioni fornite in queste pubblicità. Come sempre, è importante consultare il proprio medico prima di assumere qualsiasi farmaco. Contatta gli esperti Freyr per una conformità End-to-End!










