
Oprócz wypełniania wymaganych zgłoszeń danych xEVMPD, organizacje z branży nauk przyrodniczych będą teraz musiały korzystać z internetowego formularza aplikacyjnego o nazwie Integracja Cyfrowych Zestawów Danych Aplikacyjnych (DADI). Europejska Agencja Leków (EMA) zaprojektowała DADI jako długoterminowe zastępstwo dla elektronicznego formularza aplikacyjnego (eAF) opartego na PDF, który został stworzony w celu wspierania zgłoszeń eCTD.
Harmonogramy tego przejścia zostały niedawno opublikowane przez EMA. DADI zastąpi formularz zmian produktów leczniczych w 2022 roku. Inne formularze zgłoszeniowe dla Produktów Dopuszczonych Centralnie (CAP) i Produktów Dopuszczonych Krajowo (NAP) wkrótce zostaną zastąpione do 2023 roku. Projekt zastąpi również formularze używane do kluczowych procedur UE, w tym Procedury Scentralizowanej (CP), Procedury Wzajemnego Uznawania (MRP), Procedury Zdecentralizowanej (DCP) i Procedury Krajowej (NP).
Formularze internetowe (w tym Formularz Zmian Ludzkich (HVF) dla produktów leczniczych przeznaczonych dla ludzi) ujednolicą dane wejściowe dla eAF, aby zapewnić standardowe dane podstawowe produktu dla produktów leczniczych. Umożliwią one zarówno istniejący wynik czytelny dla człowieka, jak i nowy wynik czytelny dla maszyny do przetwarzania cyfrowego, w oparciu o standard wymiany danych Fast Healthcare Interoperability Resources (FHIR) dla produktów leczniczych. Będą również wykorzystywać istniejące dane podstawowe produktu z Usług Zarządzania Produktem (PMS) do wstępnego wypełniania pól formularza, tam gdzie ma to zastosowanie.
Internetowe formularze DADI mają na celu umożliwienie bardziej metodycznego przetwarzania wniosków, tym samym zmniejszając obciążenie pracą organizacji. Na przykład, błędy i rozbieżności zostaną zredukowane dzięki formularzom wspierającym weryfikację złożonych wniosków przez Organy ds. Zdrowia. Formularze utorują również drogę dla danych wprowadzanych do baz danych poprawnie za pierwszym razem, czyniąc integrację systemów i wymianę danych między Organami ds. Zdrowia bezproblemową. Ponadto, nowe formularze zastąpią archaiczną technologię.
Korzyści z DADI
Celem DADI i tej transformacji procesów regulacyjnych opartej na danych można podsumować następująco:
- Aby zwiększyć wydajność w obszarach regulacyjnych, badawczo-rozwojowych (R&D) i produkcyjnych.
- Aby szybciej komunikować się z organami ds. zdrowia
- Aby umożliwić podejmowanie decyzji w oparciu o dane zarówno firmom, jak i organom regulacyjnym.
- Aby lepiej zrozumieć i przewidywać wyniki biznesowe oraz ogólną wydajność
W ujęciu całościowym ma to na celu przyniesienie korzyści pacjentom, organom regulacyjnym, a także całej branży.
Najnowsze zmiany w harmonogramie wprowadzone przez EMA
- Data uruchomienia HVF została przesunięta na październik 2022 roku z wcześniej ustalonego terminu w kwietniu 2022 roku.
- Obecnie HVF przechodzi zamknięte testy akceptacyjne użytkowników (UAT) przeprowadzane przez grupę ekspertów merytorycznych ds. DADI.
- Następnie, w drugim kwartale 2022 roku, odbędzie się zintegrowany UAT z udziałem większej grupy różnych interesariuszy.
- Po uruchomieniu nastąpi sześciomiesięczna (06) faza przejściowa, w której równolegle będą akceptowane zarówno eAF (stara wersja PDF), jak i formularze internetowe. Po tym okresie akceptowany będzie wyłącznie HVF.
Prosimy zapoznać się z poniższą infografiką, aby zapoznać się z harmonogramem wdrożenia HVF (Aktualizacja: luty 2022, z zastrzeżeniem zmian wprowadzanych przez EMA):
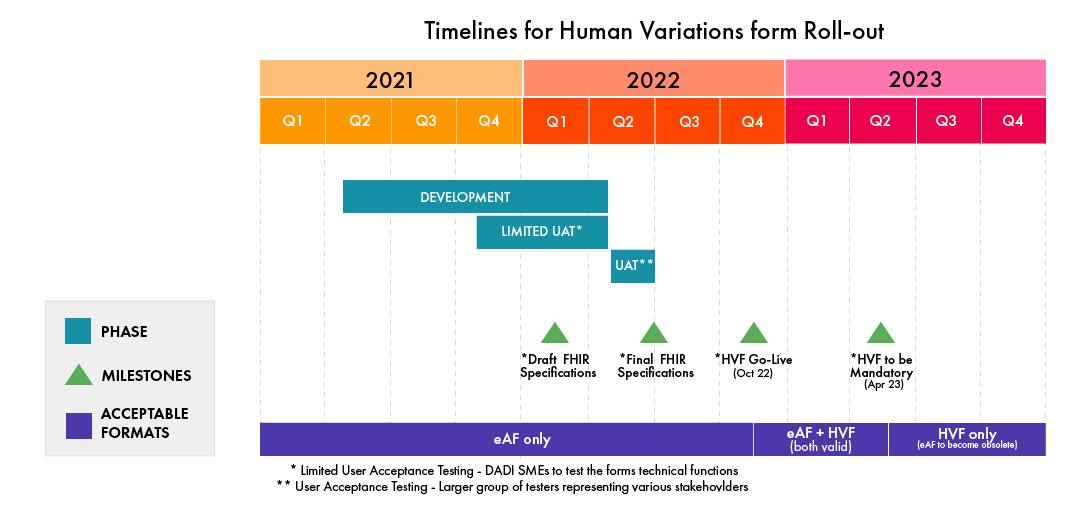
(źródło: EMA)
Zapewnienie elastyczności w dynamicznym środowisku regulacyjnym.
Wszystkie główne Urzędy Zdrowia zmierzają obecnie w kierunku przyjmowania wysokiej jakości zestawów danych i dokumentów. Ważne jest, aby organizacje utrzymywały je w ujednoliconym systemie.
Kluczowe jest również posiadanie jasnego zrozumienia całego cyklu życia zgłoszenia – jego wymagań, związanych z nim osób i procesów, a także aktualnego miejsca przechowywania danych źródłowych, co wymaga dokładnej oceny potrzeb. Czyszczenie i wzbogacanie danych należy traktować priorytetowo, jeśli ocena wskaże taką konieczność.
Konieczne jest posiadanie systemu zarządzania informacjami regulacyjnymi (RIMS), który dostosowuje się do zmieniających się przepisów i wytycznych, a także jest elastyczny, aby dostosować się do bieżących potrzeb organizacji i jest zgodny z dynamicznym środowiskiem regulacyjnym. Aby dowiedzieć się więcej o pakiecie rozwiązań regulacyjnych Freyr, które przygotują Twoją organizację na DADI i inne takie zmiany procesowe, odwiedź nas na Freyr Digital.









