Rozporządzenie Unii Europejskiej w sprawie wyrobów medycznych (EU MDR) 2017/745 definiuje zakres sterylnych wyrobów medycznych jako wyroby, które muszą być wolne od mikroorganizmów (bakterii, wirusów itp.). Wyroby klasy I o funkcji sterylnej mogą również uzyskać samocertyfikację, ale różni się ona pod względem wymagań w porównaniu do innych podkategorii wyrobów klasy I.
Wymagania dotyczące wyrobów klasy I znacznie różnią się w zależności od etapu – od produkcji po wprowadzenie wyrobu na rynek. To samo dotyczy wyrobów medycznych klasy I w warunkach sterylnych. Na przykład, jeśli jest to wyrób klasy I o funkcji sterylnej, wymagania dotyczące produkcji i ustanowienia Systemu Zarządzania Jakością (QMS) będą znacznie różnić się w porównaniu z wyrobami klasy I z funkcjami pomiarowymi.
Celem tego artykułu jest przedstawienie zwięzłej listy kontrolnej do rozważenia podczas wprowadzania do obrotu wyrobu klasy I w warunkach sterylnych w Unii Europejskiej. Lista kontrolna pomoże producentom w podejmowaniu świadomych decyzji dotyczących różnych aspektów.
Co robić!
Poznaj zakres przed produkcją
Zgodnie z EU MDR, wyroby medyczne o funkcjach sterylnych muszą być opracowywane i wytwarzane z zastosowaniem odpowiednich procedur w celu zapewnienia sterylności do momentu wprowadzenia ich do obrotu. Wyroby te mogą być ponownie użyte wyłącznie po odpowiednich procedurach czyszczenia, dezynfekcji i sterylizacji.
Wybór właściwych praktyk sterylizacyjnych
Producent ma do wyboru różne metody sterylizacji wyrobu. Metoda tlenku etylenu (EtO) jest szeroko stosowana do sterylizacji wyrobów medycznych. Wybór metody sterylizacji musi być odpowiednio uzasadniony. Niektóre normy, którymi producenci mogą się kierować przy ustanawianiu, zabezpieczaniu i utrzymywaniu sterylizacji, to EN ISO 14937, ISO TS 21387, ISO TS 13004, ISO 11137 i inne.
Należy również pamiętać, że dokumentacja szczegółowej metody sterylizacji, metody wewnątrzzakładowej i walidacji danych musi być wykonana dokładnie. Informacje dotyczące sterylizacji, takie jak temperatura ogrzewania, warunki pomieszczenia, walidacje procesu itp., muszą być dostarczone zgodnie z wymaganiami EU MDR.
Poznaj wymagania oraz wytyczne, których należy przestrzegać
Jednym z kluczowych kroków jest dokumentowanie wymagań technicznych oraz znajomość norm akceptowanych w ramach EU MDR. Na przykład EN 556 to europejska norma dla wyrobów sterylnych. EN 556 szczegółowo określa wymagania dotyczące uznawania wyrobu medycznego za sterylny. Ponadto ISO TS 19930 określa strategie zapewnienia sterylności wyrobów. Jednakże nie została jeszcze przyjęta jako norma UE.
Poznaj swoją ścieżkę
Przy uzyskiwaniu znaku CE należy zapoznać się z zaangażowaniem Jednostek Notyfikowanych oraz ścieżką oceny zgodności, którą należy wybrać. Dodatkowo, wyroby medyczne w warunkach sterylnych muszą być zgodne z Załącznikami IX i XI.
Zaangażowanie jednostki notyfikowanej jest wymagane, lecz ograniczone. W przypadku wyrobów sterylnych, zaangażowanie jednostek notyfikowanych będzie dotyczyło utrzymania i zapewnienia warunków sterylności. Na przykład, oceny zgodności będą obejmować oceny mikrobiologiczne, metody aseptyczne itp.
Czego nie robić!
Nie przegap wymagań dotyczących pakowania i etykietowania

Istnieją dodatkowe wymagania dotyczące zgodności opakowania i etykietowania w przypadku urządzeń sterylnych. Spełniając wymagania dotyczące opakowania i etykietowania, nie należy zapominać o informacjach, które muszą być umieszczone. Pierwszym i najważniejszym krokiem jest umieszczenie symbolu sterylności (wspomnianego poniżej) na etykiecie urządzenia.
Należy dołączyć informacje takie jak deklaracja sterylności, metoda sterylizacji, instrukcja postępowania w przypadku uszkodzenia lub niezamierzonego otwarcia sterylnego opakowania itp. Ponadto, należy uwzględnić okres trwałości sterylnego produktu oraz proces ponownej sterylizacji (jeśli dotyczy). Numer identyfikacyjny jednostki notyfikowanej powinien być również umieszczony na wyrobie.
Niektóre z symboli, które należy dodać (w zależności od zastosowania) w etykietowaniu sterylnych wyrobów medycznych, to:
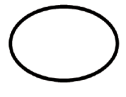
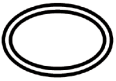
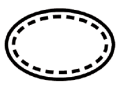
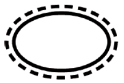
Symbol | Wskazanie |
| Sterylne wyroby medyczne ze sterylizacją metodą aseptyczną |
| Sterylne wyroby medyczne sterylizowane tlenkiem etylenu |
| Sterylne wyroby medyczne ze sterylizacją metodą suchego gorąca lub parą |
| Sterylne wyroby medyczne sterylizowane nadtlenkiem wodoru w fazie gazowej |
| Sterylne wyroby medyczne sterylizowane promieniowaniem |
| Urządzenie nie może być ponownie sterylizowane. |
| Urządzenie nie jest sterylizowane. |
| Nie używaj, jeśli opakowanie jest uszkodzone. |
| Pojedynczy system sterylnej bariery |
| Podwójny system jałowej bariery |
| Pojedynczy system sterylnej bariery z opakowaniem ochronnym wewnątrz |
| Pojedynczy system sterylnej bariery z opakowaniem ochronnym na zewnątrz |
Nie zapomnij o wymaganiach dotyczących okresu po wprowadzeniu na rynek
W przypadku sterylnych wyrobów wymagane jest prowadzenie rejestru zdarzeń niepożądanych. Zarejestrowane incydenty, takie jak dokumenty, muszą być następnie przedstawione przez właściwe organy na żądanie.
EU MDR ma specyficzne wymagania dotyczące samocertyfikacji. Jest to złożona procedura, której głównym czynnikiem są różne klasy w ramach urządzeń klasy I oraz ich różne aspekty wymagań w zakresie uzyskania znaku CE. Producenci urządzeń klasy I w warunkach sterylnych powinni być świadomi określania zakresu i specyficznych wymagań.
Chcesz szczegółowo zrozumieć różne aspekty sterylnych wyrobów klasy I? Chcesz omówić to ze sprawdzonym ekspertem? Skontaktuj się z nami.